Rechazo a los trasplantes renales se asocia con un locus discordante nuevo
|
Por el equipo editorial de LabMedica en español Actualizado el 19 Jun 2019 |

Imagen: El escáner de detección de microarrays NimbleGen MS 200 CGH LOH (Fotografía cortesía de Roche).
Aproximadamente el 20% de la lista de espera de riñones en los Estados Unidos está formada por candidatos cuyos aloinjertos han fallado. El rechazo agudo es uno de los predictores más fuertes de la disminución de la supervivencia del aloinjerto.
En el contexto del trasplante de riñón, las incompatibilidades genómicas entre el donante y el receptor pueden conducir a la alosensibilización contra nuevos antígenos. Se ha identificado una nueva forma de desajuste genético, o “colisión genómica”, entre los receptores de trasplante de riñón y los donantes de órganos que parece aumentar el riesgo de rechazo del aloinjerto.
Un gran equipo de científicos dirigido por los de la Universidad de Columbia (Nueva York, NY, EUA) realizó un estudio de asociación genética, en dos etapas, del rechazo de aloinjerto renal. El objetivo del estudio fue descubrir variantes en el número de copias de alta prioridad que influyen en el rechazo del aloinjerto renal en más de 700 receptores de trasplantes. En particular, se centraron en las llamadas situaciones de colisión genómica, en las que los receptores de trasplantes llevaban dos copias de una deleción que no era homocigótica en el donante de órganos.
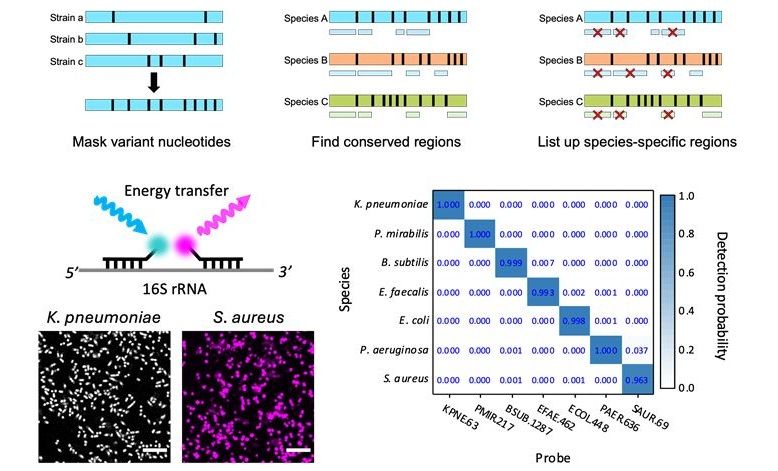
La identificación de los aloanticuerpos se realizó con el uso de arrays de proteínas, ensayos inmunoabsorbentes ligados a enzimas (ELISA) y análisis de transferencia Western blot. El equipo utilizó la hibridación del genoma comparativo basado en arrays de NimbleGen (Madison, WI, EUA) para buscar 50 deleciones sospechosas que afectan a partes del genoma que codifican proteínas en 705 receptores de trasplantes de riñón. A partir de ahí, buscaron asociaciones con el rechazo de aloinjerto renal en un “análisis de supervivencia desde el momento del evento” en los pacientes, a los que se realizó un seguimiento de más de ocho años y medio, en promedio.
En la cohorte de descubrimiento, que incluyó a 705 receptores, encontraron una asociación significativa con el rechazo de aloinjerto en el locus LIMS1 representado por rs893403 (relación de riesgo con el genotipo de riesgo versus genotipos sin riesgo: 1,84). Este efecto se replicó bajo el modelo de colisión genómica en tres cohortes independientes que cubrió un total de 2.004 pares de donantes y receptores (proporción de riesgo: 1,55). En el análisis combinado (cohorte de descubrimiento más cohortes de replicación), el genotipo de riesgo se asoció con un mayor riesgo de rechazo que el genotipo sin riesgo (índice de riesgo, 1,63). El equipo pudo identificar una respuesta de anticuerpos específica contra LIMS1, una proteína expresada en el riñón, codificada dentro del locus de la colisión. La respuesta incluyó predominantemente a las subclases de anticuerpos IgG2 e IgG3.
El equipo obtuvo evidencia adicional para la hipótesis después de un análisis funcional de la variante de riesgo relacionada con el rechazo y experimentos de reactividad serológica que se basaron en datos de arrays de proteínas para cientos de receptores de trasplante de riñón que experimentaron o no un rechazo al aloinjerto. Los autores notaron que la proteína LIMS1 también parece expresarse en otros órganos comúnmente trasplantados, incluyendo el corazón y el pulmón, aunque advirtieron que los estudios de seguimiento serán útiles para determinar si sus hallazgos son generalizables a otros órganos. El estudio fue publicado el 16 de mayo de 2019 en la revista The New England Journal of Medicine.
Enlace relacionado:
Universidad de Columbia
NimbleGen
En el contexto del trasplante de riñón, las incompatibilidades genómicas entre el donante y el receptor pueden conducir a la alosensibilización contra nuevos antígenos. Se ha identificado una nueva forma de desajuste genético, o “colisión genómica”, entre los receptores de trasplante de riñón y los donantes de órganos que parece aumentar el riesgo de rechazo del aloinjerto.
Un gran equipo de científicos dirigido por los de la Universidad de Columbia (Nueva York, NY, EUA) realizó un estudio de asociación genética, en dos etapas, del rechazo de aloinjerto renal. El objetivo del estudio fue descubrir variantes en el número de copias de alta prioridad que influyen en el rechazo del aloinjerto renal en más de 700 receptores de trasplantes. En particular, se centraron en las llamadas situaciones de colisión genómica, en las que los receptores de trasplantes llevaban dos copias de una deleción que no era homocigótica en el donante de órganos.
La identificación de los aloanticuerpos se realizó con el uso de arrays de proteínas, ensayos inmunoabsorbentes ligados a enzimas (ELISA) y análisis de transferencia Western blot. El equipo utilizó la hibridación del genoma comparativo basado en arrays de NimbleGen (Madison, WI, EUA) para buscar 50 deleciones sospechosas que afectan a partes del genoma que codifican proteínas en 705 receptores de trasplantes de riñón. A partir de ahí, buscaron asociaciones con el rechazo de aloinjerto renal en un “análisis de supervivencia desde el momento del evento” en los pacientes, a los que se realizó un seguimiento de más de ocho años y medio, en promedio.
En la cohorte de descubrimiento, que incluyó a 705 receptores, encontraron una asociación significativa con el rechazo de aloinjerto en el locus LIMS1 representado por rs893403 (relación de riesgo con el genotipo de riesgo versus genotipos sin riesgo: 1,84). Este efecto se replicó bajo el modelo de colisión genómica en tres cohortes independientes que cubrió un total de 2.004 pares de donantes y receptores (proporción de riesgo: 1,55). En el análisis combinado (cohorte de descubrimiento más cohortes de replicación), el genotipo de riesgo se asoció con un mayor riesgo de rechazo que el genotipo sin riesgo (índice de riesgo, 1,63). El equipo pudo identificar una respuesta de anticuerpos específica contra LIMS1, una proteína expresada en el riñón, codificada dentro del locus de la colisión. La respuesta incluyó predominantemente a las subclases de anticuerpos IgG2 e IgG3.
El equipo obtuvo evidencia adicional para la hipótesis después de un análisis funcional de la variante de riesgo relacionada con el rechazo y experimentos de reactividad serológica que se basaron en datos de arrays de proteínas para cientos de receptores de trasplante de riñón que experimentaron o no un rechazo al aloinjerto. Los autores notaron que la proteína LIMS1 también parece expresarse en otros órganos comúnmente trasplantados, incluyendo el corazón y el pulmón, aunque advirtieron que los estudios de seguimiento serán útiles para determinar si sus hallazgos son generalizables a otros órganos. El estudio fue publicado el 16 de mayo de 2019 en la revista The New England Journal of Medicine.
Enlace relacionado:
Universidad de Columbia
NimbleGen
Últimas Diagnóstico Molecular noticias
- Prueba de biomarcadores sanguíneos podría detectar predisposición genética al Alzheimer
- Se descubre nuevo autoanticuerpo contra DAGLA en cerebelitis
- Análisis de sangre podría identificar a pacientes con riesgo de esclerodermia grave
- Prueba de sangre basada en genes predice recurrencia del cáncer de piel avanzado
- Prueba de sangre rápida identifica pacientes presintomáticos con enfermedad de Parkinson
- Análisis de sangre para detección temprana del Alzheimer con precisión de 90 %
- Prueba basada en ARN detecta riesgo de preeclampsia antes de síntomas
- Primera prueba que utiliza microARN para predecir toxicidad de terapia contra el cáncer
- Ensayo basado en células proporciona detección sensible y específica de autoanticuerpos en desmielinización
- Novedosa tecnología en POC ofrece resultados precisos del VIH en minutos
- Análisis de sangre descarta riesgo futuro de demencia
- Prueba de dímero D puede identificar pacientes con mayor riesgo de embolia pulmonar
- Nuevos biomarcadores mejoran la detección temprana y seguimiento de la lesión renal
- Inmunoensayos de quimioluminiscencia respaldan diagnóstico de Alzheimer
- Análisis de sangre identifica múltiples biomarcadores para diagnóstico rápido de lesiones de médula espinal
- Análisis de sangre muy preciso diagnostica Alzheimer y mide progresión de demencia
Canales
Química Clínica
ver canal
Herramienta química a nanoescala 'brillantemente luminosa' mejora detección de enfermedades
Miles de moléculas brillantes disponibles comercialmente, conocidas como fluoróforos, se utilizan comúnmente en imágenes médicas, detección de enfermedades, marcado... Más
Prueba de detección portátil económica transforma detección de enfermedades renales
Millones de personas padecen enfermedad renal, que a menudo permanece sin diagnosticar hasta que alcanza una etapa crítica. Esta epidemia silenciosa no solo disminuye la calidad de vida de los afectados,... MásHematología
ver canal
Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
La citopenia clonal de significado incierto (CCSI) es un trastorno sanguíneo común en adultos mayores, caracterizado por mutaciones en las células sanguíneas y un recuento ... Más
Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
En los Estados Unidos, aproximadamente el 15 % de las embarazadas son RhD negativas. Sin embargo, en aproximadamente el 40 % de estos casos, el feto también es RhD negativo, lo que hace innecesaria la... MásInmunología
ver canal
Prueba de células madre predice resultado del tratamiento en cáncer de ovario resistente al platino
El cáncer de ovario epitelial suele responder inicialmente a la quimioterapia, pero con el tiempo, el tumor desarrolla resistencia a la terapia, lo que provoca su recrecimiento. Esta resistencia... Más
Análisis de sangre con aprendizaje automático predice respuesta a inmunoterapia en pacientes con linfoma
La terapia de células T con receptores de antígenos quiméricos (CAR) se ha convertido en uno de los avances recientes más prometedores en el tratamiento de los cánceres... MásMicrobiología
ver canal
Dispositivo portátil ofrece resultados de tuberculosis económico y rápido
La tuberculosis (TB) sigue siendo la enfermedad infecciosa más mortal a nivel mundial, afectando a aproximadamente 10 millones de personas al año. En 2021, alrededor de 4,2 millones de casos... Más
Método basado en IA mejora diagnóstico de infecciones resistentes a fármacos
Las infecciones resistentes a los medicamentos, en particular las causadas por bacterias mortales como la tuberculosis y el estafilococo, se están convirtiendo rápidamente en una emergencia... MásPatología
ver canal
Nuevo método basado en aprendizaje automático detecta contaminación microbiana en cultivos celulares
La terapia celular tiene un gran potencial en el tratamiento de enfermedades como el cáncer, las enfermedades inflamatorias y los trastornos degenerativos crónicos mediante la manipulación o el reemplazo... Más
Nuevo método con corrección de errores detecta cáncer únicamente en muestras de sangre
La tecnología de biopsia líquida, que se basa en análisis de sangre para la detección temprana del cáncer y el seguimiento de la carga oncológica en los pacientes,... MásTecnología
ver canal
Tecnología de microchip desechable podría detectar selectivamente VIH en muestras de sangre completa
A finales de 2023, aproximadamente 40 millones de personas en todo el mundo vivían con VIH, y alrededor de 630.000 personas murieron por enfermedades relacionadas con el sida ese mismo año.... Más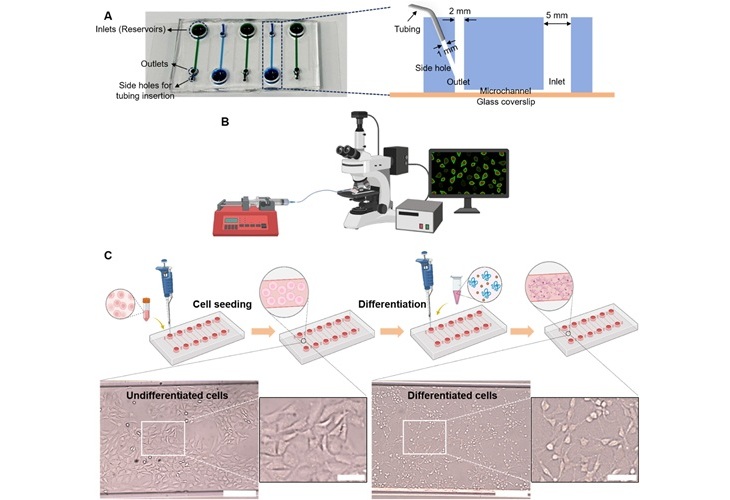
Dispositivo microfluídico Dolor en un Chip determina tipos de dolor crónico desde muestras de sangre
El dolor crónico es una afección generalizada que sigue siendo difícil de controlar, y los métodos clínicos existentes para su tratamiento se basan en gran medida en... MásIndustria
ver canal
Cepheid y Oxford Nanopore se unen para desarrollar soluciones con secuenciación automatizada
Cepheid (Sunnyvale, CA, EUA), una empresa líder en diagnóstico molecular, y Oxford Nanopore Technologies (Oxford, Reino Unido), la empresa detrás de una nueva generación de... Más