Asocian mutaciones de Mycobacterium con resistencia a la claritromicina
|
Por el equipo editorial de LabMedica en español Actualizado el 29 Jan 2018 |
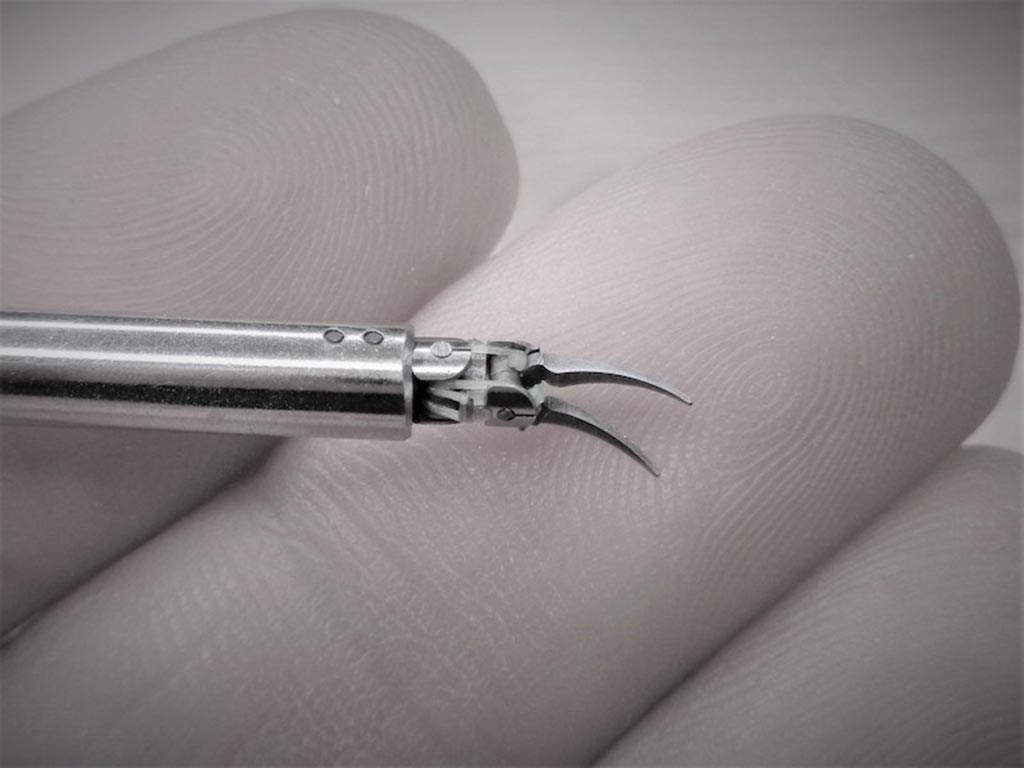
Imagen: El sistema de lectura de placa fluorométrica automatizado, Sensititre OptiRead, para uso con placas de microtitulación Sensititre en las pruebas de susceptibilidad a los antibióticos (Fotografía cortesía de Thermo Fisher Scientific).
La bacteria Mycobacterium abscessus es la principal causa de enfermedades respiratorias y de infecciones de los tejidos blandos y tiene una resistencia natural a muchos antibióticos in vitro, lo que complica el tratamiento clínico y conduce a resultados insatisfactorios.
Los macrólidos, como la claritromicina y la azitromicina, son considerados como la base del régimen terapéutico para las infecciones complejas por M. abscessus. Sin embargo, la resistencia a la claritromicina está aumentando dramáticamente entre el complejo de M. abscessus.
Los microbiólogos de la Facultad de Medicina de la Universidad de Tongji (Shanghái, China), recolectaron muestras del Hospital Pulmonar afiliado de Shanghái y se usaron una colección de 139 aislados clínicos de M. abscessus subsp. abscessus y 36 de M. abscessus subsp. massiliense para explorar la utilidad de la técnica de la reacción en cadena de la polimerasa-electroforesis en gel de gradiente de desnaturalización (PCR-DGGE) para la identificación rápida del ARNr 23S (Adenina (2058) -N (6)) - metiltransferasa Erm (41) (erm (41) y las mutaciones del gen 23S rARN (rrl).
El equipo diseñó cuatro conjuntos de cebadores para buscar mutaciones en los genes erm (41) y rrl usando DGGE. Las reacciones de PCR y la electroforesis, así como la recuperación de las bandas y el análisis en gel, se realizaron según los protocolos descritos previamente. Se usó un panel Sensititre RAPMYCO (TREK Diagnostic Systems, East Grinstead, Reino Unido) para probar la susceptibilidad de varios antibióticos, incluida la claritromicina contra los aislados del complejo 175 M. abscessus.
Los autores encontraron una combinación de 16 patrones diferentes de DGGE para el gen erm (41), incluyendo 16 en M. abscessus subsp. abscessus y uno en M. abscessus subsp. massiliense. Se obtuvieron seis patrones de DGGE para el gen rrl. Las mutaciones en los genes erm (41) y rrl detectadas por DGGE fueron 100% idénticas a las mutaciones detectadas por secuenciación de ADN. Entre los 139 aislados de M. abscessus subsp. abscessus, 36 aislamientos exhibieron resistencia a la claritromicina en el día 5. Los otros 103 fueron sensibles a la claritromicina en el día 5 y 83 de estos mostraron resistencia inducible después de 14 días de incubación. De los 36 aislados de M. abscessus subsp. massiliense, 27 fueron sensibles y ocho fueron resistentes a la claritromicina en los días 5 y 14. Cabe destacar que uno de los aislados fue sensible a la claritromicina el día 5 pero mostró resistencia inducible el día 14.
Los autores concluyeron que sus resultados demostraron que la tecnología DGGE es muy sensible a las mutaciones puntuales, así como a las pequeñas inserciones y deleciones en las secuencias de ADN. La exactitud fue esencialmente del 100% entre los fragmentos dirigidos de los genes erm (41) y rrl. Los resultados de la secuenciación del genoma completo confirmaron la eficacia de DGGE; se detectaron todos los polimorfismos de nucleótidos distintos. La PCR basada en DGGE es una técnica práctica para la detección rápida de mutaciones en los genes erm (41) y rrl, asociados con la resistencia a la claritromicina en el complejo de M. abscessus. El estudio fue publicado en la edición de diciembre de 2017 de la revista Journal of Microbiological Methods.
Los macrólidos, como la claritromicina y la azitromicina, son considerados como la base del régimen terapéutico para las infecciones complejas por M. abscessus. Sin embargo, la resistencia a la claritromicina está aumentando dramáticamente entre el complejo de M. abscessus.
Los microbiólogos de la Facultad de Medicina de la Universidad de Tongji (Shanghái, China), recolectaron muestras del Hospital Pulmonar afiliado de Shanghái y se usaron una colección de 139 aislados clínicos de M. abscessus subsp. abscessus y 36 de M. abscessus subsp. massiliense para explorar la utilidad de la técnica de la reacción en cadena de la polimerasa-electroforesis en gel de gradiente de desnaturalización (PCR-DGGE) para la identificación rápida del ARNr 23S (Adenina (2058) -N (6)) - metiltransferasa Erm (41) (erm (41) y las mutaciones del gen 23S rARN (rrl).
El equipo diseñó cuatro conjuntos de cebadores para buscar mutaciones en los genes erm (41) y rrl usando DGGE. Las reacciones de PCR y la electroforesis, así como la recuperación de las bandas y el análisis en gel, se realizaron según los protocolos descritos previamente. Se usó un panel Sensititre RAPMYCO (TREK Diagnostic Systems, East Grinstead, Reino Unido) para probar la susceptibilidad de varios antibióticos, incluida la claritromicina contra los aislados del complejo 175 M. abscessus.
Los autores encontraron una combinación de 16 patrones diferentes de DGGE para el gen erm (41), incluyendo 16 en M. abscessus subsp. abscessus y uno en M. abscessus subsp. massiliense. Se obtuvieron seis patrones de DGGE para el gen rrl. Las mutaciones en los genes erm (41) y rrl detectadas por DGGE fueron 100% idénticas a las mutaciones detectadas por secuenciación de ADN. Entre los 139 aislados de M. abscessus subsp. abscessus, 36 aislamientos exhibieron resistencia a la claritromicina en el día 5. Los otros 103 fueron sensibles a la claritromicina en el día 5 y 83 de estos mostraron resistencia inducible después de 14 días de incubación. De los 36 aislados de M. abscessus subsp. massiliense, 27 fueron sensibles y ocho fueron resistentes a la claritromicina en los días 5 y 14. Cabe destacar que uno de los aislados fue sensible a la claritromicina el día 5 pero mostró resistencia inducible el día 14.
Los autores concluyeron que sus resultados demostraron que la tecnología DGGE es muy sensible a las mutaciones puntuales, así como a las pequeñas inserciones y deleciones en las secuencias de ADN. La exactitud fue esencialmente del 100% entre los fragmentos dirigidos de los genes erm (41) y rrl. Los resultados de la secuenciación del genoma completo confirmaron la eficacia de DGGE; se detectaron todos los polimorfismos de nucleótidos distintos. La PCR basada en DGGE es una técnica práctica para la detección rápida de mutaciones en los genes erm (41) y rrl, asociados con la resistencia a la claritromicina en el complejo de M. abscessus. El estudio fue publicado en la edición de diciembre de 2017 de la revista Journal of Microbiological Methods.
Últimas Microbiología noticias
- Innovadora plataforma de diagnóstico proporciona resultados de AST con velocidad sin precedentes
- Análisis de sangre predice sepsis e insuficiencia orgánica en niños
- Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
- Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
- Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
- Nuevo análisis para tuberculosis podría ampliar acceso a pruebas en países de ingresos bajos y medios
- Prueba rápida diagnostica enfermedades tropicales en horas para tratamiento con antibióticos más rápido
- Pruebas moleculares rápidas permiten tratamiento antibiótico más rápido y específico para neumonía
- Plataforma rápida de PSA proporciona resultados terapéuticos específicos días antes que el estándar de atención actual
- Nuevo método de análisis detecta patógenos en sangre de forma más rápida y precisa al fundir ADN
- Prueba rápida de sepsis ofrece resultados dos días más rápidos
- Diagnóstico rápido portátil por PCR podría detectar gonorrea y susceptibilidad a antibióticos
- Prueba CRISPR diagnostica mpox más rápido que método de PCR de laboratorio
- Prueba de PCR multiplexada para detección de patógenos y resistencia a antibióticos ayuda a brindar un tratamiento rápido de ITU
- Nuevo algoritmo detecta e identifica nuevos organismos bacterianos
- Analizador de mesa promete detección de ITU en 1 hora e indicación de sensibilidad a antibióticos
Canales
Química Clínica
ver canal
Espectrómetro de masas impreso en 3D para el punto de atención supera a los modelos de última generación
La espectrometría de masas es una técnica precisa para identificar los componentes químicos de una muestra y tiene un potencial significativo para monitorear estados de salud de enfermedades... Más.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal.jpeg)
Ensayo de aprendizaje automático basado en sangre detecta de forma no invasiva el cáncer de ovario
El cáncer de ovario es una de las causas más comunes de muerte por cáncer entre las mujeres y tiene una tasa de supervivencia a cinco años de alrededor del 50%.... Más
Ensayo de PCR simple diferencia con precisión entre los subtipos de cáncer de pulmón de células pequeñas
El cáncer de pulmón de células pequeñas (CPCP), una neoplasia maligna neuroendocrina que progresa rápidamente, presenta bajas tasas de supervivencia. A pesar de su heterogeneidad molecular y clínica, el... MásHematología
ver canal
Primera prueba NAT 4 en 1 para el cribado de arbovirus podría reducir el riesgo de infecciones transmitidas por transfusiones
Los arbovirus representan una amenaza emergente para la salud mundial, exacerbada por el cambio climático y el aumento de la conectividad mundial que está facilitando su propagación a nuevas regiones.... Más
Instrumento de próxima generación detecta trastornos de la hemoglobina en recién nacidos
Las hemoglobinopatías, las enfermedades hereditarias más extendidas a nivel mundial, afectan a alrededor del 7 % de la población como portadores, y el 2,7 % de los recién nacidos nacen con estas enfermedades.... Más
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásPatología
ver canal
Biopsia de piel virtual determina la presencia de células cancerosas
Cuando los dermatólogos detectan una marca inusual en la piel de un paciente, se enfrentan a una elección: controlarla durante algún tiempo o extraerla para realizar una biopsia.... Más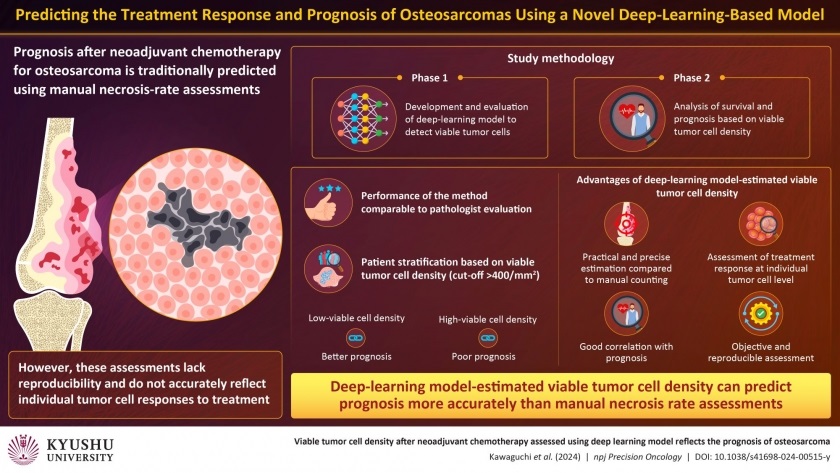
Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico... Más
Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
La comunidad médica mundial reconoce cada vez más que la biopsia líquida es un enfoque transformador para mejorar la atención al paciente con cáncer. Este innovador método de diagnóstico implica detectar... MásTecnología
ver canal
Nuevo sistema de diagnóstico de laboratorio en un chip iguala la precisión de las pruebas de PCR
Si bien las pruebas de PCR son el estándar de oro en cuanto a precisión para las pruebas de virología, tienen limitaciones como la complejidad, la necesidad de operadores de laboratorio capacitados y tiempos... Más
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más













.jpg)


