Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
Actualizado el 03 May 2024
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico del osteosarcoma metastásico avanzado sigue siendo desalentador. Los métodos tradicionales de pronóstico posterior al tratamiento, basados en la evaluación de la necrosis o la evaluación de la proporción de tejido muerto dentro del tumor, sufren de variabilidad entre observadores y podrían no predecir con precisión la respuesta al tratamiento. Ahora los investigadores han desarrollado y validado un modelo de aprendizaje automático capaz de evaluar con precisión la densidad de células tumorales supervivientes en imágenes patológicas de osteosarcoma, ofreciendo una predicción de pronóstico más fiable.
El modelo, desarrollado por investigadores de la Universidad de Kyushu (Fukuoka, Japón), utiliza algoritmos de aprendizaje profundo para identificar células tumorales viables dentro de imágenes patológicas, coincidiendo con las habilidades de evaluación de patólogos expertos. Este enfoque supera las limitaciones del método tradicional para la evaluación de la tasa de necrosis, que calcula el área necrótica sin considerar el recuento de células individuales, lo que genera evaluaciones inconsistentes entre patólogos y una reflexión inadecuada de los efectos de la quimioterapia. En la fase 1 del estudio, el equipo entrenó el modelo de aprendizaje profundo para detectar células tumorales supervivientes y validó su rendimiento utilizando datos de pacientes. El modelo de IA fue tan competente en la detección de células tumorales viables en imágenes patológicas como los patólogos expertos.
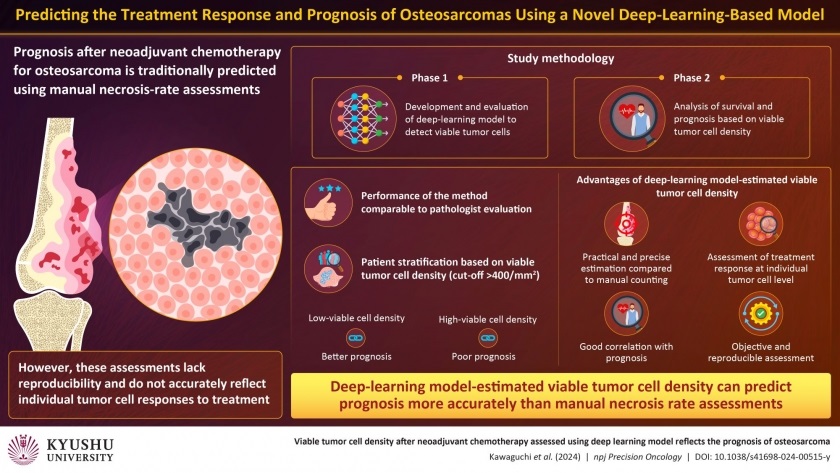
En la fase 2, los investigadores se centraron en la supervivencia específica de la enfermedad y la supervivencia libre de metástasis. Mientras que la supervivencia específica de la enfermedad rastrea la duración después del diagnóstico o tratamiento sin muerte causada directamente por la enfermedad, la supervivencia libre de metástasis monitorea el tiempo posterior al tratamiento sin que las células cancerosas se propaguen a partes distantes del cuerpo. También examinaron la correlación entre la densidad de células tumorales viables estimada por IA y el pronóstico. Los hallazgos revelaron que el rendimiento de detección y la precisión del modelo de IA eran comparables a los del patólogo, además de una buena reproducibilidad. Luego, el equipo dividió a los pacientes en grupos según si la densidad de células tumorales viables era superior o inferior a 400/mm2. Descubrieron que una mayor densidad se correlacionaba con un peor pronóstico, mientras que una menor densidad indicaba un mejor resultado.
El equipo descubrió que la tasa de necrosis no se asociaba con la supervivencia específica de la enfermedad ni con la supervivencia libre de metástasis. Un análisis más detallado de casos individuales mostró que la densidad de células tumorales viables estimada por IA es un predictor de pronóstico más confiable que la tasa de necrosis. Estos hallazgos sugieren que al incorporar IA en el análisis de imágenes patológicas, este método mejora la precisión de la detección, minimiza la variabilidad entre los evaluadores y ofrece evaluaciones rápidas. La estimación de la densidad de células tumorales viables, que indica el potencial de proliferación de las células después de la quimioterapia, surge como un indicador superior de la eficacia del tratamiento sobre la evaluación tradicional de la tasa de necrosis. Este modelo de IA promete avances significativos en entornos clínicos después de una validación más amplia para facilitar su aplicación generalizada.
"Este nuevo enfoque tiene el potencial de mejorar la precisión del pronóstico de los pacientes con osteosarcoma tratados con quimioterapia", afirmó el Dr. Makoto Endo, profesor de Cirugía Ortopédica en el Hospital Universitario de Kyushu. “En el futuro, pretendemos aplicar activamente la IA a enfermedades raras como el osteosarcoma, que han experimentado avances limitados en epidemiología, patogénesis y etiología. A pesar del paso de las décadas, particularmente en las estrategias de tratamiento, sigue siendo difícil lograr avances sustanciales. Al aplicar la IA al problema, esto finalmente podría cambiar”.
Enlaces relacionados:
Universidad de Kyushu