Biomarcadores en suero diferencian la COVID-19 de los síndromes clásicos de tormenta de citoquinas
|
Por el equipo editorial de LabMedica en español Actualizado el 15 Jun 2021 |

Imagen: Los kits ELISA Quantikine están disponibles en una variedad de formatos para medir proteínas intracelulares y extracelulares (Fotografía cortesía de R&D Systems)
Una tormenta de citoquinas, también llamada hipercitoquinemia, es una reacción fisiológica en humanos y otros animales en la que el sistema inmunológico innato provoca una liberación incontrolada y excesiva de moléculas de señalización proinflamatorias llamadas citoquinas.
La infección por el nuevo coronavirus SARS-CoV-2 desencadena una enfermedad grave con alta mortalidad en un subgrupo de pacientes. Se cree que este curso crítico de la enfermedad por coronavirus (COVID-19) se asocia con la tormenta de citoquinas como en el síndrome de activación de macrófagos o la linfohistiocitosis hemofagocítica secundaria.
Un equipo internacional de reumatólogos e inmunólogos pediátricos dirigido por el equipo del Hospital Infantil Universitario de Muenster (Muenster, Alemania), examinó si la activación inmune en la COVID-19 imitaba las condiciones observadas en la linfohistiocitosis hemofagocítica secundaria (sHLH) o síndrome de activación de macrófagos (MAS), ambos síndromes clásicos de tormenta de citoquinas, y analizaron 83 muestras de suero de 30 pacientes con COVID-19. El equipo también incluyó 20 muestras de suero de sHLH, así como 17 muestras de MAS relacionadas con la enfermedad de Still del adulto. Estas muestras de suero se obtuvieron de adultos en estudios anteriores. Mientras tanto, se recolectaron cuatro muestras de sHLH juveniles y nueve de MAS juveniles, así como nueve de controles sanos.
Los científicos utilizaron un ensayo de matriz de perlas, así como un ELISA de marcador único, para cuantificar los niveles de 22 biomarcadores en las muestras de suero incluidas. Estos incluyeron IL-1, antagonista del receptor de IL-1 (Ra), IL-4, IL-6, IL-8, IL-10, IL-18, TNF, interferón (IFN), IFN, IFN-, MCP2 (CCL8), MCP3 (CCL7), CXCL9, CXCL10, MCSF, LRG1, ligando Fas soluble (sFasL), molécula de adhesión intracelular 1 (ICAM-1), VCAM-1 y Galectina-3 (R&D Systems, Minneapolis, MN, EUA). La adquisición y el análisis de datos se realizaron en un instrumento MAGPIX (Merck Millipore, Darmstadt, Alemania).
Los científicos observaron una activación espectacular en sHLH/MAS del eje interleuquina (IL) -18-interferón (IFN) -γ, mientras que se aumentaron los niveles séricos del antagonista del receptor de IL-1 (IL-1Ra), de la molécula de adhesión intracelular 1 (ICAM-1 ) y de la IL-8, así como niveles fuertemente reducidos de ligando Fas soluble (sFasL) en el curso de la infección por SARS-CoV-2 que discrimina la mala regulación inmune en la COVID-19 crítica de las condiciones de tormenta de citoquinas bien reconocidas ya investigadas.
Christoph Kessel, PhD, autor principal del estudio, dijo: “Nuestros análisis pueden generar dudas sobre la eficacia de los ensayos clínicos dirigidos a moléculas y vías clave asociadas con sHLH y/o MAS en el tratamiento de la COVID-19. El bloqueo terapéutico de IFN-, que aparece como una opción terapéutica prometedora en el tratamiento de la HLH y potencialmente también el MAS, puede ser menos efectivo en la COVID-19, ya que la activación general del eje IL-18-IFN- parece mucho menos pronunciada en el contexto de la infección por SARS-CoV-2. En contraste con la IL-18 y el IFN-, los niveles de IL-1Ra en la COVID-19 están sustancialmente elevados”.
Los autores concluyeron que los perfiles de biomarcadores séricos separan claramente a la COVID-19 del MAS o del sHLH, lo que cuestiona la importancia de la hiperinflamación sistémica después de la infección por SARS-CoV-2, así como la eficacia de los fármacos dirigidos a moléculas clave y vías específicamente asociadas con las condiciones de tormenta de citoquinas sistémicas en el tratamiento de la COVID-19. El estudio se publicó originalmente el 20 de abril de 2021 en la revista Arthritis & Rheumatology.
Enlace relacionado:
Hospital Infantil Universitario de Muenster
R&D Systems
La infección por el nuevo coronavirus SARS-CoV-2 desencadena una enfermedad grave con alta mortalidad en un subgrupo de pacientes. Se cree que este curso crítico de la enfermedad por coronavirus (COVID-19) se asocia con la tormenta de citoquinas como en el síndrome de activación de macrófagos o la linfohistiocitosis hemofagocítica secundaria.
Un equipo internacional de reumatólogos e inmunólogos pediátricos dirigido por el equipo del Hospital Infantil Universitario de Muenster (Muenster, Alemania), examinó si la activación inmune en la COVID-19 imitaba las condiciones observadas en la linfohistiocitosis hemofagocítica secundaria (sHLH) o síndrome de activación de macrófagos (MAS), ambos síndromes clásicos de tormenta de citoquinas, y analizaron 83 muestras de suero de 30 pacientes con COVID-19. El equipo también incluyó 20 muestras de suero de sHLH, así como 17 muestras de MAS relacionadas con la enfermedad de Still del adulto. Estas muestras de suero se obtuvieron de adultos en estudios anteriores. Mientras tanto, se recolectaron cuatro muestras de sHLH juveniles y nueve de MAS juveniles, así como nueve de controles sanos.
Los científicos utilizaron un ensayo de matriz de perlas, así como un ELISA de marcador único, para cuantificar los niveles de 22 biomarcadores en las muestras de suero incluidas. Estos incluyeron IL-1, antagonista del receptor de IL-1 (Ra), IL-4, IL-6, IL-8, IL-10, IL-18, TNF, interferón (IFN), IFN, IFN-, MCP2 (CCL8), MCP3 (CCL7), CXCL9, CXCL10, MCSF, LRG1, ligando Fas soluble (sFasL), molécula de adhesión intracelular 1 (ICAM-1), VCAM-1 y Galectina-3 (R&D Systems, Minneapolis, MN, EUA). La adquisición y el análisis de datos se realizaron en un instrumento MAGPIX (Merck Millipore, Darmstadt, Alemania).
Los científicos observaron una activación espectacular en sHLH/MAS del eje interleuquina (IL) -18-interferón (IFN) -γ, mientras que se aumentaron los niveles séricos del antagonista del receptor de IL-1 (IL-1Ra), de la molécula de adhesión intracelular 1 (ICAM-1 ) y de la IL-8, así como niveles fuertemente reducidos de ligando Fas soluble (sFasL) en el curso de la infección por SARS-CoV-2 que discrimina la mala regulación inmune en la COVID-19 crítica de las condiciones de tormenta de citoquinas bien reconocidas ya investigadas.
Christoph Kessel, PhD, autor principal del estudio, dijo: “Nuestros análisis pueden generar dudas sobre la eficacia de los ensayos clínicos dirigidos a moléculas y vías clave asociadas con sHLH y/o MAS en el tratamiento de la COVID-19. El bloqueo terapéutico de IFN-, que aparece como una opción terapéutica prometedora en el tratamiento de la HLH y potencialmente también el MAS, puede ser menos efectivo en la COVID-19, ya que la activación general del eje IL-18-IFN- parece mucho menos pronunciada en el contexto de la infección por SARS-CoV-2. En contraste con la IL-18 y el IFN-, los niveles de IL-1Ra en la COVID-19 están sustancialmente elevados”.
Los autores concluyeron que los perfiles de biomarcadores séricos separan claramente a la COVID-19 del MAS o del sHLH, lo que cuestiona la importancia de la hiperinflamación sistémica después de la infección por SARS-CoV-2, así como la eficacia de los fármacos dirigidos a moléculas clave y vías específicamente asociadas con las condiciones de tormenta de citoquinas sistémicas en el tratamiento de la COVID-19. El estudio se publicó originalmente el 20 de abril de 2021 en la revista Arthritis & Rheumatology.
Enlace relacionado:
Hospital Infantil Universitario de Muenster
R&D Systems
Últimas Microbiología noticias
- Prueba de PCR múltiplex identifica el 95 % de los patógenos que causan la sepsis en una hora
- Prueba de bacterias bucales podría predecir la progresión del cáncer de colon
- Firma metabólica unica podría permitir el diagnóstico de sepsis dentro de una hora de la extracción de sangre
- Innovadora plataforma de diagnóstico proporciona resultados de AST con velocidad sin precedentes
- Análisis de sangre predice sepsis e insuficiencia orgánica en niños
- Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
- Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
- Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
- Nuevo análisis para tuberculosis podría ampliar acceso a pruebas en países de ingresos bajos y medios
- Prueba rápida diagnostica enfermedades tropicales en horas para tratamiento con antibióticos más rápido
- Pruebas moleculares rápidas permiten tratamiento antibiótico más rápido y específico para neumonía
- Plataforma rápida de PSA proporciona resultados terapéuticos específicos días antes que el estándar de atención actual
- Nuevo método de análisis detecta patógenos en sangre de forma más rápida y precisa al fundir ADN
- Prueba rápida de sepsis ofrece resultados dos días más rápidos
- Diagnóstico rápido portátil por PCR podría detectar gonorrea y susceptibilidad a antibióticos
- Prueba CRISPR diagnostica mpox más rápido que método de PCR de laboratorio
Canales
Química Clínica
ver canal
Espectrómetro de masas impreso en 3D para el punto de atención supera a los modelos de última generación
La espectrometría de masas es una técnica precisa para identificar los componentes químicos de una muestra y tiene un potencial significativo para monitorear estados de salud de enfermedades... Más.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal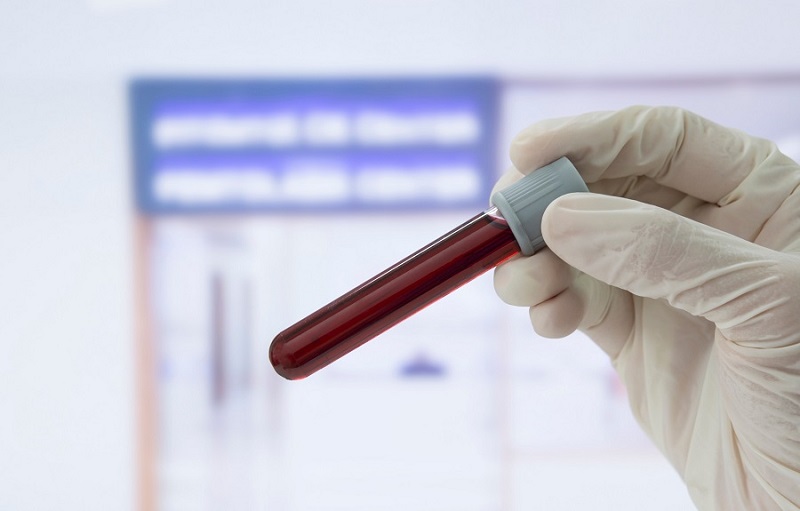
Prueba de sangre predice con precisión el riesgo de cáncer de pulmón y reduce la necesidad de escaneos de TC
El cáncer de pulmón es extremadamente difícil de detectar tempranamente debido a las limitaciones de las tecnologías de detección actuales, que son costosas, a veces... Más
Firma única de autoanticuerpos ayuda a diagnosticar la esclerosis múltiple años antes de la aparición de síntomas
Se cree que las enfermedades autoinmunes como la esclerosis múltiple (EM) ocurren en parte debido a respuestas inmunes inusuales a infecciones comunes. Los primeros síntomas de la EM, incluidos... Más
Prueba de sangre podría detectar cánceres asociados al VPH 10 años antes del diagnóstico clínico
Se sabe que el virus del papiloma humano (VPH) causa varios cánceres, incluidos los de genitales, ano, boca, garganta y cuello uterino. El cáncer orofaríngeo asociado al VPH (VPH+COF)... Más
Un diagnóstico de bajo costo en el punto de atención ampliará el acceso a pruebas de enfermedades de transmisión sexual
La gonorrea es la segunda infección bacteriana de transmisión sexual (ITS) más comúnmente reportada, con alrededor de 82 millones de casos en todo el mundo en 2020. La infección puede tener graves consecuencias... MásHematología
ver canal
Primera prueba NAT 4 en 1 para el cribado de arbovirus podría reducir el riesgo de infecciones transmitidas por transfusiones
Los arbovirus representan una amenaza emergente para la salud mundial, exacerbada por el cambio climático y el aumento de la conectividad mundial que está facilitando su propagación a nuevas regiones.... Más
Instrumento de próxima generación detecta trastornos de la hemoglobina en recién nacidos
Las hemoglobinopatías, las enfermedades hereditarias más extendidas a nivel mundial, afectan a alrededor del 7 % de la población como portadores, y el 2,7 % de los recién nacidos nacen con estas enfermedades.... Más
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásMicrobiología
ver canal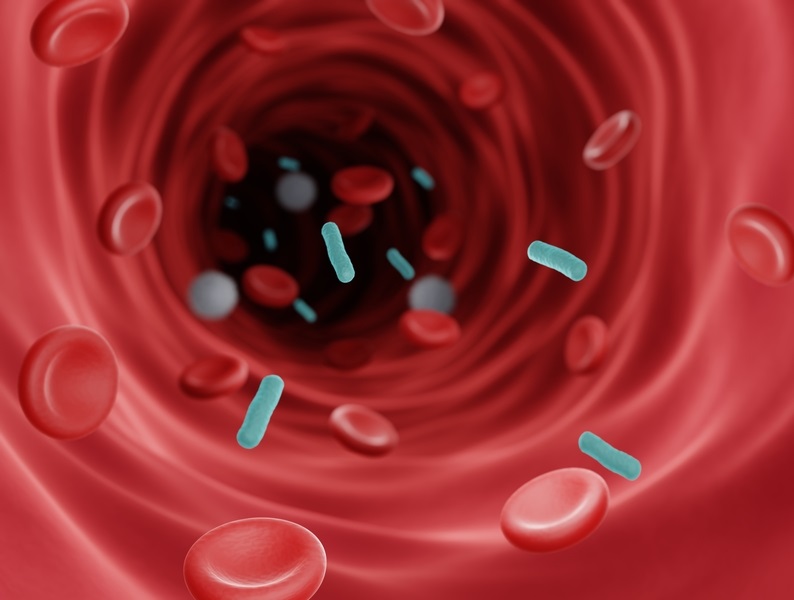
Prueba de PCR múltiplex identifica el 95 % de los patógenos que causan la sepsis en una hora
La sepsis contribuye a una de cada tres muertes hospitalarias en los Estados Unidos y, a nivel mundial, el shock séptico conlleva una tasa de mortalidad del 30 al 40 %. El diagnóstico temprano... Más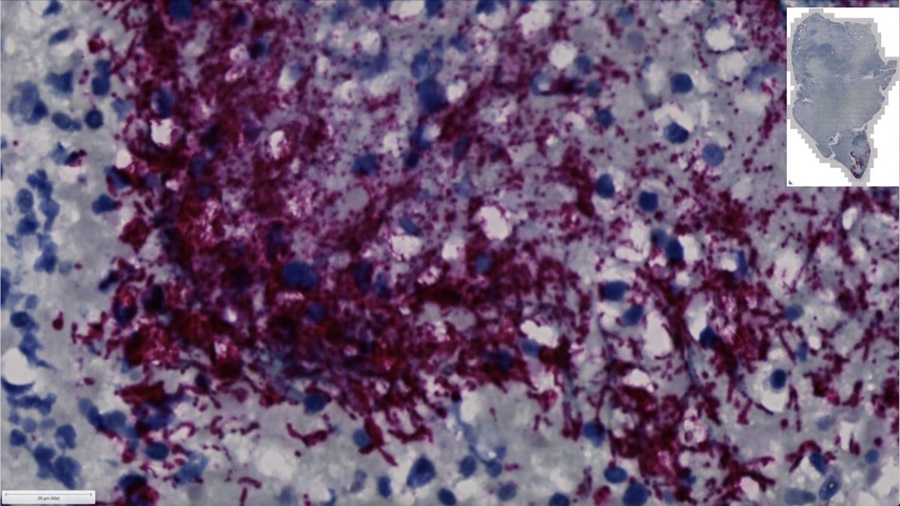
Prueba de bacterias bucales podría predecir la progresión del cáncer de colon
El cáncer de colon, una enfermedad relativamente común pero difícil de diagnosticar, requiere confirmación mediante una colonoscopia o cirugía. Recientemente, ha habido... Más.jpg)
Firma metabólica unica podría permitir el diagnóstico de sepsis dentro de una hora de la extracción de sangre
La sepsis es una afección potencialmente mortal provocada por una respuesta extrema del cuerpo a una infección. Requiere intervención médica inmediata para evitar una posible muerte o daños duraderos.... Más
Innovadora plataforma de diagnóstico proporciona resultados de AST con velocidad sin precedentes
Una plataforma de diagnóstico innovadora que ofrece resultados de pruebas de susceptibilidad a los antibióticos (AST) con una velocidad sin precedentes puede convertirse en una herramienta importante para... MásPatología
ver canal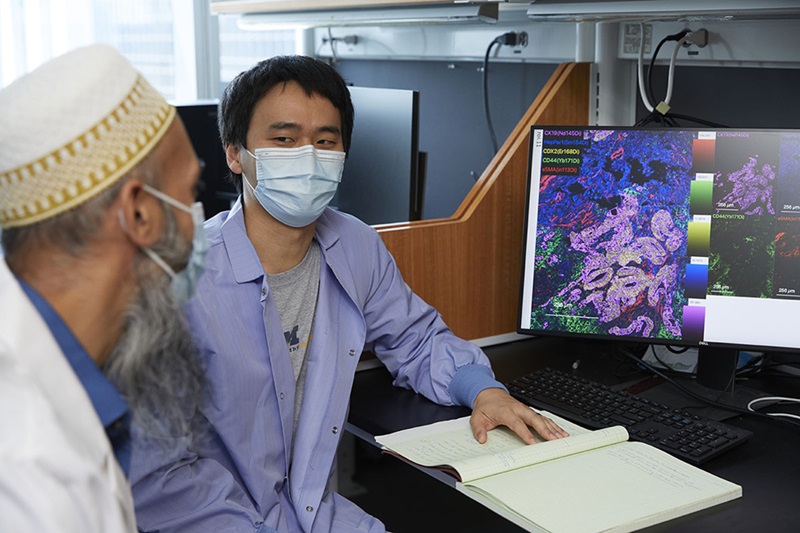
Análisis de tejido espacial identifica patrones asociados con la recaída del cáncer de ovario
El carcinoma de ovario seroso de alto grado es el tipo más letal de cáncer de ovario y plantea importantes desafíos de detección. Por lo general, los pacientes responden inicialmente... Más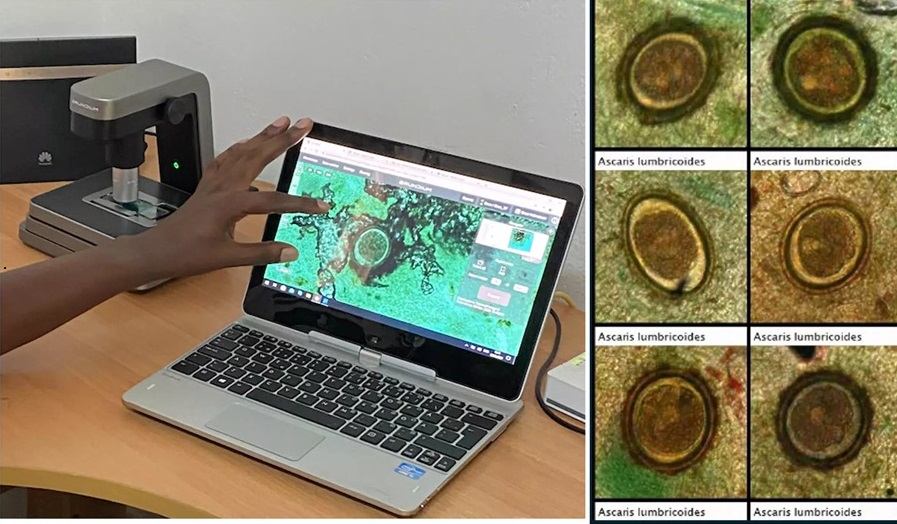
IA basada en imágenes se muestra prometedora para detección de parásitos en muestras de heces digitalizadas
Las infecciones por helmintos transmitidos por el suelo (STH), comúnmente conocidas como gusanos parásitos intestinales, se encuentran entre las enfermedades tropicales desatendidas más... Más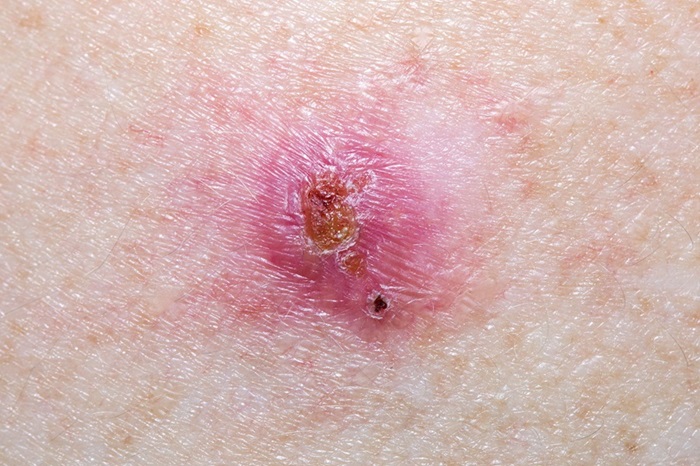
Algoritmos de inteligencia artificial potenciados por aprendizaje profundo mejoran la precisión en el diagnóstico de cáncer de piel.
Algoritmos de inteligencia artificial (IA) se utilizan cada vez más en diversos entornos clínicos, como la dermatología. Estos algoritmos se desarrollan entrenando una computadora... MásTecnología
ver canal
Nuevo sistema de diagnóstico de laboratorio en un chip iguala la precisión de las pruebas de PCR
Si bien las pruebas de PCR son el estándar de oro en cuanto a precisión para las pruebas de virología, tienen limitaciones como la complejidad, la necesidad de operadores de laboratorio capacitados y tiempos... Más
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más













