Desarrollan análisis LAMP para la trichomoniasis
|
Por el equipo editorial de LabMedica en español Actualizado el 24 Sep 2014 |
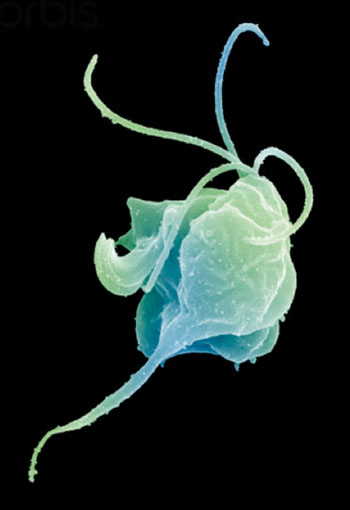
Imagen: Microfotografía electrónica de barrido (SEM) de un trofozoito de Trichomonas vaginalis (Fotografía cortesía del Dr. Dennis Kunkel).
Se desarrolló un análisis de amplificación isotérmica de ácidos nucleicos (LAMP, por sus siglas en inglés) dirigido contra una secuencia repetida de especie en el ADN, para la detección de Trichomonas vaginalis, el agente causante de la trichomoniasis
Las pruebas de diagnóstico de laboratorio más comunes para las infecciones por T. vaginalis incluyen microscopía en montaje húmedo; los cultivos y, recientemente, las pruebas de amplificación de ácidos nucleicos (NAAT) utilizando muestras de hisopos genitales, orina o de semen. El cultivo es el estándar de oro para el diagnóstico de T. vaginalis, aunque su sensibilidad puede ser tan baja como la de las microscopía, y requiere al menos una semana de incubación y microscopía diaria para obtener un desempeño óptimo.
Parasitólogos de la Universidad de las Filipinas (Manila, Filipinas) recogieron un total de 16 hisopos genitales y dos muestras de orina de mujeres que acudieron a un Centro de Salud y de Bienestar Reproductivos. Los cultivos de T. vaginalis axémicos en la fase log-media (107 trichomonas/mL) y un mL de alícuota de las muestras clínicas fueron concentrados en una bolita, por centrifugación. Todas las muestras fueron examinadas en busca de la presencia de T. vaginalis por reacción en cadena de la polimerasa (PCR).
Los cebadores LAMP específicos para T. vaginalis fueron diseñados con base en un fragmento de ADN de dos de kilo-bases de pares (2 kpb) repetidos de T. vaginalis. Los productos LAMP fueron evaluados por electroforesis en gel, por evaluación de la turbidez, y la adición de la Coloración SYBR Safe DNA Gel (Invitrogen, Carlsbad, CA, EUA) y fueron visualizados bajo un transiluminador ultravioleta (UVP, Upland, CA, EUA). Un cambio de color de naranja-a-rosa a la luz natural o una señal opaca a fluorescente bajo el transiluminador UV indicaron una reacción positiva.
De las 16 muestras de frotis genitales, 15 fueron negativas por PCR, y las dos muestras de orina también fueron negativas. Todas las muestras negativas fueron mezcladas y se utilizaron para adicionarlas para la evaluación de sensibilidad analítica. En muestras de hisopos genitales adicionadas, los resultados indican que el límite de detección del método LAMP fue de 100 trichomonas/mL o una trichomona, ya sea por electroforesis en gel, turbidez, o adición de SYBR Safe, mientras que el límite de detección de la PCR fue 103 trichomonas/mL o 1000 trichomonas. La LAMP para T. vaginalis no mostró reactividad cruzada con extractos de ADN de trichomonas estrechamente relacionados, Trichomonas tenax y Pentatrichomonas hominis, y otros microorganismos entéricos y urogenitales, Entamoeba histolytica, Candida albicans, Escherichia coli, Pseudomonas aeruginosa y Staphylococcus aureus.
Los autores concluyeron que el ensayo LAMP para T. vaginalis, desarrollado, era un método simple, rápido, sensible y específico para la detección de la trichomoniasis, la infección de transmisión sexual, curable, más común. Esta NAAT eficiente y rentable, tiene un gran potencial como aplicación para el diagnóstico y la vigilancia a gran escala, la detección primaria y el control de la trichomoniasis, en los puntos de atención y en entornos con recursos limitados. El estudio fue publicado en la edición de julio de 2014 de la revista Diagnostic Microbiology and Infectious Disease.
Enlaces relacionados:
University of the Philippines
Invitrogen
UVP
Las pruebas de diagnóstico de laboratorio más comunes para las infecciones por T. vaginalis incluyen microscopía en montaje húmedo; los cultivos y, recientemente, las pruebas de amplificación de ácidos nucleicos (NAAT) utilizando muestras de hisopos genitales, orina o de semen. El cultivo es el estándar de oro para el diagnóstico de T. vaginalis, aunque su sensibilidad puede ser tan baja como la de las microscopía, y requiere al menos una semana de incubación y microscopía diaria para obtener un desempeño óptimo.
Parasitólogos de la Universidad de las Filipinas (Manila, Filipinas) recogieron un total de 16 hisopos genitales y dos muestras de orina de mujeres que acudieron a un Centro de Salud y de Bienestar Reproductivos. Los cultivos de T. vaginalis axémicos en la fase log-media (107 trichomonas/mL) y un mL de alícuota de las muestras clínicas fueron concentrados en una bolita, por centrifugación. Todas las muestras fueron examinadas en busca de la presencia de T. vaginalis por reacción en cadena de la polimerasa (PCR).
Los cebadores LAMP específicos para T. vaginalis fueron diseñados con base en un fragmento de ADN de dos de kilo-bases de pares (2 kpb) repetidos de T. vaginalis. Los productos LAMP fueron evaluados por electroforesis en gel, por evaluación de la turbidez, y la adición de la Coloración SYBR Safe DNA Gel (Invitrogen, Carlsbad, CA, EUA) y fueron visualizados bajo un transiluminador ultravioleta (UVP, Upland, CA, EUA). Un cambio de color de naranja-a-rosa a la luz natural o una señal opaca a fluorescente bajo el transiluminador UV indicaron una reacción positiva.
De las 16 muestras de frotis genitales, 15 fueron negativas por PCR, y las dos muestras de orina también fueron negativas. Todas las muestras negativas fueron mezcladas y se utilizaron para adicionarlas para la evaluación de sensibilidad analítica. En muestras de hisopos genitales adicionadas, los resultados indican que el límite de detección del método LAMP fue de 100 trichomonas/mL o una trichomona, ya sea por electroforesis en gel, turbidez, o adición de SYBR Safe, mientras que el límite de detección de la PCR fue 103 trichomonas/mL o 1000 trichomonas. La LAMP para T. vaginalis no mostró reactividad cruzada con extractos de ADN de trichomonas estrechamente relacionados, Trichomonas tenax y Pentatrichomonas hominis, y otros microorganismos entéricos y urogenitales, Entamoeba histolytica, Candida albicans, Escherichia coli, Pseudomonas aeruginosa y Staphylococcus aureus.
Los autores concluyeron que el ensayo LAMP para T. vaginalis, desarrollado, era un método simple, rápido, sensible y específico para la detección de la trichomoniasis, la infección de transmisión sexual, curable, más común. Esta NAAT eficiente y rentable, tiene un gran potencial como aplicación para el diagnóstico y la vigilancia a gran escala, la detección primaria y el control de la trichomoniasis, en los puntos de atención y en entornos con recursos limitados. El estudio fue publicado en la edición de julio de 2014 de la revista Diagnostic Microbiology and Infectious Disease.
Enlaces relacionados:
University of the Philippines
Invitrogen
UVP
Últimas Microbiología noticias
- Prueba de bacterias bucales podría predecir la progresión del cáncer de colon
- Firma metabólica unica podría permitir el diagnóstico de sepsis dentro de una hora de la extracción de sangre
- Innovadora plataforma de diagnóstico proporciona resultados de AST con velocidad sin precedentes
- Análisis de sangre predice sepsis e insuficiencia orgánica en niños
- Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
- Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
- Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
- Nuevo análisis para tuberculosis podría ampliar acceso a pruebas en países de ingresos bajos y medios
- Prueba rápida diagnostica enfermedades tropicales en horas para tratamiento con antibióticos más rápido
- Pruebas moleculares rápidas permiten tratamiento antibiótico más rápido y específico para neumonía
- Plataforma rápida de PSA proporciona resultados terapéuticos específicos días antes que el estándar de atención actual
- Nuevo método de análisis detecta patógenos en sangre de forma más rápida y precisa al fundir ADN
- Prueba rápida de sepsis ofrece resultados dos días más rápidos
- Diagnóstico rápido portátil por PCR podría detectar gonorrea y susceptibilidad a antibióticos
- Prueba CRISPR diagnostica mpox más rápido que método de PCR de laboratorio
- Prueba de PCR multiplexada para detección de patógenos y resistencia a antibióticos ayuda a brindar un tratamiento rápido de ITU
Canales
Química Clínica
ver canal
Espectrómetro de masas impreso en 3D para el punto de atención supera a los modelos de última generación
La espectrometría de masas es una técnica precisa para identificar los componentes químicos de una muestra y tiene un potencial significativo para monitorear estados de salud de enfermedades... Más.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Prueba en orina detecta cáncer de cabeza y cuello
El virus del papiloma humano (VPH) es bien conocido por su papel en la causa del cáncer de cuello uterino y también se identifica cada vez más como responsable de los cánceres... Más.jpg)
Prueba de sangre detecta y monitorea cáncer pulmonar de células pequeñas agresivo
El cáncer de pulmón de células pequeñas (CPCP) es un tipo de cáncer muy agresivo conocido por su capacidad de metastatizar. El comportamiento de los tumores se rige en... Más.jpeg)
Ensayo de aprendizaje automático basado en sangre detecta de forma no invasiva el cáncer de ovario
El cáncer de ovario es una de las causas más comunes de muerte por cáncer entre las mujeres y tiene una tasa de supervivencia a cinco años de alrededor del 50%.... Más
Ensayo de PCR simple diferencia con precisión entre los subtipos de cáncer de pulmón de células pequeñas
El cáncer de pulmón de células pequeñas (CPCP), una neoplasia maligna neuroendocrina que progresa rápidamente, presenta bajas tasas de supervivencia. A pesar de su heterogeneidad molecular y clínica, el... MásHematología
ver canal
Primera prueba NAT 4 en 1 para el cribado de arbovirus podría reducir el riesgo de infecciones transmitidas por transfusiones
Los arbovirus representan una amenaza emergente para la salud mundial, exacerbada por el cambio climático y el aumento de la conectividad mundial que está facilitando su propagación a nuevas regiones.... Más
Instrumento de próxima generación detecta trastornos de la hemoglobina en recién nacidos
Las hemoglobinopatías, las enfermedades hereditarias más extendidas a nivel mundial, afectan a alrededor del 7 % de la población como portadores, y el 2,7 % de los recién nacidos nacen con estas enfermedades.... Más
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásInmunología
ver canal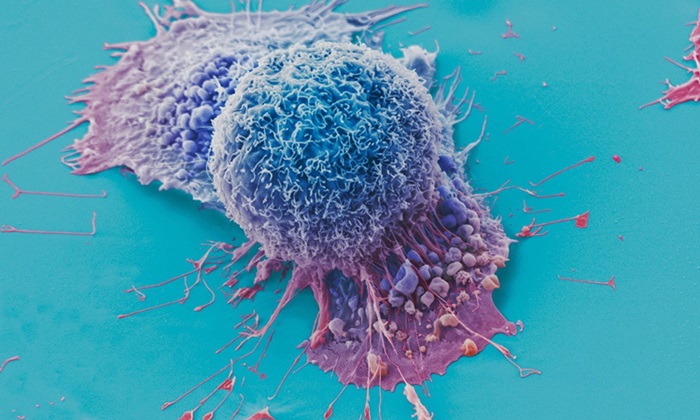
Herramienta de IA ajusta con precisión los medicamentos contra el cáncer con los pacientes utilizando información de cada célula tumoral
Las estrategias actuales para emparejar a los pacientes con cáncer con tratamientos específicos a menudo dependen de la secuenciación masiva de ADN y ARN tumoral, que proporciona un perfil promedio de... Más
Pruebas genéticas combinadas con la detección de fármacos personalizadas en muestras de tumores podrían revolucionar el tratamiento del cáncer
El tratamiento del cáncer generalmente se adhiere a un estándar de atención: regímenes establecidos y validados estadísticamente que son efectivos para la mayoría de los pacientes. Sin embargo, la variabilidad... Más
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... MásPatología
ver canal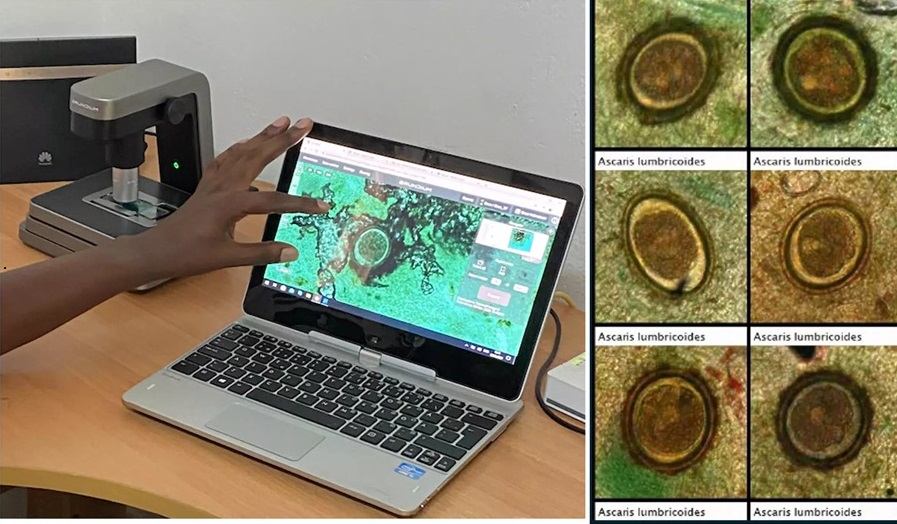
IA basada en imágenes se muestra prometedora para detección de parásitos en muestras de heces digitalizadas
Las infecciones por helmintos transmitidos por el suelo (STH), comúnmente conocidas como gusanos parásitos intestinales, se encuentran entre las enfermedades tropicales desatendidas más... Más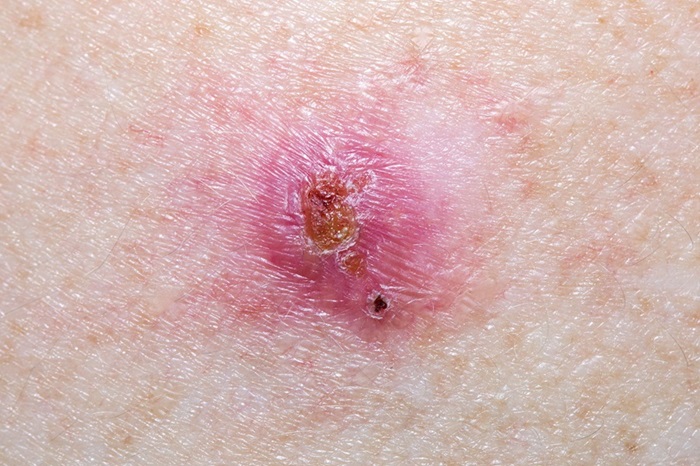
Algoritmos de inteligencia artificial potenciados por aprendizaje profundo mejoran la precisión en el diagnóstico de cáncer de piel.
Algoritmos de inteligencia artificial (IA) se utilizan cada vez más en diversos entornos clínicos, como la dermatología. Estos algoritmos se desarrollan entrenando una computadora... MásTecnología
ver canal
Nuevo sistema de diagnóstico de laboratorio en un chip iguala la precisión de las pruebas de PCR
Si bien las pruebas de PCR son el estándar de oro en cuanto a precisión para las pruebas de virología, tienen limitaciones como la complejidad, la necesidad de operadores de laboratorio capacitados y tiempos... Más
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más