Técnica de microscopía permite más biopsias informativas
|
Por el equipo editorial de LabMedica en español Actualizado el 14 Aug 2017 |
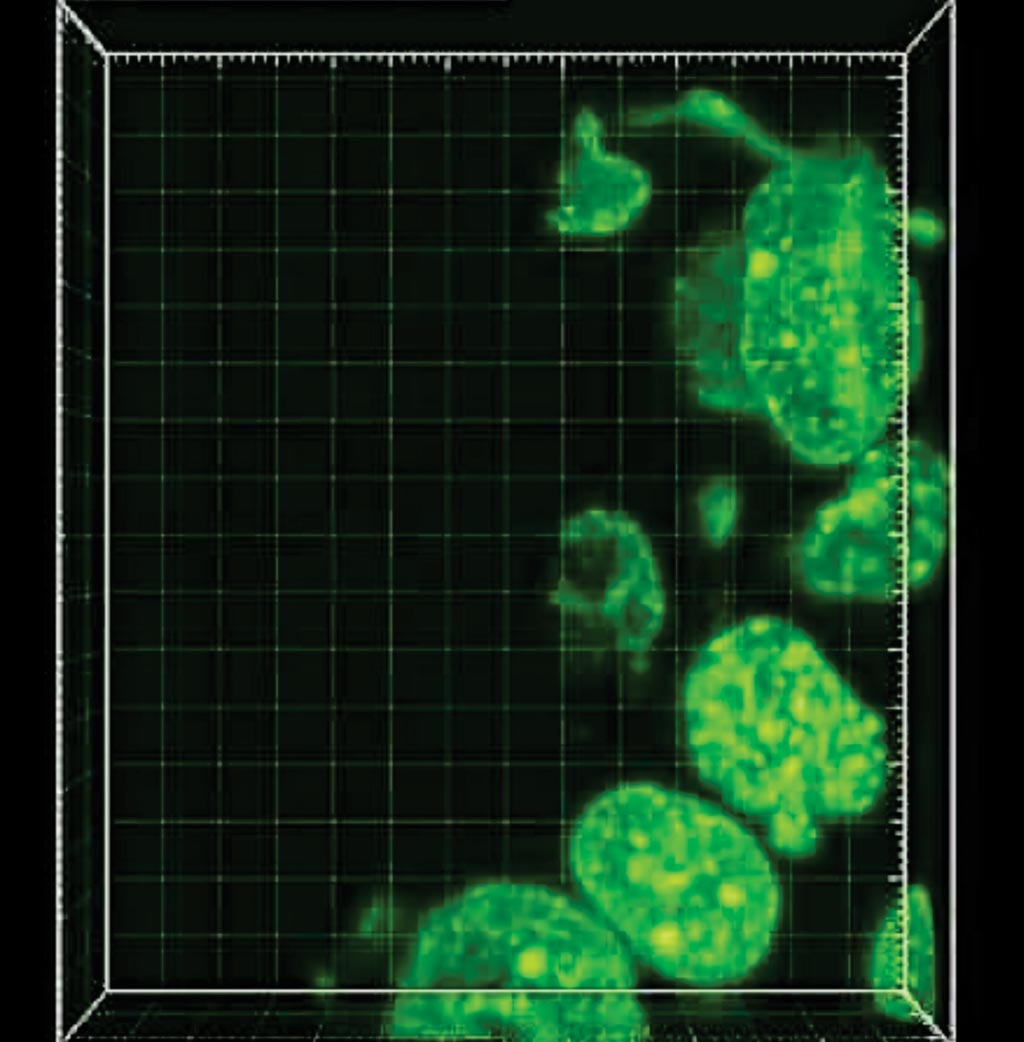
Imagen: La técnica de patología de expansión (ExPath) muestra el tejido expandido del cáncer de mama, facilitando la visualización de los núcleos en 3D (Fotografía cortesía del Instituto Ludwig para la Investigación del Cáncer).
La microscopía de expansión (ExM), es un método para mejorar la resolución de la microscopía óptica mediante la expansión física de una muestra, pero esta técnica no ha sido aplicada a muestras de tejido clínico. En este método ExM, una muestra de tejido se expande hasta 100 veces su volumen original, antes de empezar a ver las imágenes.
Esta expansión permite a los científicos ver las características, con un microscopio de luz convencional, que normalmente sólo se podrían ver con un microscopio electrónico costoso. También revela información molecular adicional que el microscopio electrónico no puede proporcionar.
Los científicos del Instituto Tecnológico de Massachusetts (Cambridge, MA, EUA) y sus colegas, desarrollaron una forma clínicamente optimizada de ExM que permite ver las imágenes en nanoescala de muestras de tejidos humanos que se han fijado con formol, han sido incluidas en parafina, coloreadas con hematoxilina y eosina, y/o se han mantenido congeladas o frescas. El método, que denominan patología de expansión (ExPath), convierte las muestras clínicas en un estado compatible con ExM, luego aplica un protocolo ExM con anclaje de proteínas y pasos de homogeneización mecánica optimizados para muestras clínicas.
El equipo ensayó este método en muestras de tejidos de pacientes con lesiones mamarias en etapas tempranas. Una forma de predecir si estas lesiones se convertirán en malignas es evaluar la apariencia de los núcleos de las células. Las lesiones benignas con núcleos atípicos tienen aproximadamente una probabilidad cinco veces mayor de progresar a cáncer que aquellas que muestran núcleos típicos. Sin embargo, los estudios han revelado discrepancias significativas entre las evaluaciones de las atipias nucleares realizadas por diferentes patólogos, que pueden conducir potencialmente a un diagnóstico inexacto y cirugía innecesaria. ExPath permite obtener imágenes con ~ 70 nm de resolución de diversas biomoléculas en tejidos intactos usando microscopios convencionales de difracción limitada, anticuerpos estándar y reactivos de hibridación fluorescente in situ.
Después de expandir las muestras de tejido, los científicos las analizaron con un algoritmo de aprendizaje automático que puede clasificar los núcleos con base en docenas de características, incluyendo orientación, diámetro y cuánto se desvían de la circularidad verdadera. Este algoritmo fue capaz de diferenciar entre las lesiones que tenían mucha probabilidad de convertirse en invasoras y las que no lo eran, con una exactitud del 93% en las muestras expandidas, en comparación con sólo el 71% en el tejido pre-expandido. También analizaron muestras de tejido renal de pacientes con síndrome nefrótico y cuando mostraron las imágenes de las muestras de tejido expandido a un grupo de científicos que incluía patólogos y no patólogos, el grupo fue capaz de identificar el tejido enfermo con un 90% de exactitud, en comparación con solo 65% de exactitud en las muestras de tejidos no expandidas.
Edward S. Boyden, PhD, un profesor de Ingeniería Biológica y coautor principal del estudio, dijo: “Ahora usted puede diagnosticar la enfermedad renal nefrótica sin necesidad de un microscopio electrónico, una máquina muy cara. Usted puede hacerlo con unos pocos productos químicos y un microscopio de luz. Si se puede ampliar un tejido por cien veces en volumen, manteniendo todas las demás cosas iguales, obtendrá 100 veces la cantidad de información”. El estudio fue publicado el 17 de julio de 2017 en la revista Nature Biotechnology.
Esta expansión permite a los científicos ver las características, con un microscopio de luz convencional, que normalmente sólo se podrían ver con un microscopio electrónico costoso. También revela información molecular adicional que el microscopio electrónico no puede proporcionar.
Los científicos del Instituto Tecnológico de Massachusetts (Cambridge, MA, EUA) y sus colegas, desarrollaron una forma clínicamente optimizada de ExM que permite ver las imágenes en nanoescala de muestras de tejidos humanos que se han fijado con formol, han sido incluidas en parafina, coloreadas con hematoxilina y eosina, y/o se han mantenido congeladas o frescas. El método, que denominan patología de expansión (ExPath), convierte las muestras clínicas en un estado compatible con ExM, luego aplica un protocolo ExM con anclaje de proteínas y pasos de homogeneización mecánica optimizados para muestras clínicas.
El equipo ensayó este método en muestras de tejidos de pacientes con lesiones mamarias en etapas tempranas. Una forma de predecir si estas lesiones se convertirán en malignas es evaluar la apariencia de los núcleos de las células. Las lesiones benignas con núcleos atípicos tienen aproximadamente una probabilidad cinco veces mayor de progresar a cáncer que aquellas que muestran núcleos típicos. Sin embargo, los estudios han revelado discrepancias significativas entre las evaluaciones de las atipias nucleares realizadas por diferentes patólogos, que pueden conducir potencialmente a un diagnóstico inexacto y cirugía innecesaria. ExPath permite obtener imágenes con ~ 70 nm de resolución de diversas biomoléculas en tejidos intactos usando microscopios convencionales de difracción limitada, anticuerpos estándar y reactivos de hibridación fluorescente in situ.
Después de expandir las muestras de tejido, los científicos las analizaron con un algoritmo de aprendizaje automático que puede clasificar los núcleos con base en docenas de características, incluyendo orientación, diámetro y cuánto se desvían de la circularidad verdadera. Este algoritmo fue capaz de diferenciar entre las lesiones que tenían mucha probabilidad de convertirse en invasoras y las que no lo eran, con una exactitud del 93% en las muestras expandidas, en comparación con sólo el 71% en el tejido pre-expandido. También analizaron muestras de tejido renal de pacientes con síndrome nefrótico y cuando mostraron las imágenes de las muestras de tejido expandido a un grupo de científicos que incluía patólogos y no patólogos, el grupo fue capaz de identificar el tejido enfermo con un 90% de exactitud, en comparación con solo 65% de exactitud en las muestras de tejidos no expandidas.
Edward S. Boyden, PhD, un profesor de Ingeniería Biológica y coautor principal del estudio, dijo: “Ahora usted puede diagnosticar la enfermedad renal nefrótica sin necesidad de un microscopio electrónico, una máquina muy cara. Usted puede hacerlo con unos pocos productos químicos y un microscopio de luz. Si se puede ampliar un tejido por cien veces en volumen, manteniendo todas las demás cosas iguales, obtendrá 100 veces la cantidad de información”. El estudio fue publicado el 17 de julio de 2017 en la revista Nature Biotechnology.
Últimas Patología noticias
- Nuevo método basado en aprendizaje automático detecta contaminación microbiana en cultivos celulares
- Nuevo método con corrección de errores detecta cáncer únicamente en muestras de sangre
- Algoritmo "detector de metales" consigue tumores vulnerables
- Nueva técnica identifica y clasifica subtipos de células de cáncer de páncreas
- Imágenes avanzadas revelan mecanismos que causan enfermedades autoinmunes
- Modelo de IA predice eficazmente resultados de pacientes con cáncer de pulmón
- Modelo de IA predice respuesta al tratamiento del cáncer de vejiga
- Nuevo método basado en láser acelera diagnóstico del cáncer
- Nuevo modelo de IA predice efectos de variantes genéticas en enfermedades específicas
- Herramienta de IA diagnostica enfermedad celíaca en imágenes de biopsia con precisión superior al 97%
- Condiciones preanalíticas influyen en estabilidad de microARN libres de células en muestras de plasma sanguíneo
- Sistema de cultivo celular 3D podría revolucionar diagnóstico del cáncer
- Técnica indolora mide concentraciones de glucosa en solución y tejido mediante ondas sonoras
- Prueba cutánea mejora diagnóstico de enfermedades neurodegenerativas raras y debilitantes
- Uromodulina sérica podría indicar lesión renal aguda en pacientes con COVID-19
- Modelo de IA revela edad biológica real con cinco gotas de sangre
Canales
Química Clínica
ver canal
Herramienta química a nanoescala 'brillantemente luminosa' mejora detección de enfermedades
Miles de moléculas brillantes disponibles comercialmente, conocidas como fluoróforos, se utilizan comúnmente en imágenes médicas, detección de enfermedades, marcado... Más
Prueba de detección portátil económica transforma detección de enfermedades renales
Millones de personas padecen enfermedad renal, que a menudo permanece sin diagnosticar hasta que alcanza una etapa crítica. Esta epidemia silenciosa no solo disminuye la calidad de vida de los afectados,... MásDiagnóstico Molecular
ver canal
Prueba de biomarcadores sanguíneos podría detectar predisposición genética al Alzheimer
Nuevos medicamentos para la enfermedad de Alzheimer, la forma más común de demencia, están ahora disponibles. Estos tratamientos, conocidos como "anticuerpos amiloides",... Más
Se descubre nuevo autoanticuerpo contra DAGLA en cerebelitis
Las ataxias cerebelosas autoinmunes son trastornos muy incapacitantes que se caracterizan por una disminución de la habilidad para coordinar el movimiento muscular. Los autoanticuerpos cerebelosos... MásHematología
ver canal
Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
La citopenia clonal de significado incierto (CCSI) es un trastorno sanguíneo común en adultos mayores, caracterizado por mutaciones en las células sanguíneas y un recuento ... Más
Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
En los Estados Unidos, aproximadamente el 15 % de las embarazadas son RhD negativas. Sin embargo, en aproximadamente el 40 % de estos casos, el feto también es RhD negativo, lo que hace innecesaria la... MásInmunología
ver canal
Prueba de células madre predice resultado del tratamiento en cáncer de ovario resistente al platino
El cáncer de ovario epitelial suele responder inicialmente a la quimioterapia, pero con el tiempo, el tumor desarrolla resistencia a la terapia, lo que provoca su recrecimiento. Esta resistencia... Más
Análisis de sangre con aprendizaje automático predice respuesta a inmunoterapia en pacientes con linfoma
La terapia de células T con receptores de antígenos quiméricos (CAR) se ha convertido en uno de los avances recientes más prometedores en el tratamiento de los cánceres... MásMicrobiología
ver canal
Dispositivo portátil ofrece resultados de tuberculosis económico y rápido
La tuberculosis (TB) sigue siendo la enfermedad infecciosa más mortal a nivel mundial, afectando a aproximadamente 10 millones de personas al año. En 2021, alrededor de 4,2 millones de casos... Más
Método basado en IA mejora diagnóstico de infecciones resistentes a fármacos
Las infecciones resistentes a los medicamentos, en particular las causadas por bacterias mortales como la tuberculosis y el estafilococo, se están convirtiendo rápidamente en una emergencia... MásTecnología
ver canal
Tecnología de microchip desechable podría detectar selectivamente VIH en muestras de sangre completa
A finales de 2023, aproximadamente 40 millones de personas en todo el mundo vivían con VIH, y alrededor de 630.000 personas murieron por enfermedades relacionadas con el sida ese mismo año.... Más
Dispositivo microfluídico Dolor en un Chip determina tipos de dolor crónico desde muestras de sangre
El dolor crónico es una afección generalizada que sigue siendo difícil de controlar, y los métodos clínicos existentes para su tratamiento se basan en gran medida en... MásIndustria
ver canal
Cepheid y Oxford Nanopore se unen para desarrollar soluciones con secuenciación automatizada
Cepheid (Sunnyvale, CA, EUA), una empresa líder en diagnóstico molecular, y Oxford Nanopore Technologies (Oxford, Reino Unido), la empresa detrás de una nueva generación de... Más