Diagnostican la infección congénita por citomegalovirus a través de muestras de sangre seca
|
Por el equipo editorial de LabMedica en español Actualizado el 26 Aug 2019 |
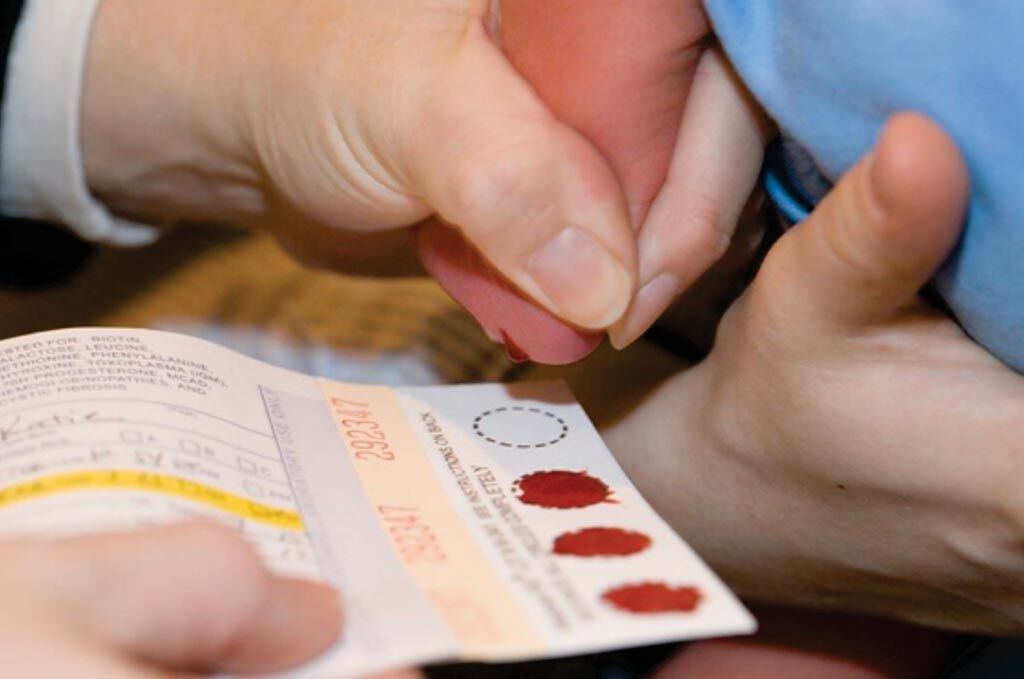
Imagen: Aplicación de la sangre de un recién nacido a una tarjeta Guthrie para analizar varias enfermedades, incluido el citomegalovirus (Fotografía cortesía del NHS).
El citomegalovirus es la principal causa de infección congénita (cCMV) afectando a hasta el 0,8% de los recién nacidos en países de altos ingresos y es la causa más común de sordera no genética en la infancia. Se han correlacionado una amplia gama de enfermedades, diagnosticadas al nacer o en la infancia, con la infección congénita por CMV.
El diagnóstico de la infección congénita por CMV se puede lograr mediante el examen de muestras salivales/urinarias recolectadas dentro de las primeras 2 a 3 semanas de edad como resultado del programa de detección auditiva para recién nacidos (NHSP). Después de este período temprano de la vida, es posible distinguir entre la infección congénita y la adquirida por CMV simplemente examinando las muestras de Manchas de sangre seca (DBS, por sus siglas en inglés) en las tarjetas “Guthrie” que se recolectan universalmente dentro de los tres días posteriores al nacimiento.
Científicos médicos de la Università degli Studi di Milano (Milán, Italia) recolectaron muestras de DBS de niños con un diagnóstico de sordera, que fueron recuperadas del centro regional de detección neonatal y analizadas para detectar el CMV entre el 1 de enero de 2014 y 31 de diciembre de 2018. Las muestras de DBS se procesaron mediante dos pasos internos separados que consistieron en la extracción de ADN de las muestras de DBS mediante un método de extracción por calor, seguido de la amplificación de un fragmento del genoma de CMV utilizando una reacción en cadena de polimerasa anidada. El límite inferior de detección de la prueba CMV-DBS fue de 400 copias de ADN de CMV/mL.
Los investigadores informaron que, en general, se incluyeron 82 niños con una edad media de 3,4 meses; (cuartiles inferior-superior: 2–5,3 meses; varones: 60,9%). La mayoría de ellos (70,7%) presentaron hipoacusia bilateral con un patrón simétrico en el 79,3% de los casos. Los umbrales de las respuestas auditivas del tronco encefálico (ABR) fueron ≥ 70 dB HL (sordera severa/profunda) en 46,5% de los niños. Entre todos los niños evaluados, el 6,1% resultó positivo para cCMV. La tasa de sordera severa/profunda fue estadísticamente más alta en niños con infección congénita por CMV.
Los autores concluyeron que la adición de la prueba DBS al NHSP permitió la identificación, en sus primeros meses de vida, de una infección congénita por CMV en el 6,1% de los niños que no habían mostrado resultados positivos en el NHS . La introducción de una estrategia de detección selectiva de CMV podría ayudar a los médicos en el diagnóstico diferencial y en el manejo de los bebés. Las muestras de DBS pueden ser consideradas como un “biobanco universal para recién nacidos”: su sitio de almacenamiento y duración deben ser objeto de toma de decisiones políticas. El estudio fue publicado el 22 de julio de 2019 en la revista BMC Infectious Diseases.
Enlace relacionado:
Università degli Studi di Milano
El diagnóstico de la infección congénita por CMV se puede lograr mediante el examen de muestras salivales/urinarias recolectadas dentro de las primeras 2 a 3 semanas de edad como resultado del programa de detección auditiva para recién nacidos (NHSP). Después de este período temprano de la vida, es posible distinguir entre la infección congénita y la adquirida por CMV simplemente examinando las muestras de Manchas de sangre seca (DBS, por sus siglas en inglés) en las tarjetas “Guthrie” que se recolectan universalmente dentro de los tres días posteriores al nacimiento.
Científicos médicos de la Università degli Studi di Milano (Milán, Italia) recolectaron muestras de DBS de niños con un diagnóstico de sordera, que fueron recuperadas del centro regional de detección neonatal y analizadas para detectar el CMV entre el 1 de enero de 2014 y 31 de diciembre de 2018. Las muestras de DBS se procesaron mediante dos pasos internos separados que consistieron en la extracción de ADN de las muestras de DBS mediante un método de extracción por calor, seguido de la amplificación de un fragmento del genoma de CMV utilizando una reacción en cadena de polimerasa anidada. El límite inferior de detección de la prueba CMV-DBS fue de 400 copias de ADN de CMV/mL.
Los investigadores informaron que, en general, se incluyeron 82 niños con una edad media de 3,4 meses; (cuartiles inferior-superior: 2–5,3 meses; varones: 60,9%). La mayoría de ellos (70,7%) presentaron hipoacusia bilateral con un patrón simétrico en el 79,3% de los casos. Los umbrales de las respuestas auditivas del tronco encefálico (ABR) fueron ≥ 70 dB HL (sordera severa/profunda) en 46,5% de los niños. Entre todos los niños evaluados, el 6,1% resultó positivo para cCMV. La tasa de sordera severa/profunda fue estadísticamente más alta en niños con infección congénita por CMV.
Los autores concluyeron que la adición de la prueba DBS al NHSP permitió la identificación, en sus primeros meses de vida, de una infección congénita por CMV en el 6,1% de los niños que no habían mostrado resultados positivos en el NHS . La introducción de una estrategia de detección selectiva de CMV podría ayudar a los médicos en el diagnóstico diferencial y en el manejo de los bebés. Las muestras de DBS pueden ser consideradas como un “biobanco universal para recién nacidos”: su sitio de almacenamiento y duración deben ser objeto de toma de decisiones políticas. El estudio fue publicado el 22 de julio de 2019 en la revista BMC Infectious Diseases.
Enlace relacionado:
Università degli Studi di Milano
Últimas Microbiología noticias
- Análisis de sangre predice sepsis e insuficiencia orgánica en niños
- Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
- Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
- Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
- Nuevo análisis para tuberculosis podría ampliar acceso a pruebas en países de ingresos bajos y medios
- Prueba rápida diagnostica enfermedades tropicales en horas para tratamiento con antibióticos más rápido
- Pruebas moleculares rápidas permiten tratamiento antibiótico más rápido y específico para neumonía
- Plataforma rápida de PSA proporciona resultados terapéuticos específicos días antes que el estándar de atención actual
- Nuevo método de análisis detecta patógenos en sangre de forma más rápida y precisa al fundir ADN
- Prueba rápida de sepsis ofrece resultados dos días más rápidos
- Diagnóstico rápido portátil por PCR podría detectar gonorrea y susceptibilidad a antibióticos
- Prueba CRISPR diagnostica mpox más rápido que método de PCR de laboratorio
- Prueba de PCR multiplexada para detección de patógenos y resistencia a antibióticos ayuda a brindar un tratamiento rápido de ITU
- Nuevo algoritmo detecta e identifica nuevos organismos bacterianos
- Analizador de mesa promete detección de ITU en 1 hora e indicación de sensibilidad a antibióticos
- Prueba rápida junto a la cama podría proteger a recién nacidos de enfermedades potencialmente mortales
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal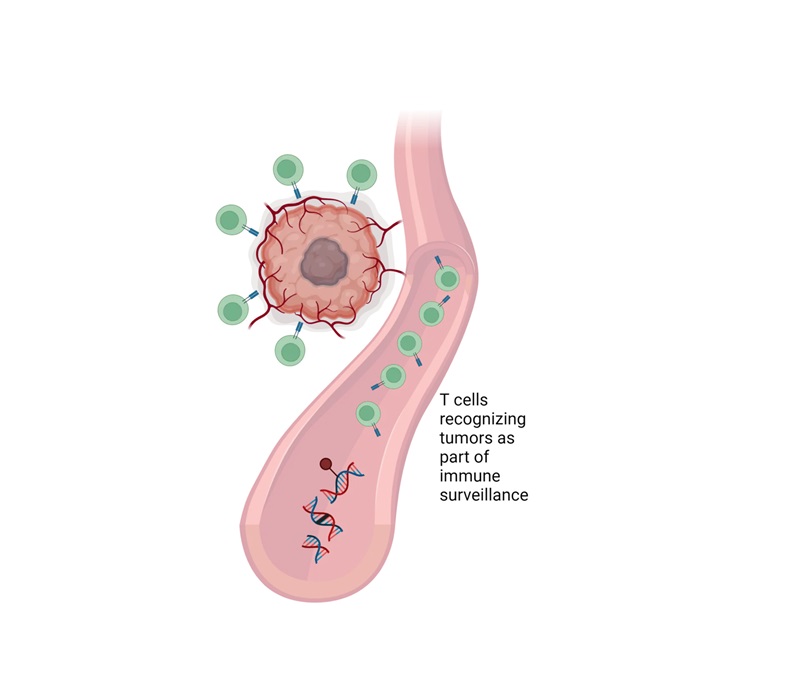
Enfoque revolucionario de análisis de células T permite detección temprana del cáncer
La biopsia líquida, un método para diagnosticar el cáncer mediante análisis de sangre de rutina, es una herramienta potencial importante para la detección temprana del... MásPrueba genética única podría acelerar el diagnóstico de trastornos raros del desarrollo
Las alteraciones en el ADN humano varían desde variaciones menores de un solo nucleótido hasta alteraciones sustanciales que implican la eliminación o duplicación de segmentos... Más
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásPatología
ver canal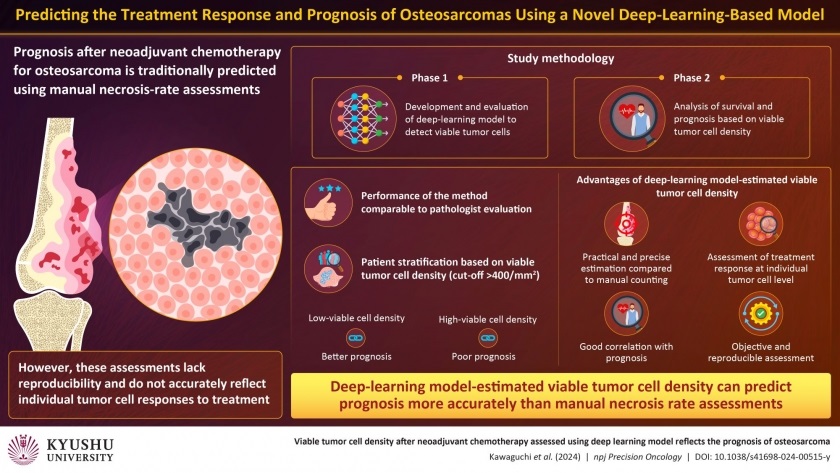
Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico... Más
Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
La comunidad médica mundial reconoce cada vez más que la biopsia líquida es un enfoque transformador para mejorar la atención al paciente con cáncer. Este innovador método de diagnóstico implica detectar... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)

.jpg)