Dispositivo de movilidad microfluídica indica la probabilidad de metástasis en el cáncer de mama
|
Por el equipo editorial de LabMedica en español Actualizado el 17 Jun 2019 |
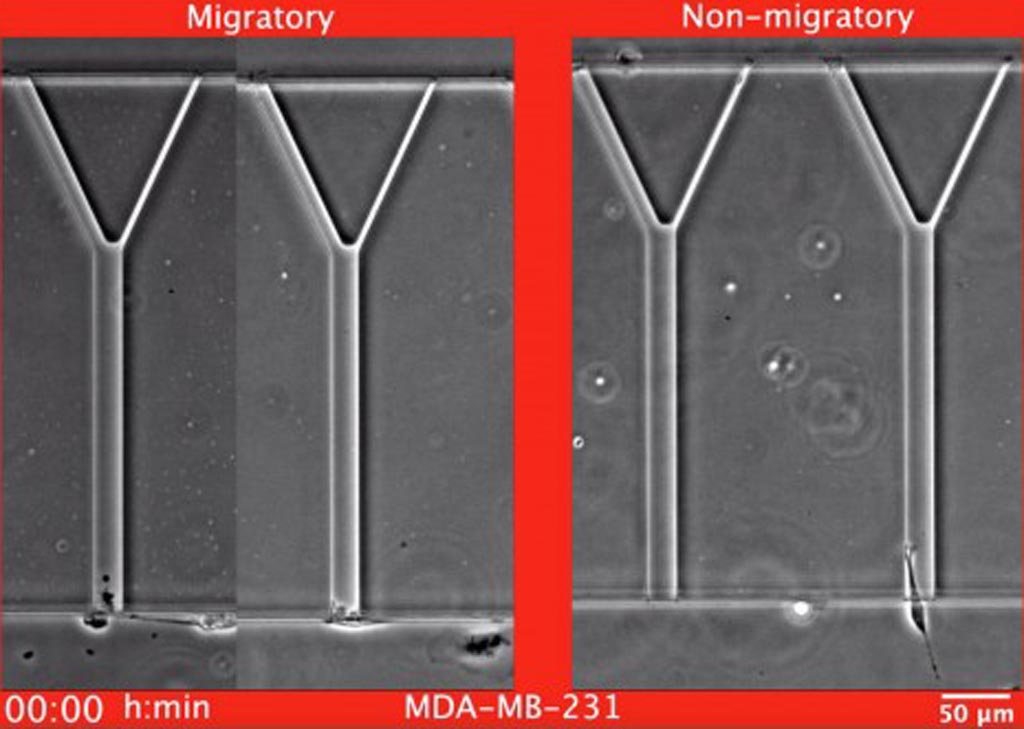
Imagen: Ejemplos de células de cáncer de mama, MDA-MB-231, migratorias y no migratorias mientras migran en el dispositivo MAqCI (Ensayo Microfluídico para la cuantificación de la invasión celular) (Fotografía cortesía de Christopher L. Yankaskas, Universidad Johns Hopkins).
Se demostró que una nueva prueba de motilidad microfluídica predice con exactitud la probabilidad de que un tumor de mama genere metástasis.
Las dificultades involucradas en la predicción de qué pacientes con cáncer de mama desarrollarán metástasis, conducen al tratamiento excesivo de pacientes con enfermedad benigna y al tratamiento inadecuado de los cánceres agresivos. Para enfrentar este desafío predictivo, los investigadores de la Universidad Johns Hopkins (Baltimore, MD, EUA) desarrollaron un ensayo microfluídico que cuantificó la abundancia y el índice proliferativo de células migratorias en especímenes de cáncer de mama, con el fin de evaluar su propensión a hacer metástasis y para la selección rápida de posibles terapias antimetastásicas.
El dispositivo comprende microcanales, en forma de Y, con dimensiones elegidas para imitar aspectos de la complejidad y la variedad de las áreas de corte transversal de las huellas de tejido que se encuentran en o a lo largo de diferentes ubicaciones del cuerpo. Este ensayo microfluídico para la cuantificación de la invasión celular (MAqCI) se diseñó para evaluar tres características clave de la metástasis: la capacidad de las células cancerosas para moverse, su capacidad de comprimirse para ingresar en canales estrechos y su capacidad de proliferar.
El dispositivo MAqCI, que ahora está patentado en los Estados Unidos, se usó junto con un microscopio invertido computarizado que tiene contraste de fase y capacidades de imagen de fluorescencia. La migración celular se monitorizó en tiempo real mediante microscopía de contraste de fase de lapso de tiempo. Los resultados de los experimentos realizados con el dispositivo MAqCI revelaron que, en comparación con una población no clasificada de células cancerosas, las células altamente móviles aisladas por el dispositivo mostraron un potencial tumorigénico similar pero aumentaron notablemente la propensión metastásica in vivo.
La secuenciación de ARN de las células altamente móviles reveló un enriquecimiento de los genes relacionados con la motilidad y la supervivencia.
“Cuando se detecta un bulto en el cuerpo de un paciente, el médico puede determinar si la masa es benigna o maligna a través de una biopsia, pero realmente no pueden decir con seguridad si un tumor maligno va a ser muy agresivo y si hará metástasis en otras ubicaciones”, dijo el autor principal, el Dr. Konstantinos Konstantopoulos, profesor de ingeniería biomédica y oncología en la Universidad Johns Hopkins. “Aunque las biopsias líquidas o las mediciones de ADN tumoral circulante pueden ser muy buenas para monitorizar la respuesta de un paciente a la terapia después de su administración, no proporcionan un medio para ayudar a los médicos a seleccionar medicamentos óptimos para prevenir la propagación”.
El uso del dispositivo MAqCI se describió en la edición digital del 6 de mayo de 2019 de la revista Nature Biomedical Engineering.
Enlace relacionado:
Johns Hopkins University
Las dificultades involucradas en la predicción de qué pacientes con cáncer de mama desarrollarán metástasis, conducen al tratamiento excesivo de pacientes con enfermedad benigna y al tratamiento inadecuado de los cánceres agresivos. Para enfrentar este desafío predictivo, los investigadores de la Universidad Johns Hopkins (Baltimore, MD, EUA) desarrollaron un ensayo microfluídico que cuantificó la abundancia y el índice proliferativo de células migratorias en especímenes de cáncer de mama, con el fin de evaluar su propensión a hacer metástasis y para la selección rápida de posibles terapias antimetastásicas.
El dispositivo comprende microcanales, en forma de Y, con dimensiones elegidas para imitar aspectos de la complejidad y la variedad de las áreas de corte transversal de las huellas de tejido que se encuentran en o a lo largo de diferentes ubicaciones del cuerpo. Este ensayo microfluídico para la cuantificación de la invasión celular (MAqCI) se diseñó para evaluar tres características clave de la metástasis: la capacidad de las células cancerosas para moverse, su capacidad de comprimirse para ingresar en canales estrechos y su capacidad de proliferar.
El dispositivo MAqCI, que ahora está patentado en los Estados Unidos, se usó junto con un microscopio invertido computarizado que tiene contraste de fase y capacidades de imagen de fluorescencia. La migración celular se monitorizó en tiempo real mediante microscopía de contraste de fase de lapso de tiempo. Los resultados de los experimentos realizados con el dispositivo MAqCI revelaron que, en comparación con una población no clasificada de células cancerosas, las células altamente móviles aisladas por el dispositivo mostraron un potencial tumorigénico similar pero aumentaron notablemente la propensión metastásica in vivo.
La secuenciación de ARN de las células altamente móviles reveló un enriquecimiento de los genes relacionados con la motilidad y la supervivencia.
“Cuando se detecta un bulto en el cuerpo de un paciente, el médico puede determinar si la masa es benigna o maligna a través de una biopsia, pero realmente no pueden decir con seguridad si un tumor maligno va a ser muy agresivo y si hará metástasis en otras ubicaciones”, dijo el autor principal, el Dr. Konstantinos Konstantopoulos, profesor de ingeniería biomédica y oncología en la Universidad Johns Hopkins. “Aunque las biopsias líquidas o las mediciones de ADN tumoral circulante pueden ser muy buenas para monitorizar la respuesta de un paciente a la terapia después de su administración, no proporcionan un medio para ayudar a los médicos a seleccionar medicamentos óptimos para prevenir la propagación”.
El uso del dispositivo MAqCI se describió en la edición digital del 6 de mayo de 2019 de la revista Nature Biomedical Engineering.
Enlace relacionado:
Johns Hopkins University
Últimas Patología noticias
- Sistema de imágenes digitales impulsado por IA podría revolucionar el diagnóstico del cáncer
- Nuevo panel de mycobacterium tuberculosis respalda la vigilancia en tiempo real y combate la resistencia a los antimicrobianos
- Análisis de tejido espacial identifica patrones asociados con la recaída del cáncer de ovario
- IA basada en imágenes se muestra prometedora para detección de parásitos en muestras de heces digitalizadas
- Algoritmos de inteligencia artificial potenciados por aprendizaje profundo mejoran la precisión en el diagnóstico de cáncer de piel.
- Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
- Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
- Innovador dispositivo de extracción de sangre supera obstáculos comunes relacionados con la flebotomía
- Dispositivo de microfluidos para detección del cáncer separa con precisión entidades tumorales
- Biopsia de piel virtual determina la presencia de células cancerosas
- Dispositivo POC intraoperatorio distingue entre quistes ováricos benignos y malignos en 15 minutos
- Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
- Herramienta bioinformática para identificar alteraciones cromosómicas en células tumorales puede mejorar diagnóstico del cáncer
- Dispositivo del tamaño de una moneda aísla rápidamente plasma sanguíneo para diagnósticos clínicos más rápidos y precisos
- IA predice propagación del cáncer al cerebro a partir de imágenes de biopsia de pulmón
- Tecnología de microagujas mejorada acelera extracción de muestra de líquido intersticial para diagnóstico de enfermedades
Canales
Química Clínica
ver canal
Espectrómetro de masas impreso en 3D para el punto de atención supera a los modelos de última generación
La espectrometría de masas es una técnica precisa para identificar los componentes químicos de una muestra y tiene un potencial significativo para monitorear estados de salud de enfermedades... Más.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Prueba de sangre predice con precisión el riesgo de cáncer de pulmón y reduce la necesidad de escaneos de TC
El cáncer de pulmón es extremadamente difícil de detectar tempranamente debido a las limitaciones de las tecnologías de detección actuales, que son costosas, a veces... Más
Firma única de autoanticuerpos ayuda a diagnosticar la esclerosis múltiple años antes de la aparición de síntomas
Se cree que las enfermedades autoinmunes como la esclerosis múltiple (EM) ocurren en parte debido a respuestas inmunes inusuales a infecciones comunes. Los primeros síntomas de la EM, incluidos... Más
Prueba de sangre podría detectar cánceres asociados al VPH 10 años antes del diagnóstico clínico
Se sabe que el virus del papiloma humano (VPH) causa varios cánceres, incluidos los de genitales, ano, boca, garganta y cuello uterino. El cáncer orofaríngeo asociado al VPH (VPH+COF)... Más
Un diagnóstico de bajo costo en el punto de atención ampliará el acceso a pruebas de enfermedades de transmisión sexual
La gonorrea es la segunda infección bacteriana de transmisión sexual (ITS) más comúnmente reportada, con alrededor de 82 millones de casos en todo el mundo en 2020. La infección puede tener graves consecuencias... MásHematología
ver canal
Primera prueba NAT 4 en 1 para el cribado de arbovirus podría reducir el riesgo de infecciones transmitidas por transfusiones
Los arbovirus representan una amenaza emergente para la salud mundial, exacerbada por el cambio climático y el aumento de la conectividad mundial que está facilitando su propagación a nuevas regiones.... Más
Instrumento de próxima generación detecta trastornos de la hemoglobina en recién nacidos
Las hemoglobinopatías, las enfermedades hereditarias más extendidas a nivel mundial, afectan a alrededor del 7 % de la población como portadores, y el 2,7 % de los recién nacidos nacen con estas enfermedades.... Más
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásInmunología
ver canal
Análisis de sangre para diagnóstico de rechazo celular después de trasplante de órganos podría reemplazar las biopsias quirúrgicas
Los órganos trasplantados enfrentan constantemente el riesgo de ser rechazados por el sistema inmunológico del receptor, que los diferencia de los órganos no propios mediante... Más
Herramienta de IA ajusta con precisión los medicamentos contra el cáncer con los pacientes utilizando información de cada célula tumoral
Las estrategias actuales para emparejar a los pacientes con cáncer con tratamientos específicos a menudo dependen de la secuenciación masiva de ADN y ARN tumoral, que proporciona un perfil promedio de... Más
Pruebas genéticas combinadas con la detección de fármacos personalizadas en muestras de tumores podrían revolucionar el tratamiento del cáncer
El tratamiento del cáncer generalmente se adhiere a un estándar de atención: regímenes establecidos y validados estadísticamente que son efectivos para la mayoría de los pacientes. Sin embargo, la variabilidad... Más
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... MásMicrobiología
ver canal
Nuevos ensayos de hepatitis con marcado CE permite la detección temprana de infecciones
Según la Organización Mundial de la Salud (OMS), se estima que 354 millones de personas en todo el mundo padecen hepatitis B o C crónica. Estos virus son las principales causas de... Más
Prueba de PCR múltiplex identifica el 95 % de los patógenos que causan la sepsis en una hora
La sepsis contribuye a una de cada tres muertes hospitalarias en los Estados Unidos y, a nivel mundial, el shock séptico conlleva una tasa de mortalidad del 30 al 40 %. El diagnóstico temprano de la sepsis... Más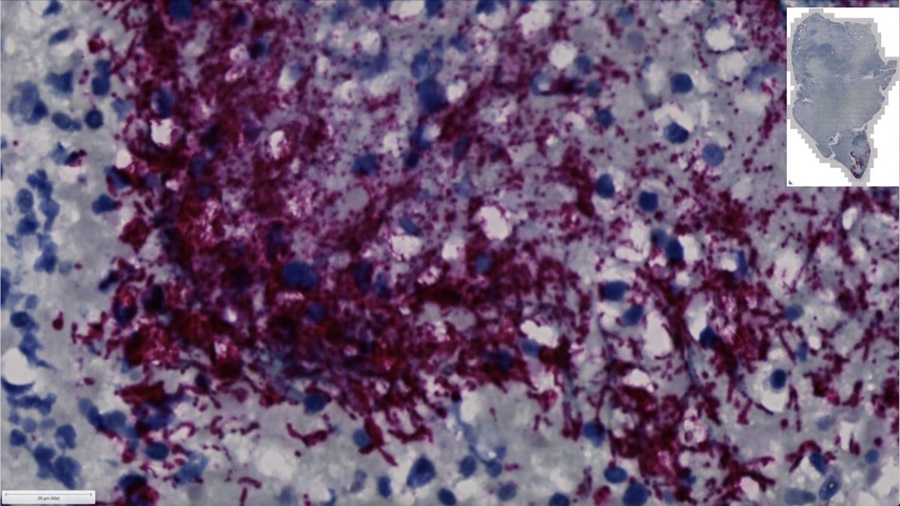
Prueba de bacterias bucales podría predecir la progresión del cáncer de colon
El cáncer de colon, una enfermedad relativamente común pero difícil de diagnosticar, requiere confirmación mediante una colonoscopia o cirugía. Recientemente, ha habido... Más.jpg)
Firma metabólica unica podría permitir el diagnóstico de sepsis dentro de una hora de la extracción de sangre
La sepsis es una afección potencialmente mortal provocada por una respuesta extrema del cuerpo a una infección. Requiere intervención médica inmediata para evitar una posible muerte o daños duraderos.... MásPatología
ver canalSistema de imágenes digitales impulsado por IA podría revolucionar el diagnóstico del cáncer
El proceso de biopsia es importante para confirmar la presencia de cáncer. En la técnica de histopatología convencional, el tejido se extirpa, se corta, se tiñe, se monta en... Más
Nuevo panel de mycobacterium tuberculosis respalda la vigilancia en tiempo real y combate la resistencia a los antimicrobianos
La tuberculosis (TB), la principal causa de muerte por enfermedad infecciosa a nivel mundial, es una infección bacteriana contagiosa que se propaga principalmente a través de la tos de pacientes con tuberculosis... Más
Análisis de tejido espacial identifica patrones asociados con la recaída del cáncer de ovario
El carcinoma de ovario seroso de alto grado es el tipo más letal de cáncer de ovario y plantea importantes desafíos de detección. Por lo general, los pacientes responden inicialmente... Más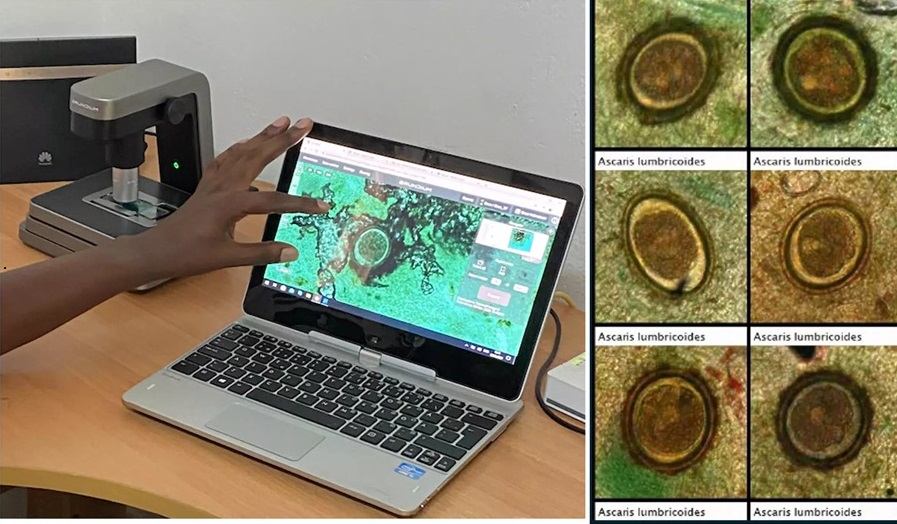
IA basada en imágenes se muestra prometedora para detección de parásitos en muestras de heces digitalizadas
Las infecciones por helmintos transmitidos por el suelo (STH), comúnmente conocidas como gusanos parásitos intestinales, se encuentran entre las enfermedades tropicales desatendidas más... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más













