Un brote de tuberculosis multirresistente no fue detectado usando las pruebas estándar
|
Por el equipo editorial de LabMedica en español Actualizado el 06 Nov 2018 |

Imagen: La prueba de secuenciación profunda Deeplex-MycTB analiza un amplio panel de genes diana en las bacterias y puede identificar resistencia a más de una docena de antibióticos simultáneamente (Fotografía cortesía de Genoscreen).
El diagnóstico rápido de Mycobacterium tuberculosis resistente a los medicamentos antituberculosos es esencial para evitar una mayor adquisición de la resistencia a los medicamentos, una alta morbilidad y mortalidad, y una transmisión ininterrumpida de las cepas resistentes.
La detección rápida de resistencia a la rifampicina, el medicamento más importante contra la tuberculosis, es especialmente crucial porque predice la resistencia a múltiples fármacos, definida como resistencia a al menos isoniazida y rifampicina. El lanzamiento global de ensayos moleculares rápidos revoluciona el diagnóstico de resistencia a la rifampicina, predictiva de resistencia a múltiples fármacos, en la tuberculosis.
Un gran equipo internacional de científicos que trabajan con la Katholieke Universiteit Leuven (Lovaina, Bélgica) examinó los registros de 37.644 cultivos positivos a Mycobacterium tuberculosis de cuatro provincias sudafricanas, para identificar aislamientos con sensibilidad a la rifampicina y resistencia a la isoniazida según las pruebas Xpert MTB/RIF (Cepheid, Sunnyvale, CA, EUA), GenoType MTBDRplus (Hain-Life Science, Nehren, Alemania;) y BACTEC MGIT 960 (Becton, Dickinson and Company, Franklin Lakes, NJ, EUA).
De 1.823 aislamientos que cumplieron con estos criterios, 277 se seleccionaron al azar y se examinaron para la detección de Ile491Phe con PCR multiplex específica de alelo y secuenciación de Sanger de rpoB. Las cepas positivas para Ile491Phe (así como 17 aislamientos portadores Ile491Phe de otro estudio) se analizaron mediante la secuenciación profunda Deeplex-MycTB (Genoscreen, Lille, Francia) y la secuenciación de todo el genoma para evaluar sus patrones de resistencia extensa de transmisión y evolución. La prueba Genoscreen analiza un amplio panel de genes objetivo en la bacteria y puede identificar resistencia a más de una docena de antibióticos simultáneamente.
El equipo identificó Ile491Phe en 37 (15%) de 249 muestras con PCR y resultados de secuenciación múltiplex válidos para alelos, reclasificándolos como resistentes a múltiples medicamentos (MDR). Deeplex-MycTB identificó además los 37 aislamientos como genotípicamente resistentes a todos los medicamentos de primera línea. Seis de los aislamientos sudafricanos albergaron cuatro mutaciones distintas potencialmente asociadas con una disminución de la sensibilidad a la bedaquilina. Consistente con los perfiles genotípicos de Deeplex-MycTB, la secuenciación del genoma completo reveló la propagación silenciosa concurrente en Sudáfrica de un linaje de cepa de tuberculosis MDR que se extiende desde el brote original y al menos otro linaje portador de Ile491Phe independiente que emergió de forma independiente.
Los autores concluyeron que las estrategias diagnósticas actuales no detectan un número importante de casos de tuberculosis MDR que albergan la mutación Ile491Phe en el gen rpoB, lo que resulta en un tratamiento ineficaz de primera línea, una amplificación continua de la resistencia a los medicamentos y una propagación silenciosa concurrente en la comunidad. El estudio fue publicado el 17 de octubre de 2018 en la revista The Lancet Infectious Diseases.
Enlace relacionado:
Katholieke Universiteit Leuven
Cepheid
Hain-Life Science
Becton, Dickinson and Company
Genoscreen
La detección rápida de resistencia a la rifampicina, el medicamento más importante contra la tuberculosis, es especialmente crucial porque predice la resistencia a múltiples fármacos, definida como resistencia a al menos isoniazida y rifampicina. El lanzamiento global de ensayos moleculares rápidos revoluciona el diagnóstico de resistencia a la rifampicina, predictiva de resistencia a múltiples fármacos, en la tuberculosis.
Un gran equipo internacional de científicos que trabajan con la Katholieke Universiteit Leuven (Lovaina, Bélgica) examinó los registros de 37.644 cultivos positivos a Mycobacterium tuberculosis de cuatro provincias sudafricanas, para identificar aislamientos con sensibilidad a la rifampicina y resistencia a la isoniazida según las pruebas Xpert MTB/RIF (Cepheid, Sunnyvale, CA, EUA), GenoType MTBDRplus (Hain-Life Science, Nehren, Alemania;) y BACTEC MGIT 960 (Becton, Dickinson and Company, Franklin Lakes, NJ, EUA).
De 1.823 aislamientos que cumplieron con estos criterios, 277 se seleccionaron al azar y se examinaron para la detección de Ile491Phe con PCR multiplex específica de alelo y secuenciación de Sanger de rpoB. Las cepas positivas para Ile491Phe (así como 17 aislamientos portadores Ile491Phe de otro estudio) se analizaron mediante la secuenciación profunda Deeplex-MycTB (Genoscreen, Lille, Francia) y la secuenciación de todo el genoma para evaluar sus patrones de resistencia extensa de transmisión y evolución. La prueba Genoscreen analiza un amplio panel de genes objetivo en la bacteria y puede identificar resistencia a más de una docena de antibióticos simultáneamente.
El equipo identificó Ile491Phe en 37 (15%) de 249 muestras con PCR y resultados de secuenciación múltiplex válidos para alelos, reclasificándolos como resistentes a múltiples medicamentos (MDR). Deeplex-MycTB identificó además los 37 aislamientos como genotípicamente resistentes a todos los medicamentos de primera línea. Seis de los aislamientos sudafricanos albergaron cuatro mutaciones distintas potencialmente asociadas con una disminución de la sensibilidad a la bedaquilina. Consistente con los perfiles genotípicos de Deeplex-MycTB, la secuenciación del genoma completo reveló la propagación silenciosa concurrente en Sudáfrica de un linaje de cepa de tuberculosis MDR que se extiende desde el brote original y al menos otro linaje portador de Ile491Phe independiente que emergió de forma independiente.
Los autores concluyeron que las estrategias diagnósticas actuales no detectan un número importante de casos de tuberculosis MDR que albergan la mutación Ile491Phe en el gen rpoB, lo que resulta en un tratamiento ineficaz de primera línea, una amplificación continua de la resistencia a los medicamentos y una propagación silenciosa concurrente en la comunidad. El estudio fue publicado el 17 de octubre de 2018 en la revista The Lancet Infectious Diseases.
Enlace relacionado:
Katholieke Universiteit Leuven
Cepheid
Hain-Life Science
Becton, Dickinson and Company
Genoscreen
Últimas Microbiología noticias
- Análisis de sangre predice sepsis e insuficiencia orgánica en niños
- Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
- Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
- Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
- Nuevo análisis para tuberculosis podría ampliar acceso a pruebas en países de ingresos bajos y medios
- Prueba rápida diagnostica enfermedades tropicales en horas para tratamiento con antibióticos más rápido
- Pruebas moleculares rápidas permiten tratamiento antibiótico más rápido y específico para neumonía
- Plataforma rápida de PSA proporciona resultados terapéuticos específicos días antes que el estándar de atención actual
- Nuevo método de análisis detecta patógenos en sangre de forma más rápida y precisa al fundir ADN
- Prueba rápida de sepsis ofrece resultados dos días más rápidos
- Diagnóstico rápido portátil por PCR podría detectar gonorrea y susceptibilidad a antibióticos
- Prueba CRISPR diagnostica mpox más rápido que método de PCR de laboratorio
- Prueba de PCR multiplexada para detección de patógenos y resistencia a antibióticos ayuda a brindar un tratamiento rápido de ITU
- Nuevo algoritmo detecta e identifica nuevos organismos bacterianos
- Analizador de mesa promete detección de ITU en 1 hora e indicación de sensibilidad a antibióticos
- Prueba rápida junto a la cama podría proteger a recién nacidos de enfermedades potencialmente mortales
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Enfoque revolucionario de análisis de células T permite detección temprana del cáncer
La biopsia líquida, un método para diagnosticar el cáncer mediante análisis de sangre de rutina, es una herramienta potencial importante para la detección temprana del... MásPrueba genética única podría acelerar el diagnóstico de trastornos raros del desarrollo
Las alteraciones en el ADN humano varían desde variaciones menores de un solo nucleótido hasta alteraciones sustanciales que implican la eliminación o duplicación de segmentos... Más
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásPatología
ver canal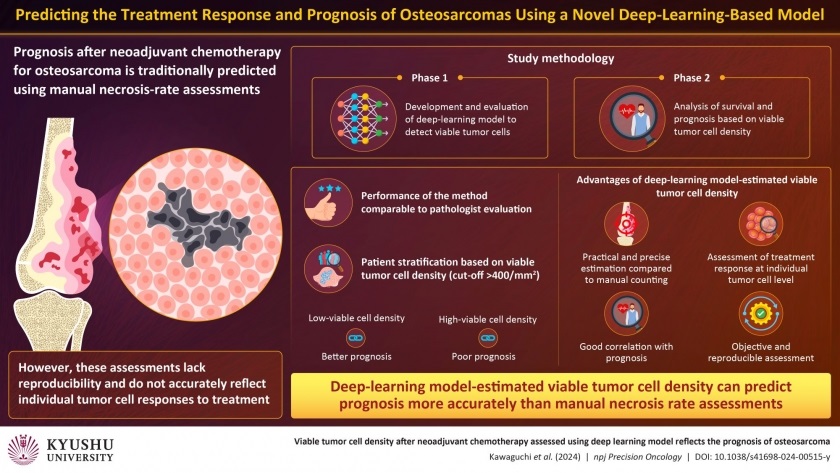
Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico... Más
Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
La comunidad médica mundial reconoce cada vez más que la biopsia líquida es un enfoque transformador para mejorar la atención al paciente con cáncer. Este innovador método de diagnóstico implica detectar... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)

.jpg)