Moderna busca una AUE de la FDA para su vacuna mARN-1273 contra la COVID-19 después de que los datos de fase tres indican una eficacia superior al 94%
|
Por el equipo editorial de LabMedica en español Actualizado el 02 Dec 2020 |
Ilustración
Moderna, Inc. (Cambridge, MA, EUA) solicitó una Autorización de Uso en Emergencias (AUE) a la Administración de Alimentos y Medicamentos de EUA (FDA), para su vacuna candidata, contra la COVID-19, después de que el análisis de eficacia principal del estudio de fase 3 de su vacuna ARNm-1273, confirmó la alta eficacia observada en el primer análisis intermedio.
El análisis de eficacia principal del estudio COVE de fase 3 de la vacuna contra la COVID-19, ARNm-1273, de Moderna, en el que participaron 30.000 participantes incluyó 196 casos de COVID-19, de los cuales 30 fueron graves. El análisis de datos indicó una eficacia de la vacuna del 94,1%. Los datos de seguridad se siguen acumulando y el estudio continúa monitoreado por una Junta de Seguimiento de Seguridad de Datos (DSMB) independiente, designada por los NIH.
El criterio de valoración principal del estudio COVE de fase 3 se basa en el análisis de los casos de COVID-19 confirmados y adjudicados a partir de dos semanas después de la segunda dosis de vacuna. La eficacia de la vacuna se demostró en el primer análisis intermedio con un total de 95 casos según el criterio de eficacia preespecificado de éxito. El análisis principal se basó en 196 casos, de los cuales se observaron 185 casos de COVID-19 en el grupo de placebo versus 11 casos observados en el grupo de ARNm-1273, lo que resultó en una estimación puntual de la eficacia de la vacuna del 94,1%. Los 196 casos de COVID-19 incluyeron 33 adultos mayores (mayores de 65 años) y 42 participantes que se identificaron como de diversas comunidades.
Un criterio de valoración secundario analizó los casos graves de COVID-19 e incluyó 30 casos graves (como se define en el protocolo del estudio) en este análisis. Los 30 casos ocurrieron en el grupo placebo y ninguno en el grupo vacunado con ARNm-1273. Hasta la fecha, hubo una muerte relacionada con COVID-19 en el estudio, que ocurrió en el grupo placebo. El perfil de seguridad del estudio de fase 3 del ARNm-1273 fue el descrito anteriormente. La revisión continua de los datos de seguridad es permanente y la empresa no ha identificado nuevos problemas de seguridad graves. Según un análisis anterior, las reacciones adversas informadas más comúnmente incluyeron dolor en el lugar de la inyección, fatiga, mialgia, artralgia, dolor de cabeza y eritema/enrojecimiento en el lugar de la inyección. Las reacciones adversas reportadas aumentaron en frecuencia y gravedad en el grupo de ARNm-1273 después de la segunda dosis. Además de solicitar una AUE a la FDA, la compañía también presentó una solicitud de Autorización de Comercialización Condicional (CMA) ante la Agencia Europea de Medicamentos.
“Este análisis primario positivo confirma la capacidad de nuestra vacuna para prevenir la enfermedad COVID-19 con una eficacia del 94,1% y, lo que es más importante, la capacidad de prevenir la enfermedad COVID-19 grave. Creemos que nuestra vacuna proporcionará una herramienta nueva y poderosa que puede cambiar el curso de esta pandemia y ayudar a prevenir enfermedades graves, hospitalizaciones y muertes”, dijo Stéphane Bancel, director ejecutivo de Moderna. “Solicitaremos hoy una Autorización de Uso en Emergencias de la FDA y continuaremos avanzando con las revisiones continuas que ya se han iniciado con varias agencias reguladoras de todo el mundo”.
Enlace relacionado:
Moderna, Inc.
El análisis de eficacia principal del estudio COVE de fase 3 de la vacuna contra la COVID-19, ARNm-1273, de Moderna, en el que participaron 30.000 participantes incluyó 196 casos de COVID-19, de los cuales 30 fueron graves. El análisis de datos indicó una eficacia de la vacuna del 94,1%. Los datos de seguridad se siguen acumulando y el estudio continúa monitoreado por una Junta de Seguimiento de Seguridad de Datos (DSMB) independiente, designada por los NIH.
El criterio de valoración principal del estudio COVE de fase 3 se basa en el análisis de los casos de COVID-19 confirmados y adjudicados a partir de dos semanas después de la segunda dosis de vacuna. La eficacia de la vacuna se demostró en el primer análisis intermedio con un total de 95 casos según el criterio de eficacia preespecificado de éxito. El análisis principal se basó en 196 casos, de los cuales se observaron 185 casos de COVID-19 en el grupo de placebo versus 11 casos observados en el grupo de ARNm-1273, lo que resultó en una estimación puntual de la eficacia de la vacuna del 94,1%. Los 196 casos de COVID-19 incluyeron 33 adultos mayores (mayores de 65 años) y 42 participantes que se identificaron como de diversas comunidades.
Un criterio de valoración secundario analizó los casos graves de COVID-19 e incluyó 30 casos graves (como se define en el protocolo del estudio) en este análisis. Los 30 casos ocurrieron en el grupo placebo y ninguno en el grupo vacunado con ARNm-1273. Hasta la fecha, hubo una muerte relacionada con COVID-19 en el estudio, que ocurrió en el grupo placebo. El perfil de seguridad del estudio de fase 3 del ARNm-1273 fue el descrito anteriormente. La revisión continua de los datos de seguridad es permanente y la empresa no ha identificado nuevos problemas de seguridad graves. Según un análisis anterior, las reacciones adversas informadas más comúnmente incluyeron dolor en el lugar de la inyección, fatiga, mialgia, artralgia, dolor de cabeza y eritema/enrojecimiento en el lugar de la inyección. Las reacciones adversas reportadas aumentaron en frecuencia y gravedad en el grupo de ARNm-1273 después de la segunda dosis. Además de solicitar una AUE a la FDA, la compañía también presentó una solicitud de Autorización de Comercialización Condicional (CMA) ante la Agencia Europea de Medicamentos.
“Este análisis primario positivo confirma la capacidad de nuestra vacuna para prevenir la enfermedad COVID-19 con una eficacia del 94,1% y, lo que es más importante, la capacidad de prevenir la enfermedad COVID-19 grave. Creemos que nuestra vacuna proporcionará una herramienta nueva y poderosa que puede cambiar el curso de esta pandemia y ayudar a prevenir enfermedades graves, hospitalizaciones y muertes”, dijo Stéphane Bancel, director ejecutivo de Moderna. “Solicitaremos hoy una Autorización de Uso en Emergencias de la FDA y continuaremos avanzando con las revisiones continuas que ya se han iniciado con varias agencias reguladoras de todo el mundo”.
Enlace relacionado:
Moderna, Inc.
Últimas COVID-19 noticias
- Inmunosensor nuevo allana el camino para pruebas rápidas POC para COVID-19 y enfermedades infecciosas emergentes
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Prueba nueva COVID + Influenza + VSR ayudará a estar preparados para la ‘tripledemia’
- IA elimina las conjeturas de las pruebas de flujo lateral
- Prueba de antígeno del SARS-CoV-2 más rápida, jamás diseñada, permite realizar pruebas de COVID-19 no invasivas en cualquier entorno
- Pruebas rápidas de antígeno detectan las variantes ómicron, delta del SARS-CoV-2
- Prueba en sangre realizada durante la infección inicial predice el riesgo de COVID prolongada
- Investigadores afirman que hay que crear “reservistas” de laboratorio para responder más rápidamente a la próxima pandemia
- Estudio encuentra que los profesionales sanitarios mostraron mayor interés en tecnologías POC durante la pandemia
- Plataforma de análisis de bajo costo para la COVID-19 combina sensibilidad de la PCR y velocidad de pruebas de antígeno
- Prueba de sangre por punción digital identifica inmunidad a la COVID-19
- Kit de prueba rápida determina inmunidad contra la COVID-19 y sus variantes
Canales
Química Clínica
ver canal
Primera prueba integral de sífilis diagnostica definitivamente infección activa en 10 minutos
En Estados Unidos, los casos de sífilis aumentaron casi un 80 % entre 2018 y 2023, con 209.253 casos registrados en el último año con datos. La sífilis, que puede transmitirse... Más
Monitorización con espectrometría de masas predice e identifica recaída temprana del mieloma
El mieloma, un tipo de cáncer que afecta la médula ósea, es actualmente incurable, aunque muchos pacientes pueden vivir más de 10 años tras el diagnóstico.... MásDiagnóstico Molecular
ver canal
Prueba de biopsia líquida detecta recurrencia en pacientes con CCR antes de las imágenes
La detección de ADN tumoral circulante (ADNtc) después del tratamiento es un indicador sólido de recurrencia en el cáncer colorrectal (CCR), pero a menudo pasa desapercibida... Más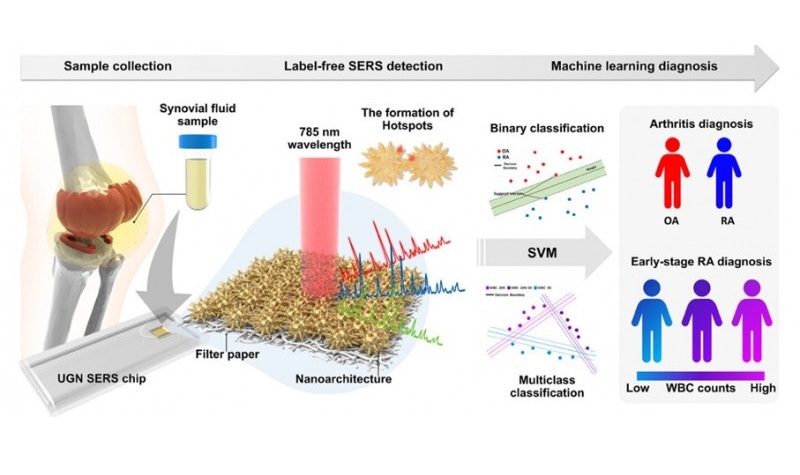
Prueba ultrarrápida de líquido sinovial diagnostica osteoartritis y artritis reumatoide en 10 minutos
Los estudios indican que más del 50 % de las personas mayores de 65 años experimentan síntomas de osteoartritis, mientras que la artritis reumatoide es una enfermedad crónica... MásHematología
ver canal
Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
La citopenia clonal de significado incierto (CCSI) es un trastorno sanguíneo común en adultos mayores, caracterizado por mutaciones en las células sanguíneas y un recuento ... Más
Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
En los Estados Unidos, aproximadamente el 15 % de las embarazadas son RhD negativas. Sin embargo, en aproximadamente el 40 % de estos casos, el feto también es RhD negativo, lo que hace innecesaria la... MásInmunología
ver canal
Prueba de células madre predice resultado del tratamiento en cáncer de ovario resistente al platino
El cáncer de ovario epitelial suele responder inicialmente a la quimioterapia, pero con el tiempo, el tumor desarrolla resistencia a la terapia, lo que provoca su recrecimiento. Esta resistencia... Más
Análisis de sangre con aprendizaje automático predice respuesta a inmunoterapia en pacientes con linfoma
La terapia de células T con receptores de antígenos quiméricos (CAR) se ha convertido en uno de los avances recientes más prometedores en el tratamiento de los cánceres... MásMicrobiología
ver canal
Nueva prueba diagnostica meningitis bacteriana con rapidez y precisión
La meningitis bacteriana es una afección potencialmente mortal: uno de cada seis pacientes fallece y la mitad de los supervivientes experimentan síntomas persistentes. Por lo tanto, un d... Más
Dispositivo portátil ofrece resultados de tuberculosis económico y rápido
La tuberculosis (TB) sigue siendo la enfermedad infecciosa más mortal a nivel mundial, afectando a aproximadamente 10 millones de personas al año. En 2021, alrededor de 4,2 millones de casos... MásPatología
ver canal
Enfoque de biopsia líquida basado en IA revolucionará detección del cáncer cerebral
Detectar cánceres cerebrales sigue siendo extremadamente difícil, ya que muchos pacientes solo reciben un diagnóstico en etapas avanzadas, tras la aparición de síntomas... Más
Análisis de imágenes de patología digital con IA mejora subtipificación del sarcoma pediátrico
Los sarcomas pediátricos son tumores poco frecuentes y diversos que pueden desarrollarse en varios tipos de tejidos blandos, como músculos, tendones, grasa, vasos sanguíneos o lin... MásTecnología
ver canal
Algoritmo de firma de luz permite diagnósticos médicos más rápidos y precisos
Cada material o molécula interactúa con la luz de forma única, creando un patrón distintivo, similar a una huella dactilar. La espectroscopia óptica, que consiste en... Más
Tecnología de microchip desechable podría detectar selectivamente VIH en muestras de sangre completa
A finales de 2023, aproximadamente 40 millones de personas en todo el mundo vivían con VIH, y alrededor de 630.000 personas murieron por enfermedades relacionadas con el sida ese mismo año.... MásIndustria
ver canal
Cepheid y Oxford Nanopore se unen para desarrollar soluciones con secuenciación automatizada
Cepheid (Sunnyvale, CA, EUA), una empresa líder en diagnóstico molecular, y Oxford Nanopore Technologies (Oxford, Reino Unido), la empresa detrás de una nueva generación de... Más









 RapiCardTM InstaTest (Serum-WB-Plasma).jpg)