Lanzan análisis en orina para determinar el riesgo de rechazo del trasplante renal
|
Por el equipo editorial de LabMedica en español Actualizado el 01 Apr 2020 |
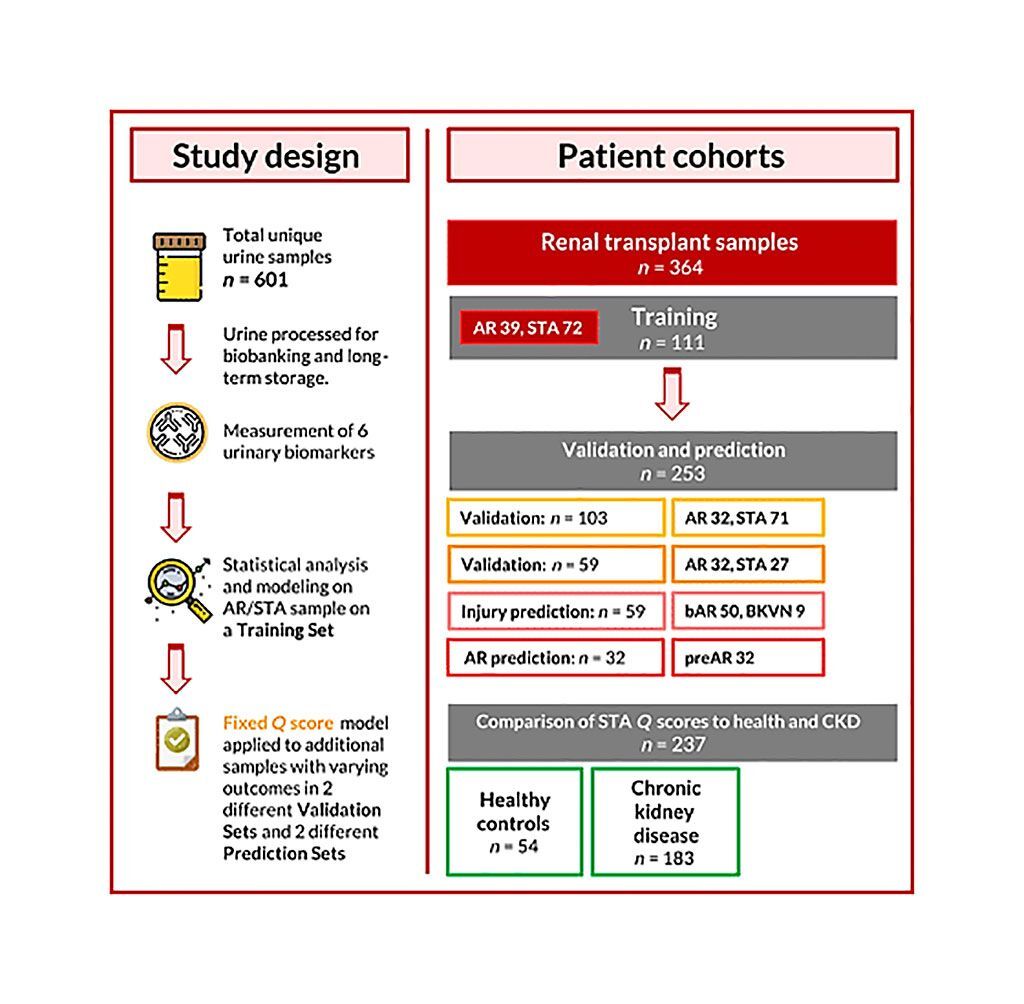
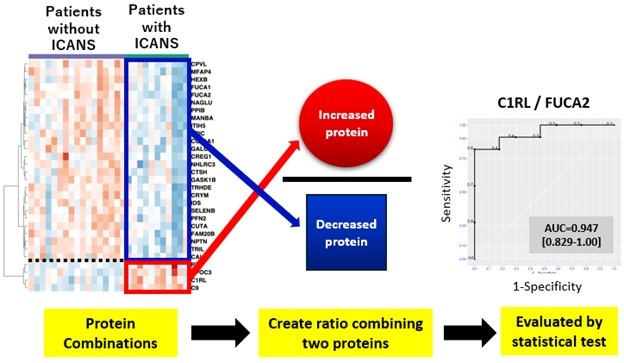
Imagen: Diagrama esquemático de una puntuación de orina para el diagnóstico exacto no invasivo y la predicción del estudio de rechazo de trasplante de riñón (Fotografía cortesía de la Universidad de California, San Francisco).
Para los receptores de trasplante de riñón, la detección rápida y exacta del rechazo de trasplante es vital para una intervención oportuna. Desafortunadamente, el estándar de oro para el diagnóstico de rechazo es la biopsia renal, un procedimiento invasivo.
Para diagnosticar el rechazo agudo en los pacientes con trasplante de riñón, los médicos generalmente extraen varias muestras pequeñas de riñón trasplantado cada pocos meses después del trasplante, además de medir los niveles de creatinina sérica del paciente. Sin embargo, las biopsias renales pueden ser invasivas y costosas, mientras que los niveles séricos de creatinina a menudo son inexactos y no lo suficientemente sensibles como para detectar el rechazo del trasplante.
Científicos de la Universidad de California, San Francisco (San Francisco, CA, EUA) y sus colegas, recolectaron un total de 601 muestras prospectivas de orina de receptores de aloinjertos renales pediátricos y adultos, inmediatamente antes de una biopsia de aloinjerto renal. Cada muestra se emparejó con una biopsia de trasplante renal y se clasificó en los siguientes diagnósticos: estable (170); rechazo agudo (AR, 103); AR límite (bAR, 50); y nefropatía por virus BK (9). El equipo también recolectó muestras de orina adicionales de 32 pacientes con AR antes del episodio de rechazo y las combinó con biopsias.
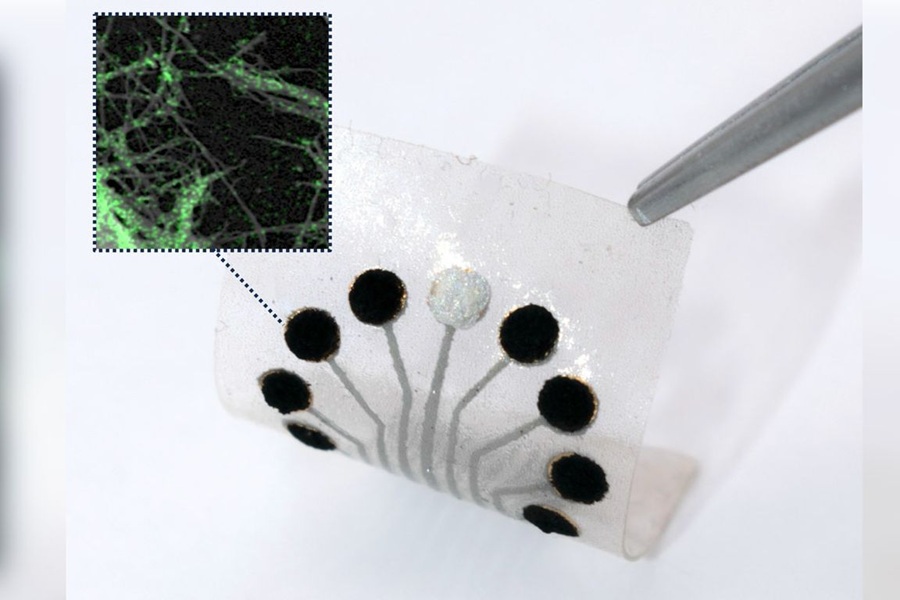
El equipo evaluó un ensayo de diagnóstico no invasivo basado en una muestra puntual de orina, usando mediciones de seis ADN urinarios, proteínas y biomarcadores metabólicos. El equipo utilizó el ensayo QiSant (Nephrosant, San Francisco, CA, EUA) que analiza seis biomarcadores con 4 mL de muestra de orina: la cantidad de ADN libre de células (ADNcf); la fracción de ADNcf metilado; las proteínas clusterina y creatinina; el marcador de inflamación CXCL10; y la cantidad total de proteína en la orina. El ensayo utiliza una herramienta patentada basada en un ensayo inmunosorbente ligado a enzimas (ELISA), que incluye una inmunosonda oligonucleada biotinilada 5', para detectar fragmentos de ADNcf, e inteligencia artificial para estimar la probabilidad de rechazo renal agudo. Después de recolectar muestras de pacientes, los científicos desarrollaron una puntuación Q compuesta, que varía de 0 a 100, en los seis biomarcadores en un conjunto de entrenamiento de 39 pacientes con AR y 72 pacientes estables (STA).
En el primer conjunto de validación, que tenía 32 pacientes con AR y 71 pacientes con STA, el grupo encontró que la puntuación entre los tipos de pacientes tenía aproximadamente un 91% de sensibilidad y un 92% de especificidad clínicas. Mientras tanto, en un segundo conjunto de validación de 32 pacientes con AR y 27 pacientes con STA, el equipo descubrió que el puntaje escalado tenía una sensibilidad del 100% y una especificidad del 96%. La mayoría de los pacientes con muestras (159) con puntuaciones superiores al umbral de AR tuvieron un diagnóstico clínico de AR activa, AR temprana, o desarrollaron AR confirmada por biopsia hasta 200 días después de usar el ensayo QiSant.
Los autores concluyeron que habían demostrado la utilidad clínica de este ensayo para predecir el AR antes de un aumento en la creatinina sérica, lo que permite una detección más temprana del rechazo de lo que actualmente es posible mediante pruebas estándar de atención. Este método no invasivo, sensible y cuantitativo es un método robusto e informativo para el seguimiento rápido y rutinario de aloinjertos renales. El estudio fue publicado el 18 de marzo de 2020 en la revista Science Translational Medicine.
Enlace relacionado:
Universidad de California, San Francisco
Nephrosant
Para diagnosticar el rechazo agudo en los pacientes con trasplante de riñón, los médicos generalmente extraen varias muestras pequeñas de riñón trasplantado cada pocos meses después del trasplante, además de medir los niveles de creatinina sérica del paciente. Sin embargo, las biopsias renales pueden ser invasivas y costosas, mientras que los niveles séricos de creatinina a menudo son inexactos y no lo suficientemente sensibles como para detectar el rechazo del trasplante.
Científicos de la Universidad de California, San Francisco (San Francisco, CA, EUA) y sus colegas, recolectaron un total de 601 muestras prospectivas de orina de receptores de aloinjertos renales pediátricos y adultos, inmediatamente antes de una biopsia de aloinjerto renal. Cada muestra se emparejó con una biopsia de trasplante renal y se clasificó en los siguientes diagnósticos: estable (170); rechazo agudo (AR, 103); AR límite (bAR, 50); y nefropatía por virus BK (9). El equipo también recolectó muestras de orina adicionales de 32 pacientes con AR antes del episodio de rechazo y las combinó con biopsias.
El equipo evaluó un ensayo de diagnóstico no invasivo basado en una muestra puntual de orina, usando mediciones de seis ADN urinarios, proteínas y biomarcadores metabólicos. El equipo utilizó el ensayo QiSant (Nephrosant, San Francisco, CA, EUA) que analiza seis biomarcadores con 4 mL de muestra de orina: la cantidad de ADN libre de células (ADNcf); la fracción de ADNcf metilado; las proteínas clusterina y creatinina; el marcador de inflamación CXCL10; y la cantidad total de proteína en la orina. El ensayo utiliza una herramienta patentada basada en un ensayo inmunosorbente ligado a enzimas (ELISA), que incluye una inmunosonda oligonucleada biotinilada 5', para detectar fragmentos de ADNcf, e inteligencia artificial para estimar la probabilidad de rechazo renal agudo. Después de recolectar muestras de pacientes, los científicos desarrollaron una puntuación Q compuesta, que varía de 0 a 100, en los seis biomarcadores en un conjunto de entrenamiento de 39 pacientes con AR y 72 pacientes estables (STA).
En el primer conjunto de validación, que tenía 32 pacientes con AR y 71 pacientes con STA, el grupo encontró que la puntuación entre los tipos de pacientes tenía aproximadamente un 91% de sensibilidad y un 92% de especificidad clínicas. Mientras tanto, en un segundo conjunto de validación de 32 pacientes con AR y 27 pacientes con STA, el equipo descubrió que el puntaje escalado tenía una sensibilidad del 100% y una especificidad del 96%. La mayoría de los pacientes con muestras (159) con puntuaciones superiores al umbral de AR tuvieron un diagnóstico clínico de AR activa, AR temprana, o desarrollaron AR confirmada por biopsia hasta 200 días después de usar el ensayo QiSant.
Los autores concluyeron que habían demostrado la utilidad clínica de este ensayo para predecir el AR antes de un aumento en la creatinina sérica, lo que permite una detección más temprana del rechazo de lo que actualmente es posible mediante pruebas estándar de atención. Este método no invasivo, sensible y cuantitativo es un método robusto e informativo para el seguimiento rápido y rutinario de aloinjertos renales. El estudio fue publicado el 18 de marzo de 2020 en la revista Science Translational Medicine.
Enlace relacionado:
Universidad de California, San Francisco
Nephrosant
Últimas Patología noticias
- Modelo de IA predice eficazmente resultados de pacientes con cáncer de pulmón
- Modelo de IA predice respuesta al tratamiento del cáncer de vejiga
- Nuevo método basado en láser acelera diagnóstico del cáncer
- Nuevo modelo de IA predice efectos de variantes genéticas en enfermedades específicas
- Herramienta de IA diagnostica enfermedad celíaca en imágenes de biopsia con precisión superior al 97%
- Condiciones preanalíticas influyen en estabilidad de microARN libres de células en muestras de plasma sanguíneo
- Sistema de cultivo celular 3D podría revolucionar diagnóstico del cáncer
- Técnica indolora mide concentraciones de glucosa en solución y tejido mediante ondas sonoras
- Prueba cutánea mejora diagnóstico de enfermedades neurodegenerativas raras y debilitantes
- Uromodulina sérica podría indicar lesión renal aguda en pacientes con COVID-19
- Modelo de IA revela edad biológica real con cinco gotas de sangre
- Herramienta de IA pionera visualiza la "red social" de las células para tratar el cáncer
- Prueba diagnostica tumores cerebrales infantiles de alto riesgo
- Dispositivo microfluídico evalúa adherencia de células tumorales para predecir propagación del cáncer
- Nueva herramienta de IA mejora métodos anteriores para identificar cáncer colorrectal en muestras de tejido
- Técnica predice tumores agresivos antes de que hagan metástasis
Canales
Química Clínica
ver canal
Nanotubos de carbono ayudan a construir sensores precisos para monitoreo continuo de la salud
Los sensores actuales pueden medir diversos indicadores de salud, como los niveles de glucosa en sangre. Sin embargo, es necesario desarrollar materiales para sensores más precisos y sensibles que... Más
Dispositivo basado en papel mejora la precisión de prueba del VIH
En las regiones donde el acceso a las clínicas para realizar análisis de sangre rutinarios presenta obstáculos financieros y logísticos, los pacientes con VIH pueden recolectar... MásDiagnóstico Molecular
ver canal
Primera prueba que utiliza microARN para predecir toxicidad de terapia contra el cáncer
Muchos hombres con cáncer de próstata en etapa temprana reciben radioterapia corporal estereotáctica (RTCE), un tratamiento de radiación de alta precisión que se completa... MásEnsayo basado en células proporciona detección sensible y específica de autoanticuerpos en desmielinización
Los anticuerpos anti-glicoproteína asociada a la mielina (MAG) sirven como marcadores de un trastorno desmielinizante autoinmune que afecta al sistema nervioso periférico y provoca deterioro sensorial.... MásHematología
ver canal
Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
La citopenia clonal de significado incierto (CCSI) es un trastorno sanguíneo común en adultos mayores, caracterizado por mutaciones en las células sanguíneas y un recuento ... Más
Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
En los Estados Unidos, aproximadamente el 15 % de las embarazadas son RhD negativas. Sin embargo, en aproximadamente el 40 % de estos casos, el feto también es RhD negativo, lo que hace innecesaria la... MásInmunología
ver canal
Prueba de células madre predice resultado del tratamiento en cáncer de ovario resistente al platino
El cáncer de ovario epitelial suele responder inicialmente a la quimioterapia, pero con el tiempo, el tumor desarrolla resistencia a la terapia, lo que provoca su recrecimiento. Esta resistencia... Más
Análisis de sangre con aprendizaje automático predice respuesta a inmunoterapia en pacientes con linfoma
La terapia de células T con receptores de antígenos quiméricos (CAR) se ha convertido en uno de los avances recientes más prometedores en el tratamiento de los cánceres... MásMicrobiología
ver canal
Método basado en IA mejora diagnóstico de infecciones resistentes a fármacos
Las infecciones resistentes a los medicamentos, en particular las causadas por bacterias mortales como la tuberculosis y el estafilococo, se están convirtiendo rápidamente en una emergencia... Más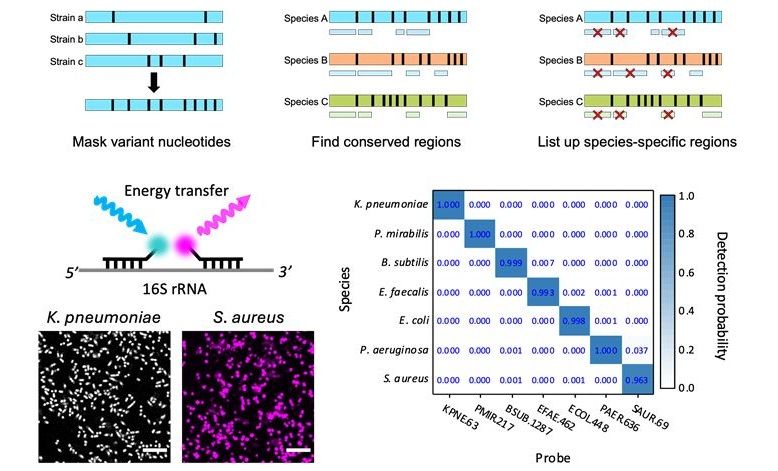
Innovadora tecnología disgnóstica identifica infecciones bacterianas con precisión de casi 100 % en tres horas
La identificación rápida y precisa de microbios patógenos en muestras de pacientes es esencial para el tratamiento eficaz de enfermedades infecciosas agudas, como la sepsis.... MásTecnología
ver canal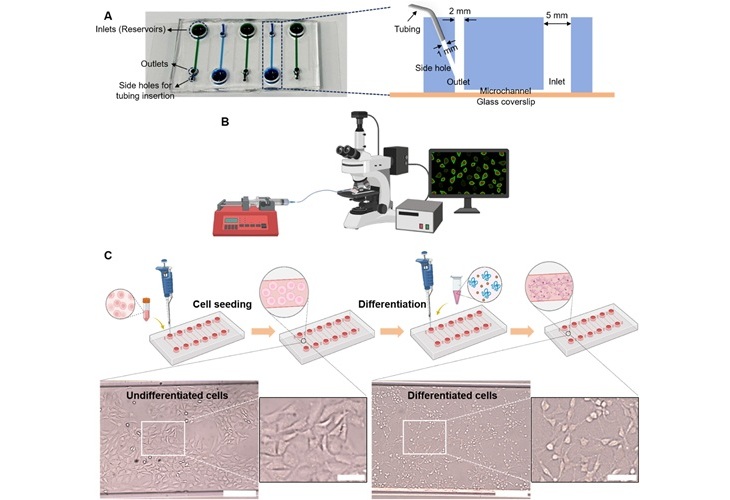
Dispositivo microfluídico Dolor en un Chip determina tipos de dolor crónico desde muestras de sangre
El dolor crónico es una afección generalizada que sigue siendo difícil de controlar, y los métodos clínicos existentes para su tratamiento se basan en gran medida en... Más
Innovador sensor fluorométrico sin etiquetas permite detección más sensible del ARN viral
Los virus representan un importante riesgo para la salud mundial, como lo demuestran las recientes pandemias, lo que hace que la detección e identificación tempranas sean esenciales para... MásIndustria
ver canal
Cepheid y Oxford Nanopore se unen para desarrollar soluciones con secuenciación automatizada
Cepheid (Sunnyvale, CA, EUA), una empresa líder en diagnóstico molecular, y Oxford Nanopore Technologies (Oxford, Reino Unido), la empresa detrás de una nueva generación de... Más