Aprueban análisis de sangre de próxima generación
|
Por el equipo editorial de LabMedica en español Actualizado el 24 Jul 2017 |

Imagen: La nueva prueba en sangre QuantiFERON-TB Gold Plus para la TB latente (Fotografía cortesía de QIAGEN).
La Agencia de Alimentos y Medicamentos de los Estados Unidos (FDA, por sus siglas en inglés), aprobó un ensayo de próxima generación para la infección latente por tuberculosis (TB), que combina el diseño de vanguardia para el análisis de CD4/CD8, para la detección de la respuesta inmune con un flujo de trabajo flexible de recolección de sangre.
La prueba aprobada por la FDA, QuantiFERON-TB Gold Plus (QFT-Plus) es la prueba en sangre de cuarta generación de QIAGEN (Germantown, MD, EUA y Hilden, Alemania) para la detección de la infección latente por TB. La prueba QFT-Plus se basa en la prueba, QuantiFERON-TB Gold (QFT), la versión de tercera generación del análisis de liberación del interferón gamma (IGRA) de Qiagen La prueba QFT es un análisis bien ensayado, con un vasto cuerpo de evidencia clínica, que se usa como una herramienta rentable y eficiente para las pruebas de infección por TB. La disponibilidad en los EUA está planeada para comenzar a finales de este año (2017).
“Estamos complacidos por la oportuna aprobación de la FDA para la prueba QuantiFERON-TB Gold Plus y que ahora podemos traer una gama de beneficios clínicos y de flujo de trabajo muy atractivos para los clientes”, dijo Thierry Bernard, vicepresidente senior y responsable del Área de Negocios de Diagnóstico Molecular de QIAGEN, “La tuberculosis es una enfermedad global que tiene un impacto en los Estados Unidos, donde hasta 13 millones de personas están infectadas y cerca de 10.000 personas padecen actualmente una enfermedad activa”.
Con la adición de la tecnología patentada, CD8+, QFT-Plus representa un hito clave en el desarrollo de pruebas de diagnóstico para la infección latente por TB. Por primera vez, una prueba tiene el potencial de ofrecer la capacidad de capturar una imagen mucho más amplia de la respuesta inmune de un individuo a la infección de TB. Este avance tecnológico es fundamental para mejorar la comprensión de cómo el sistema inmunológico reacciona a la infección de tuberculosis y se espera que establezca un nuevo estándar para el manejo de la enfermedad en el futuro.
Entre las nuevas características de la prueba, QFT-Plus, está la flexibilidad del flujo de trabajo que permite una implementación aún más eficiente, especialmente en los programas de detección de TB a gran escala. Éstos incluyen una opción estándar para la recolección de la sangre de un solo tubo, que permite que las muestras de sangre sean procesadas hasta 53 horas después la venopunción sin afectar la exactitud de la prueba. Esto se suma al diseño existente, único de “ensayo en el tubo de recolección” que permite la estimulación inmediata de la muestra de sangre.
Otra nueva característica incluye avances para apoyar la investigación sobre la estratificación del riesgo de que las infecciones latentes por TB se convierten en una enfermedad activa, basada en la incorporación, por primera vez, de los datos de respuesta de las células T CD8+, que proporcionan información valiosa mediante la medición de un rango más amplio de respuesta inmune. La evidencia científica publicada pone de relieve el potencial futuro de las células T CD8 + para diferenciar la TB activa de la latente, detectar infecciones recientes o antiguas, detectar la TB en ciertas poblaciones de riesgo (como la coinfección por VIH y los niños pequeños) y para evaluar la respuesta de la tuberculosis al tratamiento.
La prueba QFT-Plus está programado para ser lanzada en los EUA en medio de nuevas recomendaciones que amplian el uso de las IGRA. En diciembre de 2016, un grupo de trabajo apoyado por la Sociedad Americana del Tórax (ATS), los Centros para el Control y la Prevención de Enfermedades (CDC por su sigla en inglés) y la Sociedad de Enfermedades Infecciosas de América, publicó nuevas guías basadas en evidencia que recomendaban el uso de pruebas IGRA en grupos más amplios de personas con riesgo de contraer la tuberculosis. Esto siguió a las recomendaciones del Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF, por su sigla en inglés) en septiembre de 2016, de que los médicos de atención primaria deben examinar a los pacientes adultos pertenecientes a los grupos con riesgo alto de infección latente por TB. Ambos se refirieron a la QFT como una IGRA aprobada por la FDA en ese momento, preferible en ciertos grupos de pacientes a la prueba cutánea centenaria de la tuberculina (TST).
Hasta la fecha, nueve publicaciones independientes, revisadas por pares, han apoyado el desempeño de la prueba QFT-Plus, y los estudios adicionales en curso en 22 países involucran a más de 30,000 pacientes. La QFT-Plus es la única prueba IGRA para la TB en curso a ser evaluada por la Organización Mundial de la Salud (OMS) como parte de su campaña mundial para erradicar la enfermedad.
La prueba aprobada por la FDA, QuantiFERON-TB Gold Plus (QFT-Plus) es la prueba en sangre de cuarta generación de QIAGEN (Germantown, MD, EUA y Hilden, Alemania) para la detección de la infección latente por TB. La prueba QFT-Plus se basa en la prueba, QuantiFERON-TB Gold (QFT), la versión de tercera generación del análisis de liberación del interferón gamma (IGRA) de Qiagen La prueba QFT es un análisis bien ensayado, con un vasto cuerpo de evidencia clínica, que se usa como una herramienta rentable y eficiente para las pruebas de infección por TB. La disponibilidad en los EUA está planeada para comenzar a finales de este año (2017).
“Estamos complacidos por la oportuna aprobación de la FDA para la prueba QuantiFERON-TB Gold Plus y que ahora podemos traer una gama de beneficios clínicos y de flujo de trabajo muy atractivos para los clientes”, dijo Thierry Bernard, vicepresidente senior y responsable del Área de Negocios de Diagnóstico Molecular de QIAGEN, “La tuberculosis es una enfermedad global que tiene un impacto en los Estados Unidos, donde hasta 13 millones de personas están infectadas y cerca de 10.000 personas padecen actualmente una enfermedad activa”.
Con la adición de la tecnología patentada, CD8+, QFT-Plus representa un hito clave en el desarrollo de pruebas de diagnóstico para la infección latente por TB. Por primera vez, una prueba tiene el potencial de ofrecer la capacidad de capturar una imagen mucho más amplia de la respuesta inmune de un individuo a la infección de TB. Este avance tecnológico es fundamental para mejorar la comprensión de cómo el sistema inmunológico reacciona a la infección de tuberculosis y se espera que establezca un nuevo estándar para el manejo de la enfermedad en el futuro.
Entre las nuevas características de la prueba, QFT-Plus, está la flexibilidad del flujo de trabajo que permite una implementación aún más eficiente, especialmente en los programas de detección de TB a gran escala. Éstos incluyen una opción estándar para la recolección de la sangre de un solo tubo, que permite que las muestras de sangre sean procesadas hasta 53 horas después la venopunción sin afectar la exactitud de la prueba. Esto se suma al diseño existente, único de “ensayo en el tubo de recolección” que permite la estimulación inmediata de la muestra de sangre.
Otra nueva característica incluye avances para apoyar la investigación sobre la estratificación del riesgo de que las infecciones latentes por TB se convierten en una enfermedad activa, basada en la incorporación, por primera vez, de los datos de respuesta de las células T CD8+, que proporcionan información valiosa mediante la medición de un rango más amplio de respuesta inmune. La evidencia científica publicada pone de relieve el potencial futuro de las células T CD8 + para diferenciar la TB activa de la latente, detectar infecciones recientes o antiguas, detectar la TB en ciertas poblaciones de riesgo (como la coinfección por VIH y los niños pequeños) y para evaluar la respuesta de la tuberculosis al tratamiento.
La prueba QFT-Plus está programado para ser lanzada en los EUA en medio de nuevas recomendaciones que amplian el uso de las IGRA. En diciembre de 2016, un grupo de trabajo apoyado por la Sociedad Americana del Tórax (ATS), los Centros para el Control y la Prevención de Enfermedades (CDC por su sigla en inglés) y la Sociedad de Enfermedades Infecciosas de América, publicó nuevas guías basadas en evidencia que recomendaban el uso de pruebas IGRA en grupos más amplios de personas con riesgo de contraer la tuberculosis. Esto siguió a las recomendaciones del Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF, por su sigla en inglés) en septiembre de 2016, de que los médicos de atención primaria deben examinar a los pacientes adultos pertenecientes a los grupos con riesgo alto de infección latente por TB. Ambos se refirieron a la QFT como una IGRA aprobada por la FDA en ese momento, preferible en ciertos grupos de pacientes a la prueba cutánea centenaria de la tuberculina (TST).
Hasta la fecha, nueve publicaciones independientes, revisadas por pares, han apoyado el desempeño de la prueba QFT-Plus, y los estudios adicionales en curso en 22 países involucran a más de 30,000 pacientes. La QFT-Plus es la única prueba IGRA para la TB en curso a ser evaluada por la Organización Mundial de la Salud (OMS) como parte de su campaña mundial para erradicar la enfermedad.
Últimas Microbiología noticias
- Dispositivo portátil ofrece resultados de tuberculosis económico y rápido
- Método basado en IA mejora diagnóstico de infecciones resistentes a fármacos
- Innovadora tecnología disgnóstica identifica infecciones bacterianas con precisión de casi 100 % en tres horas
- Sistema de identificación y PSA ayuda a diagnosticar enfermedades infecciosas y combatir RAM
- Panel gastrointestinal permite detección rápida de cinco patógenos bacterianos comunes
- Pruebas rápidas PCR en UCI mejoran uso de antibióticos
- Firma genética única predice resistencia a fármacos en bacterias
- Sistema de código de barras rastrea bacterias de neumonía mientras infectan el torrente sanguíneo
- Prueba rápida de diagnóstico de sepsis demuestra mejor atención al paciente y ahorro en aplicaciones hospitalarias
- Sistema de diagnóstico rápido detecta sepsis neonatal en horas
- Nueva prueba diagnostica neumonía bacteriana directamente a partir de sangre completa
- Ensayo de liberación de interferón-γ es eficaz en pacientes con EPOC y tuberculosis pulmonar
- Nuevas pruebas en punto de atención ayudan a reducir uso excesivo de antibióticos
- Prueba de sepsis rápida permite diferenciar infecciones bacterianas, virales y enfermedades no infecciosas
- Prueba CRISPR-TB permite diagnóstico temprano de enfermedad y cribado de la población
- Panel sindrómico ofrece respuestas rápidas para diagnóstico ambulatorio de enfermedades gastrointestinales
Canales
Química Clínica
ver canal
Herramienta química a nanoescala 'brillantemente luminosa' mejora detección de enfermedades
Miles de moléculas brillantes disponibles comercialmente, conocidas como fluoróforos, se utilizan comúnmente en imágenes médicas, detección de enfermedades, marcado... Más
Prueba de detección portátil económica transforma detección de enfermedades renales
Millones de personas padecen enfermedad renal, que a menudo permanece sin diagnosticar hasta que alcanza una etapa crítica. Esta epidemia silenciosa no solo disminuye la calidad de vida de los afectados,... MásDiagnóstico Molecular
ver canal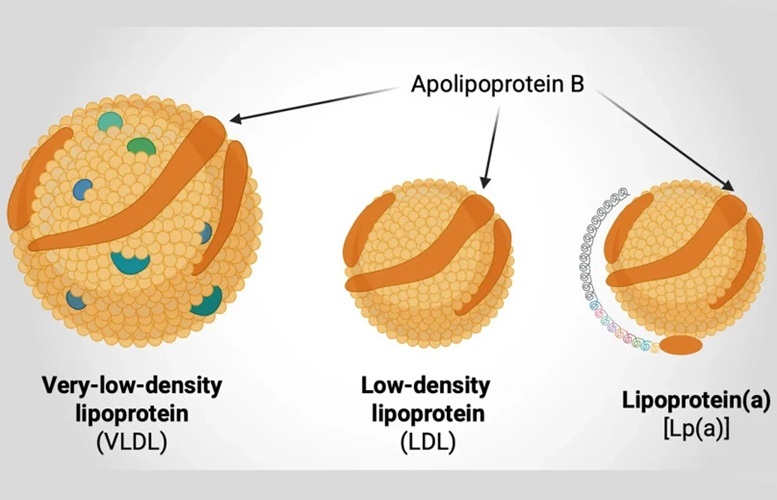
Simple análisis de sangre predice mejor riesgo de enfermedad cardíaca
Las enfermedades cardiovasculares (ECV) son la principal causa de muerte en todo el mundo. Una gran proporción de estos casos podría prevenirse abordando factores ambientales y de estilo... Más
Nuevo análisis de sangre detecta 12 cánceres antes de que aparezcan síntomas
El cáncer de intestino es el cuarto cáncer más común en el Reino Unido, con más de 42.000 nuevos diagnósticos cada año. Detectarlo en sus primeras etapas... MásHematología
ver canal
Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
La citopenia clonal de significado incierto (CCSI) es un trastorno sanguíneo común en adultos mayores, caracterizado por mutaciones en las células sanguíneas y un recuento ... Más
Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
En los Estados Unidos, aproximadamente el 15 % de las embarazadas son RhD negativas. Sin embargo, en aproximadamente el 40 % de estos casos, el feto también es RhD negativo, lo que hace innecesaria la... MásInmunología
ver canal
Prueba de células madre predice resultado del tratamiento en cáncer de ovario resistente al platino
El cáncer de ovario epitelial suele responder inicialmente a la quimioterapia, pero con el tiempo, el tumor desarrolla resistencia a la terapia, lo que provoca su recrecimiento. Esta resistencia... Más
Análisis de sangre con aprendizaje automático predice respuesta a inmunoterapia en pacientes con linfoma
La terapia de células T con receptores de antígenos quiméricos (CAR) se ha convertido en uno de los avances recientes más prometedores en el tratamiento de los cánceres... MásPatología
ver canal
Kits de ensayo de enzima DUB sensibles y específicos requieren configuración mínima sin preparación del sustrato
La ubiquitinación y la desubiquitinación son dos procesos fisiológicos importantes en el sistema ubiquitina-proteasoma, responsable de la degradación de proteínas en... Más
Primer modelo de IA para diagnóstico de cáncer de tiroides con precisión superior al 90 %
El cáncer de tiroides es uno de los cánceres más comunes en todo el mundo, y su manejo preciso generalmente se basa en dos sistemas principales: (1) la 8va edición del Comité... MásTecnología
ver canal
Tecnología de microchip desechable podría detectar selectivamente VIH en muestras de sangre completa
A finales de 2023, aproximadamente 40 millones de personas en todo el mundo vivían con VIH, y alrededor de 630.000 personas murieron por enfermedades relacionadas con el sida ese mismo año.... Más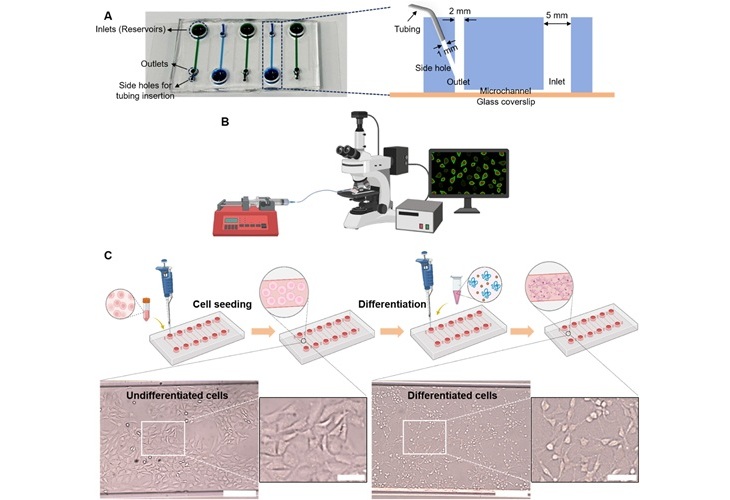
Dispositivo microfluídico Dolor en un Chip determina tipos de dolor crónico desde muestras de sangre
El dolor crónico es una afección generalizada que sigue siendo difícil de controlar, y los métodos clínicos existentes para su tratamiento se basan en gran medida en... MásIndustria
ver canal
Cepheid y Oxford Nanopore se unen para desarrollar soluciones con secuenciación automatizada
Cepheid (Sunnyvale, CA, EUA), una empresa líder en diagnóstico molecular, y Oxford Nanopore Technologies (Oxford, Reino Unido), la empresa detrás de una nueva generación de... Más