Qiagen y Clovis Oncology desarrollarán diagnóstico con fines terapéuticos
|
Por el equipo editorial de LabMedica en español Actualizado el 14 Nov 2013 |
Qiagen (Hilden, Alemania) se asociará con Clovis Oncology (Germantown, MD, EUA) para desarrollar una prueba diagnóstica con fines terapéuticos dirigida a las mutaciones resistentes a medicamentos del receptor de factor de crecimiento epidérmico (EGFR).
El proyecto de colaboración permitirá la expansión de la marca del estuche de Qiagen aprobado por la Administración de Alimentos y Medicamentos (FDA) de reacción en cadena de la polimerasa (RCP) Therascreen (EGFR) Rotor Gene Q (RGQ) y crear el marco para una sociedad a largo plazo de desarrollo y comercialización. La prueba diagnóstica con fines terapéuticos servirá de guía de uso del nuevo producto candidato CO-1686 de Clovis Oncology que se encuentra actualmente en la fase de desarrollo clínico. El fármaco candidato Clovis estará dirigido inicialmente a satisfacer una necesidad clínica en pacientes con cáncer de pulmón de células no pequeñas (NSCLC) provocado por el receptor del factor de crecimiento epidérmico (EGFR), en quienes los inhibidores actuales de EFGR ya no logran controlar la enfermedad.
La nueva prueba se basará en el estuche therascreen EGFR RGQ PCR Kit de Qiagen, que obtuvo la aprobación de la FDA en julio de 2013 como prueba diagnóstica con fines terapéuticos en el tratamiento de pacientes de NSCLC metastásico cuyos tumores tienen ciertas mutaciones de EGFR. Se ha establecido el desempeño analítico de la prueba therascreen EGFR en 21 mutaciones de EGFR, incluso la mutación de resistencia de mayor prevalencia, T790M. La prueba respalda el eficiente flujo de trabajo de laboratorio con tecnología de RCP en tiempo real por medio del instrumento Rotor-Gene Q MDx —aprobado por la FDA—, parte de la familia de soluciones de laboratorio QIAsymphony.
El plan de desarrollo de la nueva prueba complementa el plan de Clovis Oncology de acelerar el desarrollo de CO-1686, por medio de una potencial solicitud de autorización previa a la comercialización (APC) para la aplicación diagnóstica. Sujeta a las aprobaciones regulatorias, Qiagen será responsable del desarrollo y comercialización global de la prueba diagnóstica con fines terapéuticos y Clovis estará a cargo del desarrollo y comercialización global de CO-1686. Los socios también crearon un marco para posibles proyectos futuros en colaboración, para lo cual agregaron otro acuerdo maestro a la creciente cartera de proyectos de Qiagen en colaboración con algunas de las principales empresas farmacéuticas y biotecnológicas del mundo. No se develaron el resto de los términos del acuerdo.
“Estamos complacidos de asociarnos con Clovis Oncology en el desarrollo de la prueba diagnóstica con fines terapéuticos basada en la tecnología therascreen de Qiagen y expandir la marca del estuche therascreen EGFR aprobado. Juntos podemos acelerar el desarrollo de este importante fármaco candidato y proporcionar una solución para una necesidad médica insatisfecha,” dijo Peer Schatz, presidente ejecutivo de Qiagen. “Nuestro estuche therascreen EGFR, aprobado por la FDA en base a amplia información analítica y clínica, es la prueba más completa y ofrece características únicas como la detección de mutaciones puntuales en tubos separados. Qiagen es un socio de preferencia en medicina personalizada debido a la capacidad de ofrecer resultados reproducibles, plataformas de flujo de trabajo eficiente y antecedentes en desarrollos y autorizaciones regulatorias.”
La plataforma Rotor-Gene Q MDx, adoptada por la mayoría de los principales laboratorios estadounidenses y muchos laboratorios en el mundo, procesa un menú cada vez mayor de pruebas moleculares. La plataforma Rotor-Gene Q MDx está aprobada en los EUA para el uso del estuche de prueba therascreen KRAS RGQ PCR de Qiagen en pacientes con cáncer colorrectal y la prueba therascreen EGFR en pacientes con NSCLC metastásico, productos importantes de la medicina personalizada.
Qiagen continúa con la expansión de su cartera de tecnologías de medicina personalizada y pretende solicitar la aprobación regulatoria de mayor cantidad de pruebas en el mundo compatibles con la plataforma Rotor-Gene Q MDx. La empresa tiene más de 15 proyectos de desarrollo y comercialización de pruebas diagnósticas con fines terapéuticos en conjunto con empresas farmacéuticas y biotecnológicas como Amgen, AstraZeneca, Bayer, Bristol-Myers Squibb, Eli Lilly and Company y Pfizer. Qiagen está desarrollando numerosas pruebas diagnósticas con fines terapéuticos, además de una línea de pruebas moleculares, como parte de un amplio menú de pruebas confiables y rentables de diagnóstico molecular.
Clovis Oncology es una empresa biofarmacéutica centrada en la adquisición, desarrollo y comercialización de tratamientos oncológicos en los Estados Unidos, Europa y otros mercados internacionales.
Enlaces relacionados:
Qiagen
Clovis Oncology
El proyecto de colaboración permitirá la expansión de la marca del estuche de Qiagen aprobado por la Administración de Alimentos y Medicamentos (FDA) de reacción en cadena de la polimerasa (RCP) Therascreen (EGFR) Rotor Gene Q (RGQ) y crear el marco para una sociedad a largo plazo de desarrollo y comercialización. La prueba diagnóstica con fines terapéuticos servirá de guía de uso del nuevo producto candidato CO-1686 de Clovis Oncology que se encuentra actualmente en la fase de desarrollo clínico. El fármaco candidato Clovis estará dirigido inicialmente a satisfacer una necesidad clínica en pacientes con cáncer de pulmón de células no pequeñas (NSCLC) provocado por el receptor del factor de crecimiento epidérmico (EGFR), en quienes los inhibidores actuales de EFGR ya no logran controlar la enfermedad.
La nueva prueba se basará en el estuche therascreen EGFR RGQ PCR Kit de Qiagen, que obtuvo la aprobación de la FDA en julio de 2013 como prueba diagnóstica con fines terapéuticos en el tratamiento de pacientes de NSCLC metastásico cuyos tumores tienen ciertas mutaciones de EGFR. Se ha establecido el desempeño analítico de la prueba therascreen EGFR en 21 mutaciones de EGFR, incluso la mutación de resistencia de mayor prevalencia, T790M. La prueba respalda el eficiente flujo de trabajo de laboratorio con tecnología de RCP en tiempo real por medio del instrumento Rotor-Gene Q MDx —aprobado por la FDA—, parte de la familia de soluciones de laboratorio QIAsymphony.
El plan de desarrollo de la nueva prueba complementa el plan de Clovis Oncology de acelerar el desarrollo de CO-1686, por medio de una potencial solicitud de autorización previa a la comercialización (APC) para la aplicación diagnóstica. Sujeta a las aprobaciones regulatorias, Qiagen será responsable del desarrollo y comercialización global de la prueba diagnóstica con fines terapéuticos y Clovis estará a cargo del desarrollo y comercialización global de CO-1686. Los socios también crearon un marco para posibles proyectos futuros en colaboración, para lo cual agregaron otro acuerdo maestro a la creciente cartera de proyectos de Qiagen en colaboración con algunas de las principales empresas farmacéuticas y biotecnológicas del mundo. No se develaron el resto de los términos del acuerdo.
“Estamos complacidos de asociarnos con Clovis Oncology en el desarrollo de la prueba diagnóstica con fines terapéuticos basada en la tecnología therascreen de Qiagen y expandir la marca del estuche therascreen EGFR aprobado. Juntos podemos acelerar el desarrollo de este importante fármaco candidato y proporcionar una solución para una necesidad médica insatisfecha,” dijo Peer Schatz, presidente ejecutivo de Qiagen. “Nuestro estuche therascreen EGFR, aprobado por la FDA en base a amplia información analítica y clínica, es la prueba más completa y ofrece características únicas como la detección de mutaciones puntuales en tubos separados. Qiagen es un socio de preferencia en medicina personalizada debido a la capacidad de ofrecer resultados reproducibles, plataformas de flujo de trabajo eficiente y antecedentes en desarrollos y autorizaciones regulatorias.”
La plataforma Rotor-Gene Q MDx, adoptada por la mayoría de los principales laboratorios estadounidenses y muchos laboratorios en el mundo, procesa un menú cada vez mayor de pruebas moleculares. La plataforma Rotor-Gene Q MDx está aprobada en los EUA para el uso del estuche de prueba therascreen KRAS RGQ PCR de Qiagen en pacientes con cáncer colorrectal y la prueba therascreen EGFR en pacientes con NSCLC metastásico, productos importantes de la medicina personalizada.
Qiagen continúa con la expansión de su cartera de tecnologías de medicina personalizada y pretende solicitar la aprobación regulatoria de mayor cantidad de pruebas en el mundo compatibles con la plataforma Rotor-Gene Q MDx. La empresa tiene más de 15 proyectos de desarrollo y comercialización de pruebas diagnósticas con fines terapéuticos en conjunto con empresas farmacéuticas y biotecnológicas como Amgen, AstraZeneca, Bayer, Bristol-Myers Squibb, Eli Lilly and Company y Pfizer. Qiagen está desarrollando numerosas pruebas diagnósticas con fines terapéuticos, además de una línea de pruebas moleculares, como parte de un amplio menú de pruebas confiables y rentables de diagnóstico molecular.
Clovis Oncology es una empresa biofarmacéutica centrada en la adquisición, desarrollo y comercialización de tratamientos oncológicos en los Estados Unidos, Europa y otros mercados internacionales.
Enlaces relacionados:
Qiagen
Clovis Oncology
Últimas Industria noticias
- Cepheid y Oxford Nanopore se unen para desarrollar soluciones con secuenciación automatizada
- Grifols e IBL de Tecan colaboran en paneles de biomarcadores avanzados
- Nueva colaboración avanza en identificación microbiana para diagnóstico de enfermedades infecciosas
- Tecan adquiere activos de inmunoensayo ELISA de Cisbio Bioassays de Revvity
- Leica Biosystems y Bio-Techne amplían su colaboración multiómica espacial
- Philips e Ibex amplían colaboración para mejorar flujos de trabajo de patología basados en IA
- Grifols e Inpeco se asocian para crear el "laboratorio del futuro" de medicina transfusional
- Investigación impulsa imágenes ópticas en tiempo real mejoradas con IA en biopsias de cáncer de pulmón
- CACLP 2025 reúne innovadores globales de industria del IVD
- Bio-Rad adquirirá Stilla Technologies, desarrollador de PCR digital
- ABL firma acuerdo de licencia y transferencia de know-how para cartera de Fast Track Diagnostics de Siemens
- Becton Dickinson escindirá su negocio de biociencias y soluciones de diagnóstico
- Nueva colaboración revoluciona los análisis de muestras biológicas
- Medlab Middle East mira hacia el futuro de los laboratorios
- Medix Biochemica adquiere Candor Bioscience, desarrollador de soluciones de inmunoensayo
- bioMérieux adquiere SpinChip Diagnostics empresa noruega especializada en inmunoensayos
Canales
Química Clínica
ver canal
Herramienta química a nanoescala 'brillantemente luminosa' mejora detección de enfermedades
Miles de moléculas brillantes disponibles comercialmente, conocidas como fluoróforos, se utilizan comúnmente en imágenes médicas, detección de enfermedades, marcado... Más
Prueba de detección portátil económica transforma detección de enfermedades renales
Millones de personas padecen enfermedad renal, que a menudo permanece sin diagnosticar hasta que alcanza una etapa crítica. Esta epidemia silenciosa no solo disminuye la calidad de vida de los afectados,... MásDiagnóstico Molecular
ver canal
Prueba de biomarcadores sanguíneos podría detectar predisposición genética al Alzheimer
Nuevos medicamentos para la enfermedad de Alzheimer, la forma más común de demencia, están ahora disponibles. Estos tratamientos, conocidos como "anticuerpos amiloides",... Más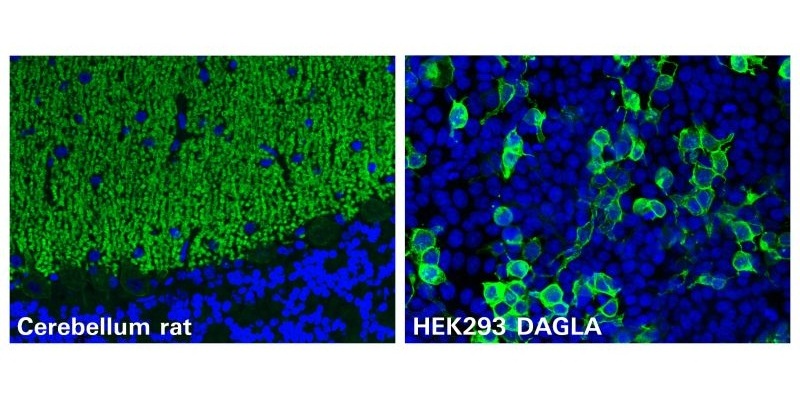
Se descubre nuevo autoanticuerpo contra DAGLA en cerebelitis
Las ataxias cerebelosas autoinmunes son trastornos muy incapacitantes que se caracterizan por una disminución de la habilidad para coordinar el movimiento muscular. Los autoanticuerpos cerebelosos... MásHematología
ver canal
Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
La citopenia clonal de significado incierto (CCSI) es un trastorno sanguíneo común en adultos mayores, caracterizado por mutaciones en las células sanguíneas y un recuento ... Más
Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
En los Estados Unidos, aproximadamente el 15 % de las embarazadas son RhD negativas. Sin embargo, en aproximadamente el 40 % de estos casos, el feto también es RhD negativo, lo que hace innecesaria la... MásInmunología
ver canal
Prueba de células madre predice resultado del tratamiento en cáncer de ovario resistente al platino
El cáncer de ovario epitelial suele responder inicialmente a la quimioterapia, pero con el tiempo, el tumor desarrolla resistencia a la terapia, lo que provoca su recrecimiento. Esta resistencia... Más
Análisis de sangre con aprendizaje automático predice respuesta a inmunoterapia en pacientes con linfoma
La terapia de células T con receptores de antígenos quiméricos (CAR) se ha convertido en uno de los avances recientes más prometedores en el tratamiento de los cánceres... MásMicrobiología
ver canal
Dispositivo portátil ofrece resultados de tuberculosis económico y rápido
La tuberculosis (TB) sigue siendo la enfermedad infecciosa más mortal a nivel mundial, afectando a aproximadamente 10 millones de personas al año. En 2021, alrededor de 4,2 millones de casos... Más
Método basado en IA mejora diagnóstico de infecciones resistentes a fármacos
Las infecciones resistentes a los medicamentos, en particular las causadas por bacterias mortales como la tuberculosis y el estafilococo, se están convirtiendo rápidamente en una emergencia... MásPatología
ver canal
Nuevo método basado en aprendizaje automático detecta contaminación microbiana en cultivos celulares
La terapia celular tiene un gran potencial en el tratamiento de enfermedades como el cáncer, las enfermedades inflamatorias y los trastornos degenerativos crónicos mediante la manipulación o el reemplazo... Más
Nuevo método con corrección de errores detecta cáncer únicamente en muestras de sangre
La tecnología de biopsia líquida, que se basa en análisis de sangre para la detección temprana del cáncer y el seguimiento de la carga oncológica en los pacientes,... MásTecnología
ver canal
Tecnología de microchip desechable podría detectar selectivamente VIH en muestras de sangre completa
A finales de 2023, aproximadamente 40 millones de personas en todo el mundo vivían con VIH, y alrededor de 630.000 personas murieron por enfermedades relacionadas con el sida ese mismo año.... Más






.jpg)