Asocian los niveles séricos de amiloide A con la probabilidad de desarrollar COVID-19 severa
|
Por el equipo editorial de LabMedica en español Actualizado el 08 Jun 2021 |
![Imagen: Esta ilustración revela la morfología ultraestructural exhibida por el coronavirus que causa COVID-19. Note los picos que adornan la superficie exterior del virus, que imparten el aspecto de una corona que rodea al virión (Fotografía cortesía de los Centros para el Control y la Prevención de Enfermedades [EUA]) Imagen: Esta ilustración revela la morfología ultraestructural exhibida por el coronavirus que causa COVID-19. Note los picos que adornan la superficie exterior del virus, que imparten el aspecto de una corona que rodea al virión (Fotografía cortesía de los Centros para el Control y la Prevención de Enfermedades [EUA])](https://globetechcdn.com/mobile_es_labmedica/images/stories/articles/article_images/2021-06-08/GMS-030B.jpg)
Imagen: Esta ilustración revela la morfología ultraestructural exhibida por el coronavirus que causa COVID-19. Note los picos que adornan la superficie exterior del virus, que imparten el aspecto de una corona que rodea al virión (Fotografía cortesía de los Centros para el Control y la Prevención de Enfermedades [EUA])
Los resultados de los trabajos de investigación publicados durante la pandemia actual sugieren que el aumento de los niveles del biomarcador sanguíneo amiloide A en suero predice el desarrollo de formas graves o fatales de COVID-19.
Las proteínas amiloide séricas A (SAA) son una familia de apolipoproteínas asociadas con lipoproteínas de alta densidad (HDL) en el plasma. Las proteínas amiloides A séricas de fase aguda (A-SAA) se secretan durante la fase aguda de la inflamación. Los genes y proteínas A-SAA se activan significativamente durante la respuesta de fase aguda, que comprende una serie de fenómenos que ocurren en presencia de inflamación e infección, por ejemplo, aumento de la temperatura y alteraciones hormonales y metabólicas.
Las concentraciones circulantes de SAA, normalmente bajas en circunstancias fisiológicas, pueden aumentar hasta 1000 veces en las primeras 24 a 48 horas de una respuesta de fase aguda. Esta es la consecuencia de una mayor síntesis en el hígado que se desencadena por varios estímulos, incluido el factor de necrosis tumoral (TNF), la interleuquina (IL)-1beta, la IL-6 y el interferón gamma (IFN-gamma). El SAA, a su vez, puede activar el sistema del complemento y aumentar aún más la síntesis de TNF, IL-1beta e IL-6, y activar otras citoquinas proinflamatorias como IL-1 alfa e IL-23.
Dos revisiones sistemáticas y metanálisis de un número relativamente limitado de estudios informaron una asociación significativa y positiva entre las concentraciones de SAA y la gravedad de la COVID-19. Por lo tanto, era plausible que el aumento agudo de las concentraciones de SAA en pacientes con COVID-19 no solo reflejara la presencia de una respuesta de fase aguda, sino que también presagiara el desarrollo de una tormenta de citoquinas y, en consecuencia, una falla multiorgánica y un aumento en el riesgo de resultados adversos.
A la luz de esto, los investigadores de la Universidad Flinders (Adelaida, Australia) y la Universidad de Sassari (Italia) analizaron los resultados de diecinueve estudios publicados que involucraron a 5.617 pacientes con COVID-19 para determinar si se podía demostrar un vínculo entre los niveles de SAA y la COVID-19.
Los investigadores informaron que los resultados combinados indicaron que las concentraciones de SAA eran significativamente más altas en pacientes con enfermedad grave y no supervivientes que en pacientes con enfermedad leve o controles. Las concentraciones de SAA se asociaron significativa y positivamente con una mayor gravedad y mortalidad de la COVID-19.
“Nuestros análisis mostraron que los pacientes con COVID-19 con enfermedad grave o que finalmente murieron tenían niveles significativamente más altos de SAA en comparación con los pacientes con COVID-19 leve”, dijo el autor principal, el Dr. Arduino Mangon, profesor de farmacología clínica en la Universidad de Flinders. “Los pacientes con formas graves de enfermedad por coronavirus 2019 tienen una inflamación excesiva, alteraciones en la formación de coágulos y daño significativo en varios órganos, particularmente el pulmón, el riñón, el corazón y el hígado. Esta sustancia química [SAA] puede ayudar, junto con otras características del paciente, a predecir qué pacientes con COVID-19 tienen probabilidad de deterioro y requieran un tratamiento agresivo”.
El estudio del amiloide A sérico se publicó en la edición en línea del 15 de marzo de 2021 de la revista Journal of Infectious Diseases.
Enlace relacionado:
Universidad Flinders
Universidad de Sassari
Las proteínas amiloide séricas A (SAA) son una familia de apolipoproteínas asociadas con lipoproteínas de alta densidad (HDL) en el plasma. Las proteínas amiloides A séricas de fase aguda (A-SAA) se secretan durante la fase aguda de la inflamación. Los genes y proteínas A-SAA se activan significativamente durante la respuesta de fase aguda, que comprende una serie de fenómenos que ocurren en presencia de inflamación e infección, por ejemplo, aumento de la temperatura y alteraciones hormonales y metabólicas.
Las concentraciones circulantes de SAA, normalmente bajas en circunstancias fisiológicas, pueden aumentar hasta 1000 veces en las primeras 24 a 48 horas de una respuesta de fase aguda. Esta es la consecuencia de una mayor síntesis en el hígado que se desencadena por varios estímulos, incluido el factor de necrosis tumoral (TNF), la interleuquina (IL)-1beta, la IL-6 y el interferón gamma (IFN-gamma). El SAA, a su vez, puede activar el sistema del complemento y aumentar aún más la síntesis de TNF, IL-1beta e IL-6, y activar otras citoquinas proinflamatorias como IL-1 alfa e IL-23.
Dos revisiones sistemáticas y metanálisis de un número relativamente limitado de estudios informaron una asociación significativa y positiva entre las concentraciones de SAA y la gravedad de la COVID-19. Por lo tanto, era plausible que el aumento agudo de las concentraciones de SAA en pacientes con COVID-19 no solo reflejara la presencia de una respuesta de fase aguda, sino que también presagiara el desarrollo de una tormenta de citoquinas y, en consecuencia, una falla multiorgánica y un aumento en el riesgo de resultados adversos.
A la luz de esto, los investigadores de la Universidad Flinders (Adelaida, Australia) y la Universidad de Sassari (Italia) analizaron los resultados de diecinueve estudios publicados que involucraron a 5.617 pacientes con COVID-19 para determinar si se podía demostrar un vínculo entre los niveles de SAA y la COVID-19.
Los investigadores informaron que los resultados combinados indicaron que las concentraciones de SAA eran significativamente más altas en pacientes con enfermedad grave y no supervivientes que en pacientes con enfermedad leve o controles. Las concentraciones de SAA se asociaron significativa y positivamente con una mayor gravedad y mortalidad de la COVID-19.
“Nuestros análisis mostraron que los pacientes con COVID-19 con enfermedad grave o que finalmente murieron tenían niveles significativamente más altos de SAA en comparación con los pacientes con COVID-19 leve”, dijo el autor principal, el Dr. Arduino Mangon, profesor de farmacología clínica en la Universidad de Flinders. “Los pacientes con formas graves de enfermedad por coronavirus 2019 tienen una inflamación excesiva, alteraciones en la formación de coágulos y daño significativo en varios órganos, particularmente el pulmón, el riñón, el corazón y el hígado. Esta sustancia química [SAA] puede ayudar, junto con otras características del paciente, a predecir qué pacientes con COVID-19 tienen probabilidad de deterioro y requieran un tratamiento agresivo”.
El estudio del amiloide A sérico se publicó en la edición en línea del 15 de marzo de 2021 de la revista Journal of Infectious Diseases.
Enlace relacionado:
Universidad Flinders
Universidad de Sassari
Últimas Diagnóstico Molecular noticias
- Enfoque revolucionario de análisis de células T permite detección temprana del cáncer
- Prueba genética única podría acelerar el diagnóstico de trastornos raros del desarrollo
- Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
- Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
- Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
- Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
- Prueba de biomarcadores líquidos detecta enfermedades neurodegenerativas antes de que aparezcan síntomas
- Nuevo método genómico ayuda a diagnosticar pacientes con enfermedad renal inexplicable
- Nuevo hidrogel inteligente allana el camino para nueva "piruleta" para diagnóstico de cáncer de boca
- Prueba de biomarcadores podría mejorar diagnóstico del cáncer de endometrio
- Prueba de ADN en heces de próxima generación supera a PIF en detección del cáncer colorrectal
- Innovador análisis de sangre de pTau217 es tan preciso como imágenes cerebrales o pruebas del LCR para diagnosticar Alzheimer
- Sistema de RT-PCR en el punto de atención de 10 minutos detecta hasta 32 objetivos por muestra
- Células extraídas de orina podrían permitir detección más temprana de enfermedad renal
- Análisis de sangre identifica a personas con mayor riesgo de morir por insuficiencia cardíaca
- Análisis de sangre muestra precisión del 83 % para detectar cáncer colorrectal
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal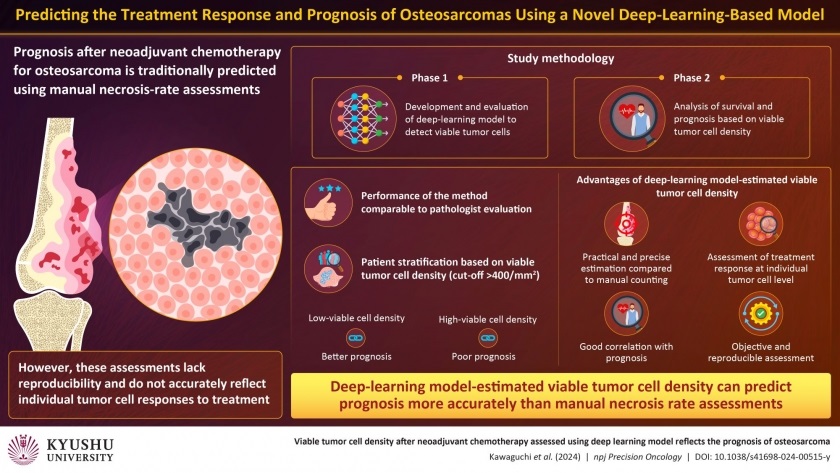
Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico... Más
Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
La comunidad médica mundial reconoce cada vez más que la biopsia líquida es un enfoque transformador para mejorar la atención al paciente con cáncer. Este innovador método de diagnóstico implica detectar... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)

.jpg)