Análisis rápido CRISPR/Cas para el diagnóstico de fiebres virales en ambientes de baja tecnología
|
Por el equipo editorial de LabMedica en español Actualizado el 07 Sep 2020 |
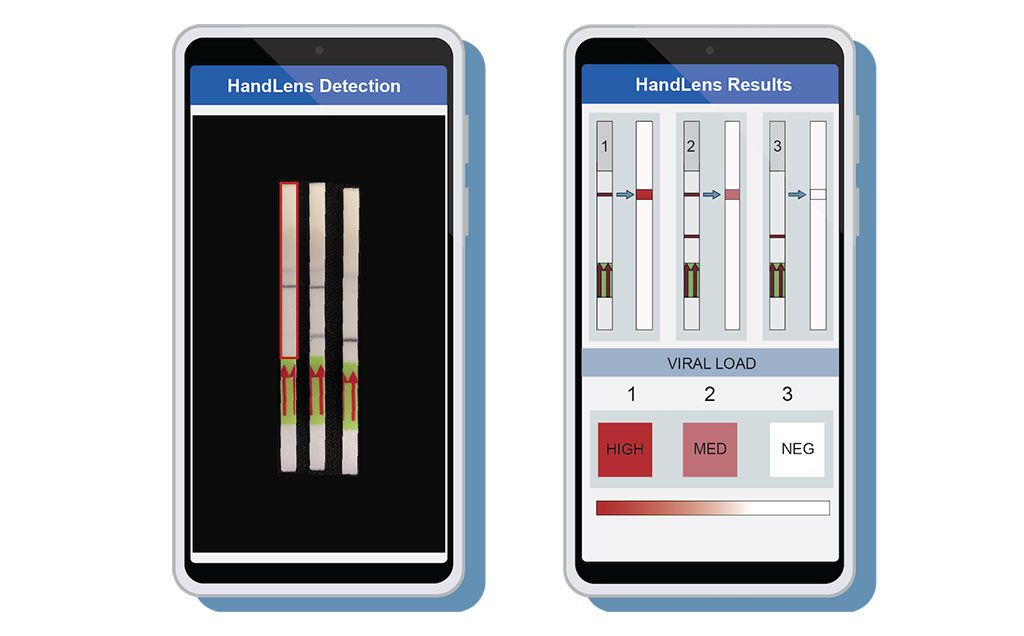
Imagen: Se diseñó una aplicación para teléfonos móviles llamada HandLens para leer e informar los resultados en las tiras de papel SHERLOCK (Fotografía cortesía de Anna Lachenauer, Facultad de Medicina de la Universidad de Stanford)
Las pruebas de diagnóstico rápido para los virus de la fiebre del Ébola y Lassa, basadas en el complejo CRISPR/Cas13a, dirigidas a la detección del ARN, se han probado con éxito en condiciones de campo en varios países africanos.
COVID-19 no es la única enfermedad que existe. Los recientes brotes de fiebres hemorrágicas virales (VHF), incluida la enfermedad por el virus del Ébola (EVE) y la fiebre de Lassa (LF), ponen de relieve la necesidad urgente de realizar pruebas sensibles y desplegables para diagnosticar estas devastadoras enfermedades humanas. En este sentido, los investigadores del Instituto Broad de MIT y Harvard (Cambridge, MA, EUA) y sus colaboradores, desarrollaron diagnósticos basados en CRISPR-Cas13a, dirigidos al virus del Ébola (EBOV) y al virus Lassa (LASV), con lecturas de flujo lateral y fluorescentes.
Los CRISPR (repeticiones palindrómicas cortas agrupadas regularmente interespaciadas) son segmentos de ADN procariótico que contienen repeticiones cortas de secuencias de bases. A cada repetición le siguen segmentos cortos de “ADN espaciador” de exposiciones anteriores a un virus bacteriano o plásmido. Desde 2013, se ha utilizado el sistema CRISPR/Cas9 en la investigación para la edición de genes (agregar, interrumpir o cambiar la secuencia de genes específicos) y la regulación de genes. Al administrar la enzima Cas9 y los ARN guía apropiados (ARNsg) a una célula, el genoma del organismo se puede cortar en cualquier ubicación deseada.
Los recientes esfuerzos computacionales para identificar nuevos sistemas CRISPR descubrieron un nuevo tipo de enzima dirigida al ARN, Cas13. La diversa familia Cas13 contiene al menos cuatro subtipos conocidos, incluidos Cas13a (anteriormente C2c2), Cas13b, Cas13c y Cas13d. Se demostró que Cas13a se une y escinde el ARN, protegiendo a las bacterias de los fagos de ARN y sirviendo como una plataforma poderosa para la manipulación del ARN. Se sugirió que Cas13a podría funcionar como parte de un sistema CRISPR/Cas versátil, guiado por ARN, dirigido a la detección del ARN, que tiene un gran potencial para aplicaciones precisas, robustas y escalables, guiadas por ARN dirigidas a la detección de ARN.
En el desarrollo de un método para diagnósticos desplegables y rápidamente adaptables, los investigadores trabajaron con la plataforma SHERLOCK (siglas en inglés para Desbloqueo de Reportero Enzimático Específico de Alta Sensibilidad), basada en CRISPR. SHERLOCK utiliza la proteína Cas13a dirigida al ARN para la detección sensible y específica del ácido nucleico viral. Este método funciona amplificando secuencias genéticas y programando una molécula CRISPR para detectar la presencia de una firma genética específica en una muestra, que también puede ser cuantificada. Cuando encuentra esas firmas, la enzima CRISPR se activa y libera una señal robusta. Esta señal se puede adaptar para trabajar en una simple tira de papel, en un equipo de laboratorio o para proporcionar una lectura electroquímica que se puede leer con un teléfono móvil.
SHERLOCK se puede combinar con el método HUDSON (Calentamiento de Muestras de Diagnóstico no Extraídas para Eliminar Nucleasas), que inactiva patógenos y libera ácido nucleico mediante una desnaturalización química y térmica combinada, eliminando la necesidad de una extracción de ácidos nucleicos basada en columna o en perlas. Este proceso hace que las muestras de los pacientes sean más seguras para que el personal clínico las manipule en entornos de baja tecnología y elimina la necesidad de extraer el material genético de un virus de las muestras, antes del análisis.
Para completar el paquete, los investigadores también desarrollaron una aplicación para teléfonos móviles llamada HandLens, que puede leer e informar inmediatamente los resultados de las tiras de papel SHERLOCK. Esta herramienta puede ayudar en situaciones en las que la tira de papel emite una señal débil que es difícil de interpretar para un médico.
Los investigadores utilizaron la técnica SHERLOCK junto con HUDSON y HandLens en Nigeria durante un reciente brote de fiebre de Lassa y en Sierra Leona y la República Democrática del Congo durante los brotes del virus del Ébola. Los resultados revelaron que los ensayos SHERLOCK funcionaron de manera tan consistente o mejor que otras metodologías de diagnóstico, lo que demuestra el potencial de la plataforma para el uso clínico en áreas con recursos limitados.
La técnica SHERLOCK para el diagnóstico rápido de enfermedades virales se describió en la edición en línea del 17 de agosto de 2020 de la revista Nature Communications.
Enlace relacionado:
Instituto Broad de MIT y Harvard
COVID-19 no es la única enfermedad que existe. Los recientes brotes de fiebres hemorrágicas virales (VHF), incluida la enfermedad por el virus del Ébola (EVE) y la fiebre de Lassa (LF), ponen de relieve la necesidad urgente de realizar pruebas sensibles y desplegables para diagnosticar estas devastadoras enfermedades humanas. En este sentido, los investigadores del Instituto Broad de MIT y Harvard (Cambridge, MA, EUA) y sus colaboradores, desarrollaron diagnósticos basados en CRISPR-Cas13a, dirigidos al virus del Ébola (EBOV) y al virus Lassa (LASV), con lecturas de flujo lateral y fluorescentes.
Los CRISPR (repeticiones palindrómicas cortas agrupadas regularmente interespaciadas) son segmentos de ADN procariótico que contienen repeticiones cortas de secuencias de bases. A cada repetición le siguen segmentos cortos de “ADN espaciador” de exposiciones anteriores a un virus bacteriano o plásmido. Desde 2013, se ha utilizado el sistema CRISPR/Cas9 en la investigación para la edición de genes (agregar, interrumpir o cambiar la secuencia de genes específicos) y la regulación de genes. Al administrar la enzima Cas9 y los ARN guía apropiados (ARNsg) a una célula, el genoma del organismo se puede cortar en cualquier ubicación deseada.
Los recientes esfuerzos computacionales para identificar nuevos sistemas CRISPR descubrieron un nuevo tipo de enzima dirigida al ARN, Cas13. La diversa familia Cas13 contiene al menos cuatro subtipos conocidos, incluidos Cas13a (anteriormente C2c2), Cas13b, Cas13c y Cas13d. Se demostró que Cas13a se une y escinde el ARN, protegiendo a las bacterias de los fagos de ARN y sirviendo como una plataforma poderosa para la manipulación del ARN. Se sugirió que Cas13a podría funcionar como parte de un sistema CRISPR/Cas versátil, guiado por ARN, dirigido a la detección del ARN, que tiene un gran potencial para aplicaciones precisas, robustas y escalables, guiadas por ARN dirigidas a la detección de ARN.
En el desarrollo de un método para diagnósticos desplegables y rápidamente adaptables, los investigadores trabajaron con la plataforma SHERLOCK (siglas en inglés para Desbloqueo de Reportero Enzimático Específico de Alta Sensibilidad), basada en CRISPR. SHERLOCK utiliza la proteína Cas13a dirigida al ARN para la detección sensible y específica del ácido nucleico viral. Este método funciona amplificando secuencias genéticas y programando una molécula CRISPR para detectar la presencia de una firma genética específica en una muestra, que también puede ser cuantificada. Cuando encuentra esas firmas, la enzima CRISPR se activa y libera una señal robusta. Esta señal se puede adaptar para trabajar en una simple tira de papel, en un equipo de laboratorio o para proporcionar una lectura electroquímica que se puede leer con un teléfono móvil.
SHERLOCK se puede combinar con el método HUDSON (Calentamiento de Muestras de Diagnóstico no Extraídas para Eliminar Nucleasas), que inactiva patógenos y libera ácido nucleico mediante una desnaturalización química y térmica combinada, eliminando la necesidad de una extracción de ácidos nucleicos basada en columna o en perlas. Este proceso hace que las muestras de los pacientes sean más seguras para que el personal clínico las manipule en entornos de baja tecnología y elimina la necesidad de extraer el material genético de un virus de las muestras, antes del análisis.
Para completar el paquete, los investigadores también desarrollaron una aplicación para teléfonos móviles llamada HandLens, que puede leer e informar inmediatamente los resultados de las tiras de papel SHERLOCK. Esta herramienta puede ayudar en situaciones en las que la tira de papel emite una señal débil que es difícil de interpretar para un médico.
Los investigadores utilizaron la técnica SHERLOCK junto con HUDSON y HandLens en Nigeria durante un reciente brote de fiebre de Lassa y en Sierra Leona y la República Democrática del Congo durante los brotes del virus del Ébola. Los resultados revelaron que los ensayos SHERLOCK funcionaron de manera tan consistente o mejor que otras metodologías de diagnóstico, lo que demuestra el potencial de la plataforma para el uso clínico en áreas con recursos limitados.
La técnica SHERLOCK para el diagnóstico rápido de enfermedades virales se describió en la edición en línea del 17 de agosto de 2020 de la revista Nature Communications.
Enlace relacionado:
Instituto Broad de MIT y Harvard
Últimas Microbiología noticias
- Análisis de sangre predice sepsis e insuficiencia orgánica en niños
- Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
- Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
- Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
- Nuevo análisis para tuberculosis podría ampliar acceso a pruebas en países de ingresos bajos y medios
- Prueba rápida diagnostica enfermedades tropicales en horas para tratamiento con antibióticos más rápido
- Pruebas moleculares rápidas permiten tratamiento antibiótico más rápido y específico para neumonía
- Plataforma rápida de PSA proporciona resultados terapéuticos específicos días antes que el estándar de atención actual
- Nuevo método de análisis detecta patógenos en sangre de forma más rápida y precisa al fundir ADN
- Prueba rápida de sepsis ofrece resultados dos días más rápidos
- Diagnóstico rápido portátil por PCR podría detectar gonorrea y susceptibilidad a antibióticos
- Prueba CRISPR diagnostica mpox más rápido que método de PCR de laboratorio
- Prueba de PCR multiplexada para detección de patógenos y resistencia a antibióticos ayuda a brindar un tratamiento rápido de ITU
- Nuevo algoritmo detecta e identifica nuevos organismos bacterianos
- Analizador de mesa promete detección de ITU en 1 hora e indicación de sensibilidad a antibióticos
- Prueba rápida junto a la cama podría proteger a recién nacidos de enfermedades potencialmente mortales
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... Más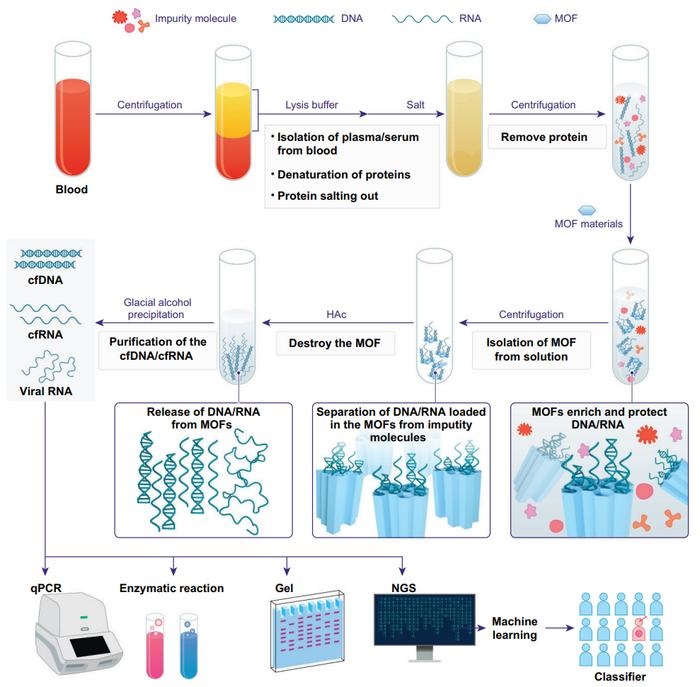
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásPatología
ver canal
Innovador dispositivo de extracción de sangre supera obstáculos comunes relacionados con la flebotomía
La incomodidad asociada con las extracciones de sangre tradicionales genera un problema importante: aproximadamente el 30 % de las pruebas de diagnóstico prescritas por los médicos nunca... Más
Dispositivo POC intraoperatorio distingue entre quistes ováricos benignos y malignos en 15 minutos
Los quistes ováricos representan un problema de salud importante para las mujeres en todo el mundo, y hasta el 10 % experimenta esta afección en algún momento de sus vidas.... Más
Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
La enfermedad de Parkinson y un grupo de trastornos neurodegenerativos relacionados conocidos como sinucleinopatías afectan a millones de personas en todo el mundo. Estas afecciones, incluida la... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más











.jpg)

.jpg)
.jpg)