Helicobacter pylori desencadena el desarrollo de enfermedades estomacales
|
Por el equipo editorial de LabMedica en español Actualizado el 27 Jan 2020 |
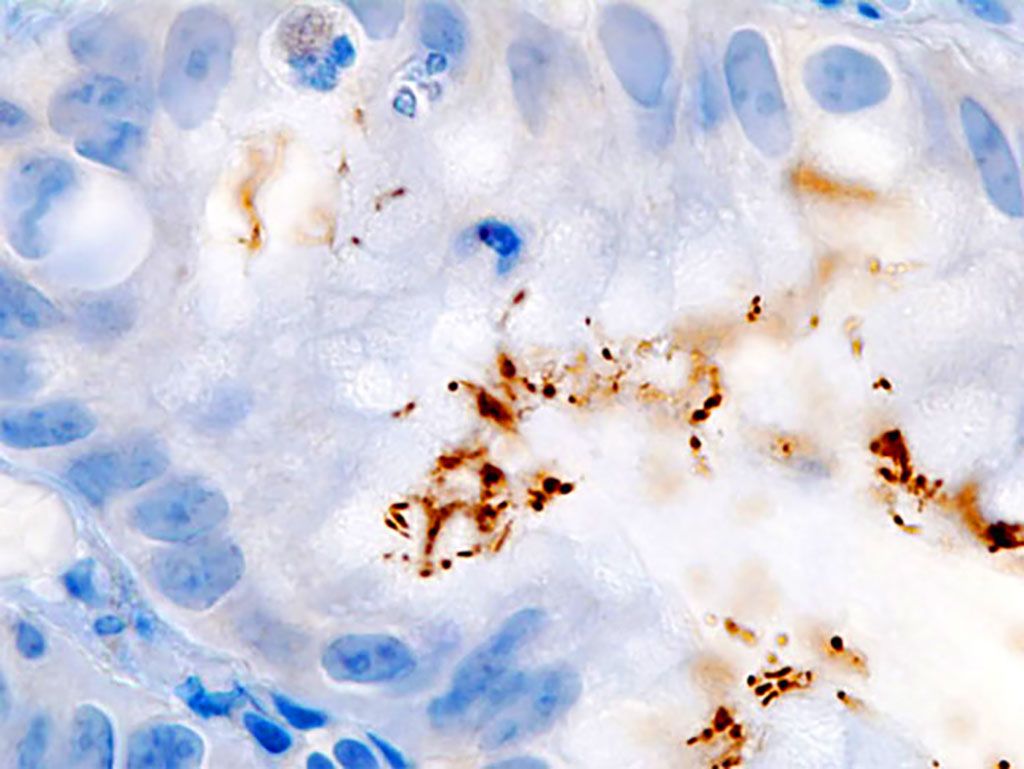
Imagen: Inmunocoloración de la infección por Helicobacter pylori en un hoyo foveolar gástrico demostrado en una biopsia gástrica endoscópica (Fotografía cortesía de KGH).
Helicobacter pylori es un patógeno paradigma persistente que coloniza aproximadamente el 50% de la población mundial humana y representa un factor de riesgo importante para la gastritis crónica, las úlcera péptica y las neoplasias gástricas.
El receptor tipo-Toll TLR5, reconoce un dominio conservado, denominado D, que está presente en las flagelinas de varias bacterias patógenas, pero no en Helicobacter pylori. Las cepas de H. pylori altamente virulentas poseen un sistema de secreción de tipo IV (T4SS) para la administración de factores de virulencia a las células epiteliales gástricas.
Los microbiólogos de la Universidad Friedrich Alexander Erlangen-Nuremberg (Erlangen, Alemania) y sus colegas, investigaron cómo H. pylori manipula el sistema inmune del huésped para garantizar su supervivencia a largo plazo en el estómago. Una inflamación crónica es la causa más común de enfermedades estomacales. El equipo puede identificar un “interruptor molecular” que utiliza un mecanismo, previamente desconocido, para regular la reacción de inflamación en el estómago.
La interacción entre H. pylori y las células del estómago activa una estructura de pilus similar a una jeringa denominada sistema de secreción de tipo IV. En la superficie de esta estructura se presenta una proteína, CagL, que permite que la toxina bacteriana conocida como proteína CagA sea enviada a las células del estómago. La CagA inyectada luego reprograma la célula huésped para que se pueda desarrollar el cáncer de estómago. Sin embargo, ahora parece que CagL también tiene otra función importante. La proteína es reconocida por el sistema inmune a través del receptor TLR5. CagL imita un motivo de reconocimiento TLR5 en la proteína flagelina de otros patógenos, controlando así la respuesta inmune humana.
Curiosamente, esta vía de señalización se puede activar y desactivar mediante el sistema de secreción de tipo IV, que, se cree, no es el caso con otras bacterias. Presumiblemente, H. pylori ha explotado esta vía de señalización durante miles de años de evolución para eliminar competidores bacterianos “molestos” en el estómago. Al mismo tiempo, CagL influye en el sistema inmunitario congénito y adaptativo, así como en la reacción inflamatoria de tal manera que H. pylori en sí no se reconoce y, en consecuencia, no se puede eliminar, un mecanismo que es crucial para las infecciones a largo plazo con H. pylori en el estómago y que desencadena una enfermedad estomacal.
El equipo también observó que TLR5 ya no se produce en las células del estómago sano, una vez que se resuelve la infección. Esto indica que la expresión de esta proteína es un indicador nuevo de la enfermedad estomacal en humanos desencadenada por H. pylori. El estudio fue publicado el 16 de diciembre de 2019 en la revista Nature Communications.
Enlace relacionado:
Universidad Friedrich Alexander Erlangen-Nuremberg
El receptor tipo-Toll TLR5, reconoce un dominio conservado, denominado D, que está presente en las flagelinas de varias bacterias patógenas, pero no en Helicobacter pylori. Las cepas de H. pylori altamente virulentas poseen un sistema de secreción de tipo IV (T4SS) para la administración de factores de virulencia a las células epiteliales gástricas.
Los microbiólogos de la Universidad Friedrich Alexander Erlangen-Nuremberg (Erlangen, Alemania) y sus colegas, investigaron cómo H. pylori manipula el sistema inmune del huésped para garantizar su supervivencia a largo plazo en el estómago. Una inflamación crónica es la causa más común de enfermedades estomacales. El equipo puede identificar un “interruptor molecular” que utiliza un mecanismo, previamente desconocido, para regular la reacción de inflamación en el estómago.
La interacción entre H. pylori y las células del estómago activa una estructura de pilus similar a una jeringa denominada sistema de secreción de tipo IV. En la superficie de esta estructura se presenta una proteína, CagL, que permite que la toxina bacteriana conocida como proteína CagA sea enviada a las células del estómago. La CagA inyectada luego reprograma la célula huésped para que se pueda desarrollar el cáncer de estómago. Sin embargo, ahora parece que CagL también tiene otra función importante. La proteína es reconocida por el sistema inmune a través del receptor TLR5. CagL imita un motivo de reconocimiento TLR5 en la proteína flagelina de otros patógenos, controlando así la respuesta inmune humana.
Curiosamente, esta vía de señalización se puede activar y desactivar mediante el sistema de secreción de tipo IV, que, se cree, no es el caso con otras bacterias. Presumiblemente, H. pylori ha explotado esta vía de señalización durante miles de años de evolución para eliminar competidores bacterianos “molestos” en el estómago. Al mismo tiempo, CagL influye en el sistema inmunitario congénito y adaptativo, así como en la reacción inflamatoria de tal manera que H. pylori en sí no se reconoce y, en consecuencia, no se puede eliminar, un mecanismo que es crucial para las infecciones a largo plazo con H. pylori en el estómago y que desencadena una enfermedad estomacal.
El equipo también observó que TLR5 ya no se produce en las células del estómago sano, una vez que se resuelve la infección. Esto indica que la expresión de esta proteína es un indicador nuevo de la enfermedad estomacal en humanos desencadenada por H. pylori. El estudio fue publicado el 16 de diciembre de 2019 en la revista Nature Communications.
Enlace relacionado:
Universidad Friedrich Alexander Erlangen-Nuremberg
Últimas Microbiología noticias
- Análisis de sangre predice sepsis e insuficiencia orgánica en niños
- Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
- Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
- Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
- Nuevo análisis para tuberculosis podría ampliar acceso a pruebas en países de ingresos bajos y medios
- Prueba rápida diagnostica enfermedades tropicales en horas para tratamiento con antibióticos más rápido
- Pruebas moleculares rápidas permiten tratamiento antibiótico más rápido y específico para neumonía
- Plataforma rápida de PSA proporciona resultados terapéuticos específicos días antes que el estándar de atención actual
- Nuevo método de análisis detecta patógenos en sangre de forma más rápida y precisa al fundir ADN
- Prueba rápida de sepsis ofrece resultados dos días más rápidos
- Diagnóstico rápido portátil por PCR podría detectar gonorrea y susceptibilidad a antibióticos
- Prueba CRISPR diagnostica mpox más rápido que método de PCR de laboratorio
- Prueba de PCR multiplexada para detección de patógenos y resistencia a antibióticos ayuda a brindar un tratamiento rápido de ITU
- Nuevo algoritmo detecta e identifica nuevos organismos bacterianos
- Analizador de mesa promete detección de ITU en 1 hora e indicación de sensibilidad a antibióticos
- Prueba rápida junto a la cama podría proteger a recién nacidos de enfermedades potencialmente mortales
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... Más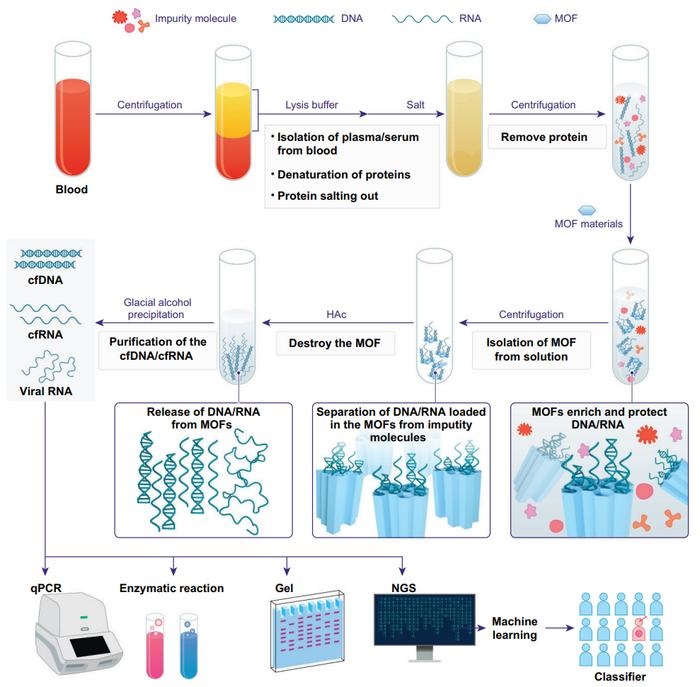
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásPatología
ver canal
Innovador dispositivo de extracción de sangre supera obstáculos comunes relacionados con la flebotomía
La incomodidad asociada con las extracciones de sangre tradicionales genera un problema importante: aproximadamente el 30 % de las pruebas de diagnóstico prescritas por los médicos nunca... Más
Dispositivo POC intraoperatorio distingue entre quistes ováricos benignos y malignos en 15 minutos
Los quistes ováricos representan un problema de salud importante para las mujeres en todo el mundo, y hasta el 10 % experimenta esta afección en algún momento de sus vidas.... Más
Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
La enfermedad de Parkinson y un grupo de trastornos neurodegenerativos relacionados conocidos como sinucleinopatías afectan a millones de personas en todo el mundo. Estas afecciones, incluida la... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)

.jpg)
.jpg)