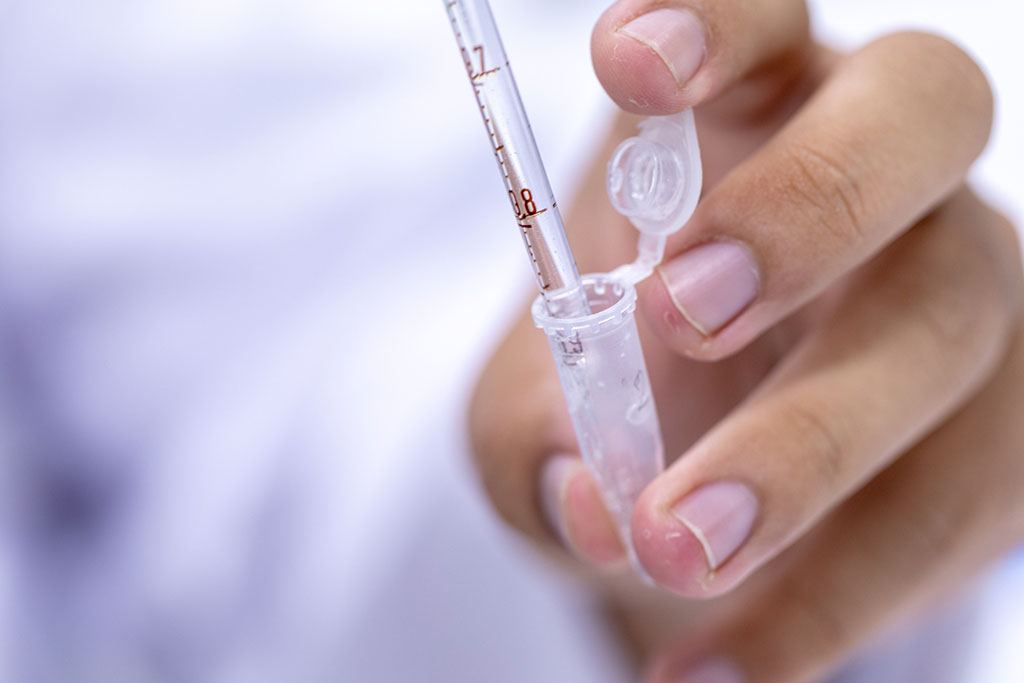
Aprueban análisis de sangre de próxima generación
|
Por el equipo editorial de LabMedica en español Actualizado el 24 Jul 2017 |

Imagen: La nueva prueba en sangre QuantiFERON-TB Gold Plus para la TB latente (Fotografía cortesía de QIAGEN).
La Agencia de Alimentos y Medicamentos de los Estados Unidos (FDA, por sus siglas en inglés), aprobó un ensayo de próxima generación para la infección latente por tuberculosis (TB), que combina el diseño de vanguardia para el análisis de CD4/CD8, para la detección de la respuesta inmune con un flujo de trabajo flexible de recolección de sangre.
La prueba aprobada por la FDA, QuantiFERON-TB Gold Plus (QFT-Plus) es la prueba en sangre de cuarta generación de QIAGEN (Germantown, MD, EUA y Hilden, Alemania) para la detección de la infección latente por TB. La prueba QFT-Plus se basa en la prueba, QuantiFERON-TB Gold (QFT), la versión de tercera generación del análisis de liberación del interferón gamma (IGRA) de Qiagen La prueba QFT es un análisis bien ensayado, con un vasto cuerpo de evidencia clínica, que se usa como una herramienta rentable y eficiente para las pruebas de infección por TB. La disponibilidad en los EUA está planeada para comenzar a finales de este año (2017).
“Estamos complacidos por la oportuna aprobación de la FDA para la prueba QuantiFERON-TB Gold Plus y que ahora podemos traer una gama de beneficios clínicos y de flujo de trabajo muy atractivos para los clientes”, dijo Thierry Bernard, vicepresidente senior y responsable del Área de Negocios de Diagnóstico Molecular de QIAGEN, “La tuberculosis es una enfermedad global que tiene un impacto en los Estados Unidos, donde hasta 13 millones de personas están infectadas y cerca de 10.000 personas padecen actualmente una enfermedad activa”.
Con la adición de la tecnología patentada, CD8+, QFT-Plus representa un hito clave en el desarrollo de pruebas de diagnóstico para la infección latente por TB. Por primera vez, una prueba tiene el potencial de ofrecer la capacidad de capturar una imagen mucho más amplia de la respuesta inmune de un individuo a la infección de TB. Este avance tecnológico es fundamental para mejorar la comprensión de cómo el sistema inmunológico reacciona a la infección de tuberculosis y se espera que establezca un nuevo estándar para el manejo de la enfermedad en el futuro.
Entre las nuevas características de la prueba, QFT-Plus, está la flexibilidad del flujo de trabajo que permite una implementación aún más eficiente, especialmente en los programas de detección de TB a gran escala. Éstos incluyen una opción estándar para la recolección de la sangre de un solo tubo, que permite que las muestras de sangre sean procesadas hasta 53 horas después la venopunción sin afectar la exactitud de la prueba. Esto se suma al diseño existente, único de “ensayo en el tubo de recolección” que permite la estimulación inmediata de la muestra de sangre.
Otra nueva característica incluye avances para apoyar la investigación sobre la estratificación del riesgo de que las infecciones latentes por TB se convierten en una enfermedad activa, basada en la incorporación, por primera vez, de los datos de respuesta de las células T CD8+, que proporcionan información valiosa mediante la medición de un rango más amplio de respuesta inmune. La evidencia científica publicada pone de relieve el potencial futuro de las células T CD8 + para diferenciar la TB activa de la latente, detectar infecciones recientes o antiguas, detectar la TB en ciertas poblaciones de riesgo (como la coinfección por VIH y los niños pequeños) y para evaluar la respuesta de la tuberculosis al tratamiento.
La prueba QFT-Plus está programado para ser lanzada en los EUA en medio de nuevas recomendaciones que amplian el uso de las IGRA. En diciembre de 2016, un grupo de trabajo apoyado por la Sociedad Americana del Tórax (ATS), los Centros para el Control y la Prevención de Enfermedades (CDC por su sigla en inglés) y la Sociedad de Enfermedades Infecciosas de América, publicó nuevas guías basadas en evidencia que recomendaban el uso de pruebas IGRA en grupos más amplios de personas con riesgo de contraer la tuberculosis. Esto siguió a las recomendaciones del Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF, por su sigla en inglés) en septiembre de 2016, de que los médicos de atención primaria deben examinar a los pacientes adultos pertenecientes a los grupos con riesgo alto de infección latente por TB. Ambos se refirieron a la QFT como una IGRA aprobada por la FDA en ese momento, preferible en ciertos grupos de pacientes a la prueba cutánea centenaria de la tuberculina (TST).
Hasta la fecha, nueve publicaciones independientes, revisadas por pares, han apoyado el desempeño de la prueba QFT-Plus, y los estudios adicionales en curso en 22 países involucran a más de 30,000 pacientes. La QFT-Plus es la única prueba IGRA para la TB en curso a ser evaluada por la Organización Mundial de la Salud (OMS) como parte de su campaña mundial para erradicar la enfermedad.
La prueba aprobada por la FDA, QuantiFERON-TB Gold Plus (QFT-Plus) es la prueba en sangre de cuarta generación de QIAGEN (Germantown, MD, EUA y Hilden, Alemania) para la detección de la infección latente por TB. La prueba QFT-Plus se basa en la prueba, QuantiFERON-TB Gold (QFT), la versión de tercera generación del análisis de liberación del interferón gamma (IGRA) de Qiagen La prueba QFT es un análisis bien ensayado, con un vasto cuerpo de evidencia clínica, que se usa como una herramienta rentable y eficiente para las pruebas de infección por TB. La disponibilidad en los EUA está planeada para comenzar a finales de este año (2017).
“Estamos complacidos por la oportuna aprobación de la FDA para la prueba QuantiFERON-TB Gold Plus y que ahora podemos traer una gama de beneficios clínicos y de flujo de trabajo muy atractivos para los clientes”, dijo Thierry Bernard, vicepresidente senior y responsable del Área de Negocios de Diagnóstico Molecular de QIAGEN, “La tuberculosis es una enfermedad global que tiene un impacto en los Estados Unidos, donde hasta 13 millones de personas están infectadas y cerca de 10.000 personas padecen actualmente una enfermedad activa”.
Con la adición de la tecnología patentada, CD8+, QFT-Plus representa un hito clave en el desarrollo de pruebas de diagnóstico para la infección latente por TB. Por primera vez, una prueba tiene el potencial de ofrecer la capacidad de capturar una imagen mucho más amplia de la respuesta inmune de un individuo a la infección de TB. Este avance tecnológico es fundamental para mejorar la comprensión de cómo el sistema inmunológico reacciona a la infección de tuberculosis y se espera que establezca un nuevo estándar para el manejo de la enfermedad en el futuro.
Entre las nuevas características de la prueba, QFT-Plus, está la flexibilidad del flujo de trabajo que permite una implementación aún más eficiente, especialmente en los programas de detección de TB a gran escala. Éstos incluyen una opción estándar para la recolección de la sangre de un solo tubo, que permite que las muestras de sangre sean procesadas hasta 53 horas después la venopunción sin afectar la exactitud de la prueba. Esto se suma al diseño existente, único de “ensayo en el tubo de recolección” que permite la estimulación inmediata de la muestra de sangre.
Otra nueva característica incluye avances para apoyar la investigación sobre la estratificación del riesgo de que las infecciones latentes por TB se convierten en una enfermedad activa, basada en la incorporación, por primera vez, de los datos de respuesta de las células T CD8+, que proporcionan información valiosa mediante la medición de un rango más amplio de respuesta inmune. La evidencia científica publicada pone de relieve el potencial futuro de las células T CD8 + para diferenciar la TB activa de la latente, detectar infecciones recientes o antiguas, detectar la TB en ciertas poblaciones de riesgo (como la coinfección por VIH y los niños pequeños) y para evaluar la respuesta de la tuberculosis al tratamiento.
La prueba QFT-Plus está programado para ser lanzada en los EUA en medio de nuevas recomendaciones que amplian el uso de las IGRA. En diciembre de 2016, un grupo de trabajo apoyado por la Sociedad Americana del Tórax (ATS), los Centros para el Control y la Prevención de Enfermedades (CDC por su sigla en inglés) y la Sociedad de Enfermedades Infecciosas de América, publicó nuevas guías basadas en evidencia que recomendaban el uso de pruebas IGRA en grupos más amplios de personas con riesgo de contraer la tuberculosis. Esto siguió a las recomendaciones del Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF, por su sigla en inglés) en septiembre de 2016, de que los médicos de atención primaria deben examinar a los pacientes adultos pertenecientes a los grupos con riesgo alto de infección latente por TB. Ambos se refirieron a la QFT como una IGRA aprobada por la FDA en ese momento, preferible en ciertos grupos de pacientes a la prueba cutánea centenaria de la tuberculina (TST).
Hasta la fecha, nueve publicaciones independientes, revisadas por pares, han apoyado el desempeño de la prueba QFT-Plus, y los estudios adicionales en curso en 22 países involucran a más de 30,000 pacientes. La QFT-Plus es la única prueba IGRA para la TB en curso a ser evaluada por la Organización Mundial de la Salud (OMS) como parte de su campaña mundial para erradicar la enfermedad.
Últimas Microbiología noticias
- Análisis de sangre predice sepsis e insuficiencia orgánica en niños
- Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
- Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
- Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
- Nuevo análisis para tuberculosis podría ampliar acceso a pruebas en países de ingresos bajos y medios
- Prueba rápida diagnostica enfermedades tropicales en horas para tratamiento con antibióticos más rápido
- Pruebas moleculares rápidas permiten tratamiento antibiótico más rápido y específico para neumonía
- Plataforma rápida de PSA proporciona resultados terapéuticos específicos días antes que el estándar de atención actual
- Nuevo método de análisis detecta patógenos en sangre de forma más rápida y precisa al fundir ADN
- Prueba rápida de sepsis ofrece resultados dos días más rápidos
- Diagnóstico rápido portátil por PCR podría detectar gonorrea y susceptibilidad a antibióticos
- Prueba CRISPR diagnostica mpox más rápido que método de PCR de laboratorio
- Prueba de PCR multiplexada para detección de patógenos y resistencia a antibióticos ayuda a brindar un tratamiento rápido de ITU
- Nuevo algoritmo detecta e identifica nuevos organismos bacterianos
- Analizador de mesa promete detección de ITU en 1 hora e indicación de sensibilidad a antibióticos
- Prueba rápida junto a la cama podría proteger a recién nacidos de enfermedades potencialmente mortales
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal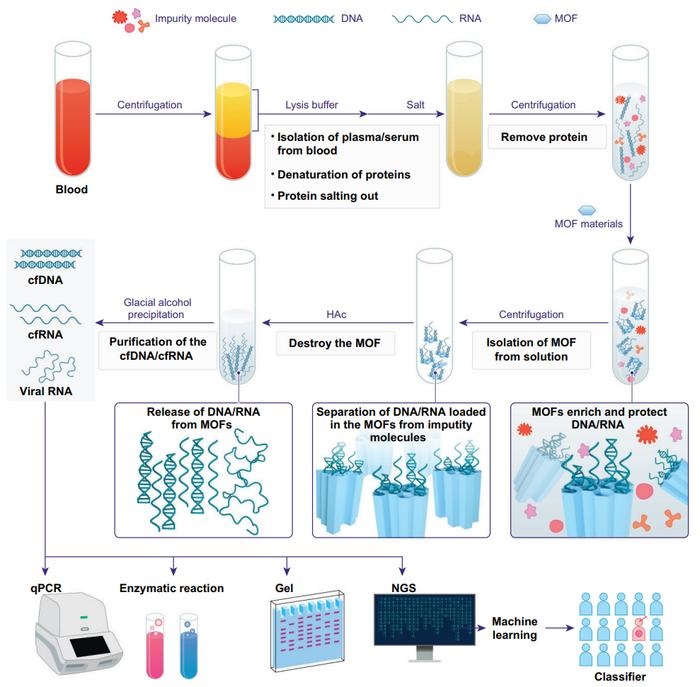
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más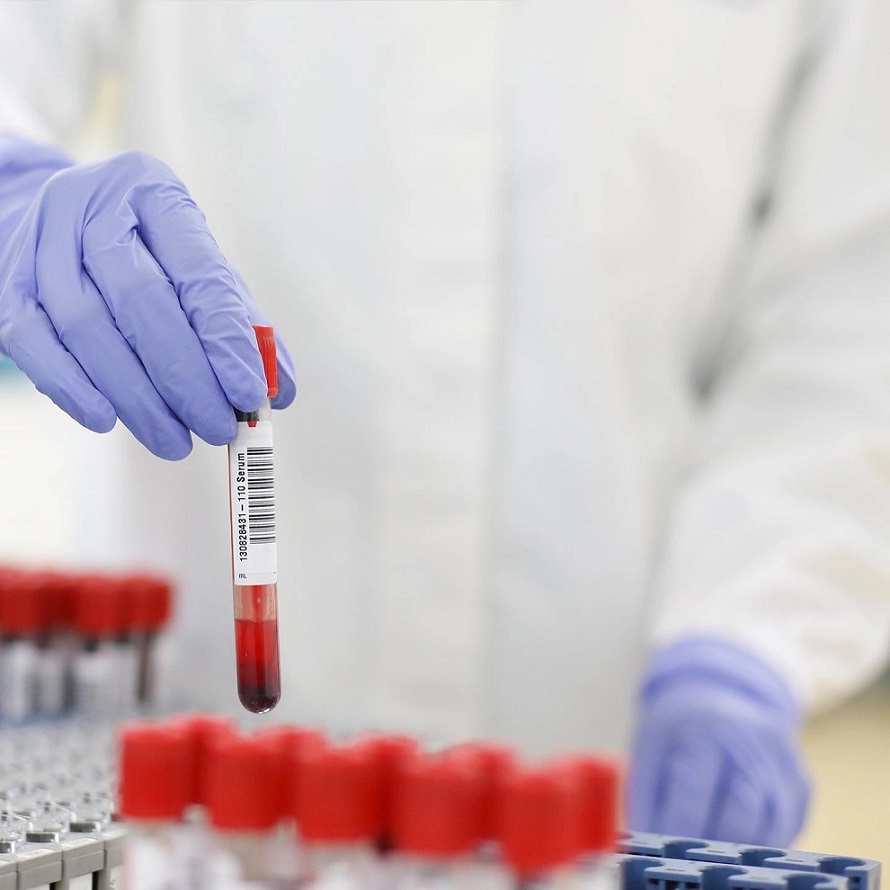
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásPatología
ver canal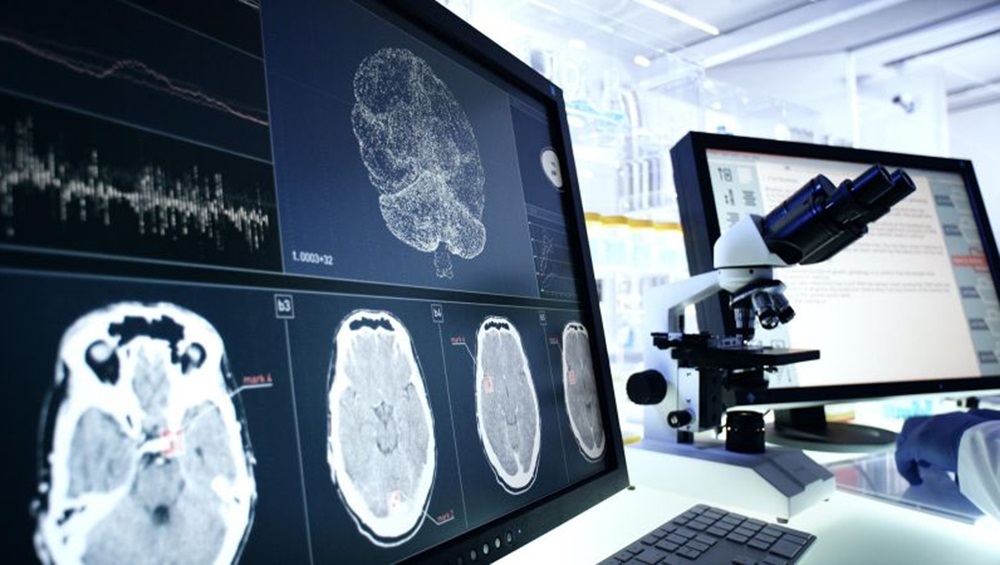
Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
La enfermedad de Parkinson y un grupo de trastornos neurodegenerativos relacionados conocidos como sinucleinopatías afectan a millones de personas en todo el mundo. Estas afecciones, incluida la... Más.jpg)
Herramienta bioinformática para identificar alteraciones cromosómicas en células tumorales puede mejorar diagnóstico del cáncer
La inestabilidad cromosómica es una característica común en los tumores sólidos y desempeña un papel crucial en el inicio, la progresión y la propagación... Más
Dispositivo del tamaño de una moneda aísla rápidamente plasma sanguíneo para diagnósticos clínicos más rápidos y precisos
La identificación de biomarcadores para diversos cánceres y enfermedades a menudo se basa en ADN, ARN y vesículas extracelulares libres de células. Tradicionalmente, separar... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más











.jpg)
.jpg)

.jpg)
.jpg)