Pruebas genéticas de la línea germinal después de la secuenciación tumoral descubre variantes susceptibles de tratamiento clínico
|
Por el equipo editorial de LabMedica en español Actualizado el 28 Oct 2020 |

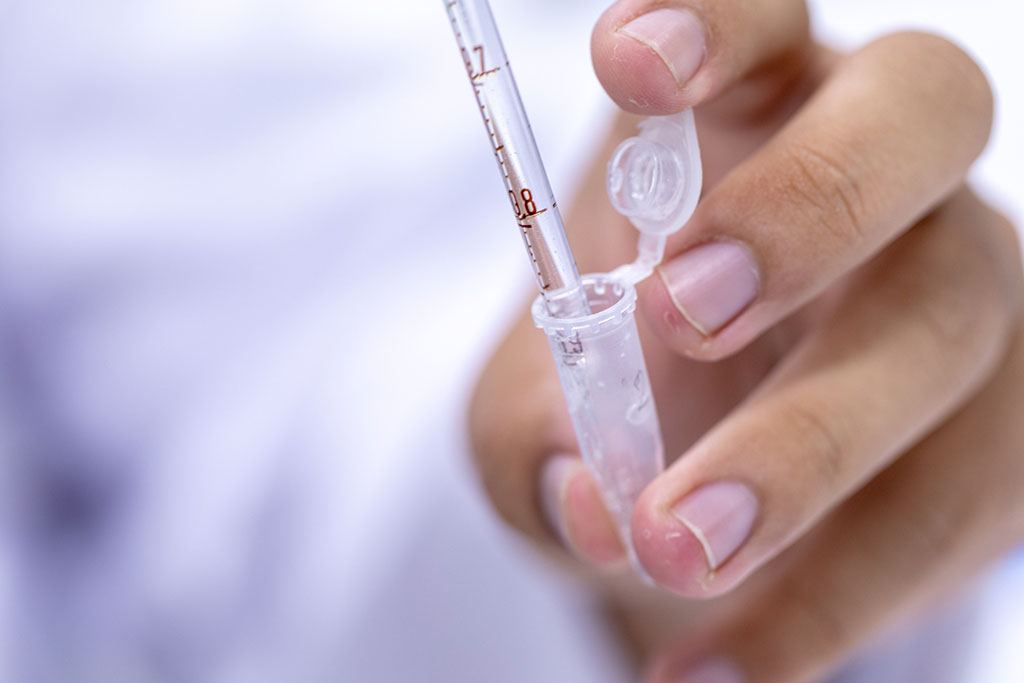
Imagen: Un kit de recolección de muestras para el panel integral expandido de 83 genes Multi-Cancer, que aumenta el rendimiento del diagnóstico. Las pruebas de la línea germinal después de la secuenciación del tumor descubren variantes clínicamente susceptibles de tratamiento (Fotografía cortesía de Invitae).
Se recomienda el asesoramiento genético y las pruebas de línea germinal para los pacientes con cáncer en quienes se sospecha enfermedad hereditaria según la presentación y los antecedentes familiares de cada paciente. Por separado, la secuenciación del ADN tumoral se utiliza cada vez más, con mayor frecuencia en pacientes con enfermedad avanzada.
La detección de variantes de la línea germinal heredadas o variantes somáticas adquiridas (es decir, mutaciones en el tumor) puede suministrar información para guiar la atención de los pacientes, incluida la selección de la terapia sistémica. Sin embargo, los dos tipos de biomarcadores son complementarios y de cada uno se pueden seguir recomendaciones diferentes.
Un equipo de científicos de la empresa de pruebas genéticas Invitae (San Francisco, CA, EUA) y sus colegas médicos, llevaron a cabo un estudio de cohorte retrospectivo de más de 2.000 pacientes con cáncer a quienes les practicaron pruebas de línea germinal después de haber secuenciado previamente su ADN tumoral. El equipo determinó el rendimiento y la utilidad de tales pruebas de línea germinal de secuenciación postumoral. De estos pacientes, el 30,5% albergaba una variante patógena de la línea germinal, la mayoría de las cuales eran potencialmente susceptibles de tratamiento, y estas variantes eran prevalentes en diversos tipos de cáncer, genes y edades de los pacientes.
El equipo informó que las variantes clínicamente importantes en ciertos genes clave tenían más probabilidades de ser de origen germinal. Aproximadamente el 40% de las variantes patógenas en BRCA1 y BRCA2 y el 28% en MLH1, MSH2, MSH6 y PMS2 eran de origen de línea germinal, mientras que solo alrededor del 4% de las variantes patógenas de TP53 lo eran. De acuerdo con las pautas de manejo actuales, las etiquetas de terapia personalizada y la elegibilidad para ensayos clínicos, la mayoría de las variantes patógenas de la línea germinal, que el equipo identificó, eran potencialmente susceptibles de tratamiento clínico.
Aproximadamente el 8% de estas variantes no se notificaron mediante la secuenciación del tumor como hallazgos somáticos o de línea germinal de importancia clínica. En gran parte se pasaron por alto debido a los límites de las diferencias de la secuenciación tumoral en la interpretación de las variantes entre los enfoques y las diferencias en los genes probados. Para los pacientes restantes, las variantes patógenas de la línea germinal se notificaron como clínicamente significativas, aunque generalmente sin una indicación de que eran de origen germinal en lugar de somático. Además, al 11,2% de los pacientes no se les detectaron variantes patógenas de la línea germinal hasta después de que desarrollaron un segundo cáncer primario que potencialmente podría haberse prevenido, ya que el 46% de esos pacientes tenían variantes patógenas asociadas con las pautas de detección o de reducción de riesgos.
Robert Nussbaum, MD, director médico de Invitae y coautor principal del estudio, dijo: “La expansión de las pautas de pruebas de la línea germinal garantizará que todos los pacientes con cáncer que puedan beneficiarse de la genética integral en su cuidado reciban esta información. Al capturar información genética tanto sobre la biología del tumor como sobre el riesgo heredado de enfermedad del paciente, podemos desarrollar planes de tratamiento personalizados más efectivos y ayudar a informar a los miembros de la familia sobre el riesgo heredado adicional, ayudando a mejorar los resultados tanto para el paciente como para la familia”.
Los autores concluyeron que la alta tasa de hallazgos procesables de las pruebas de la línea germinal después de la secuenciación tumoral sugiere beneficios para integrar aún más la genética de la línea germinal en las pruebas oncológicas de rutina y la atención a los pacientes. El estudio fue publicado el 7 de octubre de 2020 en la revista JAMA Network Open.
Enlace relacionado:
Invitae
La detección de variantes de la línea germinal heredadas o variantes somáticas adquiridas (es decir, mutaciones en el tumor) puede suministrar información para guiar la atención de los pacientes, incluida la selección de la terapia sistémica. Sin embargo, los dos tipos de biomarcadores son complementarios y de cada uno se pueden seguir recomendaciones diferentes.
Un equipo de científicos de la empresa de pruebas genéticas Invitae (San Francisco, CA, EUA) y sus colegas médicos, llevaron a cabo un estudio de cohorte retrospectivo de más de 2.000 pacientes con cáncer a quienes les practicaron pruebas de línea germinal después de haber secuenciado previamente su ADN tumoral. El equipo determinó el rendimiento y la utilidad de tales pruebas de línea germinal de secuenciación postumoral. De estos pacientes, el 30,5% albergaba una variante patógena de la línea germinal, la mayoría de las cuales eran potencialmente susceptibles de tratamiento, y estas variantes eran prevalentes en diversos tipos de cáncer, genes y edades de los pacientes.
El equipo informó que las variantes clínicamente importantes en ciertos genes clave tenían más probabilidades de ser de origen germinal. Aproximadamente el 40% de las variantes patógenas en BRCA1 y BRCA2 y el 28% en MLH1, MSH2, MSH6 y PMS2 eran de origen de línea germinal, mientras que solo alrededor del 4% de las variantes patógenas de TP53 lo eran. De acuerdo con las pautas de manejo actuales, las etiquetas de terapia personalizada y la elegibilidad para ensayos clínicos, la mayoría de las variantes patógenas de la línea germinal, que el equipo identificó, eran potencialmente susceptibles de tratamiento clínico.
Aproximadamente el 8% de estas variantes no se notificaron mediante la secuenciación del tumor como hallazgos somáticos o de línea germinal de importancia clínica. En gran parte se pasaron por alto debido a los límites de las diferencias de la secuenciación tumoral en la interpretación de las variantes entre los enfoques y las diferencias en los genes probados. Para los pacientes restantes, las variantes patógenas de la línea germinal se notificaron como clínicamente significativas, aunque generalmente sin una indicación de que eran de origen germinal en lugar de somático. Además, al 11,2% de los pacientes no se les detectaron variantes patógenas de la línea germinal hasta después de que desarrollaron un segundo cáncer primario que potencialmente podría haberse prevenido, ya que el 46% de esos pacientes tenían variantes patógenas asociadas con las pautas de detección o de reducción de riesgos.
Robert Nussbaum, MD, director médico de Invitae y coautor principal del estudio, dijo: “La expansión de las pautas de pruebas de la línea germinal garantizará que todos los pacientes con cáncer que puedan beneficiarse de la genética integral en su cuidado reciban esta información. Al capturar información genética tanto sobre la biología del tumor como sobre el riesgo heredado de enfermedad del paciente, podemos desarrollar planes de tratamiento personalizados más efectivos y ayudar a informar a los miembros de la familia sobre el riesgo heredado adicional, ayudando a mejorar los resultados tanto para el paciente como para la familia”.
Los autores concluyeron que la alta tasa de hallazgos procesables de las pruebas de la línea germinal después de la secuenciación tumoral sugiere beneficios para integrar aún más la genética de la línea germinal en las pruebas oncológicas de rutina y la atención a los pacientes. El estudio fue publicado el 7 de octubre de 2020 en la revista JAMA Network Open.
Enlace relacionado:
Invitae
Últimas Diagnóstico Molecular noticias
- Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
- Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
- Prueba de biomarcadores líquidos detecta enfermedades neurodegenerativas antes de que aparezcan síntomas
- Nuevo método genómico ayuda a diagnosticar pacientes con enfermedad renal inexplicable
- Nuevo hidrogel inteligente allana el camino para nueva "piruleta" para diagnóstico de cáncer de boca
- Prueba de biomarcadores podría mejorar diagnóstico del cáncer de endometrio
- Prueba de ADN en heces de próxima generación supera a PIF en detección del cáncer colorrectal
- Innovador análisis de sangre de pTau217 es tan preciso como imágenes cerebrales o pruebas del LCR para diagnosticar Alzheimer
- Sistema de RT-PCR en el punto de atención de 10 minutos detecta hasta 32 objetivos por muestra
- Células extraídas de orina podrían permitir detección más temprana de enfermedad renal
- Análisis de sangre identifica a personas con mayor riesgo de morir por insuficiencia cardíaca
- Análisis de sangre muestra precisión del 83 % para detectar cáncer colorrectal
- Análisis de sangre podría predecir adultos jóvenes que podrían desarrollar enfermedades del envejecimiento
- Prueba de diagnóstico molecular predice con precisión resultados de terapia en pacientes con cáncer de mama
- Novedosa tecnología de biosensor POC de molécula pequeña podría revolucionar detección temprana de enfermedades
- Simple análisis de sangre podría detectar riesgo de paro cardíaco inducido por una infección viral
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal
Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
La enfermedad de Parkinson y un grupo de trastornos neurodegenerativos relacionados conocidos como sinucleinopatías afectan a millones de personas en todo el mundo. Estas afecciones, incluida la... Más.jpg)
Herramienta bioinformática para identificar alteraciones cromosómicas en células tumorales puede mejorar diagnóstico del cáncer
La inestabilidad cromosómica es una característica común en los tumores sólidos y desempeña un papel crucial en el inicio, la progresión y la propagación... Más
Dispositivo del tamaño de una moneda aísla rápidamente plasma sanguíneo para diagnósticos clínicos más rápidos y precisos
La identificación de biomarcadores para diversos cánceres y enfermedades a menudo se basa en ADN, ARN y vesículas extracelulares libres de células. Tradicionalmente, separar... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)

.jpg)
.jpg)