Análisis rápido de un solo paso para la detección en el campo de la malaria asintomática
|
Por el equipo editorial de LabMedica en español Actualizado el 30 Sep 2020 |
Imagen: Un ensayo de diagnóstico ultrasensible aplicable en el campo, detecta específicamente secuencias de ADN y ARN de todas las especies de Plasmodium en malaria sintomática y asintomática, y entrega sus resultados rápidamente en dispositivos reporteros simples (Fotografía cortesía de Peter Nguyen, Universidad de Harvard)
Un nuevo sistema de ensayo ultrasensible, basado en CRISPR, pudo detectar los cuatro tipos principales de parásitos causantes de la malaria y se simplificó para uso en lugares que carecen de equipo de laboratorio avanzado y de técnicos altamente capacitados necesarios para las pruebas como RT-qPCR, que se utilizan extensivamente para monitorear la pandemia de COVID-19.
Los portadores asintomáticos de paludismo causado por parásitos de la especie Plasmodium (P. falciparum, P. vivax, P. ovale y P. malariae) dificultan el control y la erradicación del paludismo. Lograr la erradicación de la malaria requiere diagnósticos ultrasensibles para infecciones de baja densidad de parásitos (menos de 100 parásitos por microlitro de sangre) que se puedan utilizar en entornos con recursos limitados (SPI). Los métodos moleculares, como la PCR, tienen una alta sensibilidad y especificidad, pero siguen siendo tecnologías de alta complejidad poco prácticas para los entornos con recursos limitados.
Investigadores de la Universidad de Harvard (Cambridge, MA, EUA) y sus colaboradores en el Instituto Tecnológico de Massachusetts (Cambridge, MA, EUA) y el Instituto Wyss de Ingeniería de Inspiración Biológica (Cambridge, MA, EUA), informaron sobre el desarrollo de una herramienta de diagnóstico basada en CRISPR para la detección ultrasensible y la diferenciación de los cuatro parásitos Plasmodium, utilizando la plataforma de detección de ácido nucleico SHERLOCK (desbloqueo de reportero enzimático específico de alta sensibilidad).
Los investigadores modificaron el protocolo SHERLOCK para incorporar la enzima CRISPR-Cas12a, que programaron para que fuera activada por un ARN guía que se uniera a una secuencia diana de ácido nucleico diana específica, en este caso una secuencia de una de las cuatro especies de Plasmodium. El Cas12a activado luego escindió de forma no específica cualquier hebra de ADN monocatenario en su vecindad con una tasa de rotación extremadamente alta de aproximadamente 1250 reacciones de escisión colaterales por segundo.
La plataforma de análisis completa se amplió para incluir un protocolo SHERLOCK de extracción rápida de parásitos de 10 minutos, seguido del protocolo de diagnóstico SHERLOCK durante 60 minutos, lo que permitió la detección específica de especies de Plasmodium mediante lecturas de tira de flujo lateral o fluorescente. El ensayo fue compatible con diferentes tipos de muestras, como sangre total, plasma, suero y sangre seca y todos los componentes necesarios para la amplificación, la activación de Cas12a y la generación de señales se liofilizaron en un solo tubo de ensayo que funcionó como una “reacción de un solo recipiente” después de la reconstitución de los reactivos cuando se mezclaron con una muestra del paciente.
El desempeño del diagnóstico SHERLOCK simplificado y listo para el campo se evaluó utilizando muestras simuladas de sangre total, suero y sangre seca (DBS), así como muestras clínicas de pacientes con infecciones por P. falciparum y P. vivax. Los resultados revelaron que el ensayo era capaz de detectar menos de dos parásitos por microlitro de sangre, un límite de detección sugerido por la Organización Mundial de la Salud (OMS). Los ensayos de P. falciparum y P. vivax mostraron una sensibilidad y especificidad del 100% en muestras clínicas (cinco muestras de P. falciparum y 10 de P. vivax).
“Este ensayo de diagnóstico de paludismo SHERLOCK listo para el campo supera los requisitos de sensibilidad y especificidad establecidos por la OMS para una prueba deseada que se puede usar para detectar una baja densidad de parásitos en portadores asintomáticos de todas las principales especies de Plasmodium”, dijo el autor principal, el Dr. James Collins, profesor de ingeniería médica y ciencia en el Instituto Tecnológico de Massachusetts. “Su diseño altamente optimizado podría proporcionar una solución viable al actual cuello de botella de diagnósticos en el camino para eliminar la malaria y, en general, permitir la vigilancia de la malaria en entornos de bajos recursos”.
El ensayo rápido SHERLOCK para los parásitos de la malaria se describió en la edición en línea del 21 de septiembre de 2020 de la revista Proceedings of the National Academy of Sciences of the United States of America.
Enlace relacionado:
Universidad de Harvard
Instituto Tecnológico de Massachusetts
Instituto Wyss de Ingeniería de Inspiración Biológica
Los portadores asintomáticos de paludismo causado por parásitos de la especie Plasmodium (P. falciparum, P. vivax, P. ovale y P. malariae) dificultan el control y la erradicación del paludismo. Lograr la erradicación de la malaria requiere diagnósticos ultrasensibles para infecciones de baja densidad de parásitos (menos de 100 parásitos por microlitro de sangre) que se puedan utilizar en entornos con recursos limitados (SPI). Los métodos moleculares, como la PCR, tienen una alta sensibilidad y especificidad, pero siguen siendo tecnologías de alta complejidad poco prácticas para los entornos con recursos limitados.
Investigadores de la Universidad de Harvard (Cambridge, MA, EUA) y sus colaboradores en el Instituto Tecnológico de Massachusetts (Cambridge, MA, EUA) y el Instituto Wyss de Ingeniería de Inspiración Biológica (Cambridge, MA, EUA), informaron sobre el desarrollo de una herramienta de diagnóstico basada en CRISPR para la detección ultrasensible y la diferenciación de los cuatro parásitos Plasmodium, utilizando la plataforma de detección de ácido nucleico SHERLOCK (desbloqueo de reportero enzimático específico de alta sensibilidad).
Los investigadores modificaron el protocolo SHERLOCK para incorporar la enzima CRISPR-Cas12a, que programaron para que fuera activada por un ARN guía que se uniera a una secuencia diana de ácido nucleico diana específica, en este caso una secuencia de una de las cuatro especies de Plasmodium. El Cas12a activado luego escindió de forma no específica cualquier hebra de ADN monocatenario en su vecindad con una tasa de rotación extremadamente alta de aproximadamente 1250 reacciones de escisión colaterales por segundo.
La plataforma de análisis completa se amplió para incluir un protocolo SHERLOCK de extracción rápida de parásitos de 10 minutos, seguido del protocolo de diagnóstico SHERLOCK durante 60 minutos, lo que permitió la detección específica de especies de Plasmodium mediante lecturas de tira de flujo lateral o fluorescente. El ensayo fue compatible con diferentes tipos de muestras, como sangre total, plasma, suero y sangre seca y todos los componentes necesarios para la amplificación, la activación de Cas12a y la generación de señales se liofilizaron en un solo tubo de ensayo que funcionó como una “reacción de un solo recipiente” después de la reconstitución de los reactivos cuando se mezclaron con una muestra del paciente.
El desempeño del diagnóstico SHERLOCK simplificado y listo para el campo se evaluó utilizando muestras simuladas de sangre total, suero y sangre seca (DBS), así como muestras clínicas de pacientes con infecciones por P. falciparum y P. vivax. Los resultados revelaron que el ensayo era capaz de detectar menos de dos parásitos por microlitro de sangre, un límite de detección sugerido por la Organización Mundial de la Salud (OMS). Los ensayos de P. falciparum y P. vivax mostraron una sensibilidad y especificidad del 100% en muestras clínicas (cinco muestras de P. falciparum y 10 de P. vivax).
“Este ensayo de diagnóstico de paludismo SHERLOCK listo para el campo supera los requisitos de sensibilidad y especificidad establecidos por la OMS para una prueba deseada que se puede usar para detectar una baja densidad de parásitos en portadores asintomáticos de todas las principales especies de Plasmodium”, dijo el autor principal, el Dr. James Collins, profesor de ingeniería médica y ciencia en el Instituto Tecnológico de Massachusetts. “Su diseño altamente optimizado podría proporcionar una solución viable al actual cuello de botella de diagnósticos en el camino para eliminar la malaria y, en general, permitir la vigilancia de la malaria en entornos de bajos recursos”.
El ensayo rápido SHERLOCK para los parásitos de la malaria se describió en la edición en línea del 21 de septiembre de 2020 de la revista Proceedings of the National Academy of Sciences of the United States of America.
Enlace relacionado:
Universidad de Harvard
Instituto Tecnológico de Massachusetts
Instituto Wyss de Ingeniería de Inspiración Biológica
Últimas Tecnología noticias
- Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
- Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
- Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
- Primera tecnología de su tipo para detectar glucosa en saliva humana
- Dispositivo electroquímico identifica personas con mayor riesgo de osteoporosis mediante una sola gota de sangre
- Nueva prueba no invasiva detecta infección por malaria sin muestra de sangre
- Dispositivos de detección optofluídicos portátiles podrían realizar simultáneamente una variedad de pruebas médicas
- Solución de software para punto de atención ayuda a manejar escenarios de pruebas POC dispares en ubicaciones de prueba de pacientes
- Biosensor electrónico detecta biomarcadores en muestras de sangre completa sin agregar reactivos
- Prueba innovadora detecta marcadores biológicos relacionados con una variedad mayor de cánceres
- Kit de detección rápida POC determina la salud intestinal a partir de muestras de suero sanguíneo y heces
- Dispositivo convierte teléfono inteligente en microscopio de fluorescencia por solo 50 dólares
- Lector de tubos portátil habilitado para Wi-Fi diseñado para una fácil portabilidad
- Novedosa plataforma de pruebas de diagnóstico asegura el tiempo de respuesta a situaciones de pandemia emergentes
- Transistor revolucionario podría permitir dispositivos portátiles para medir el sodio y el potasio en la sangre
- Sensor portátil de bajo costo detecta metales pesados en el sudor
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... Más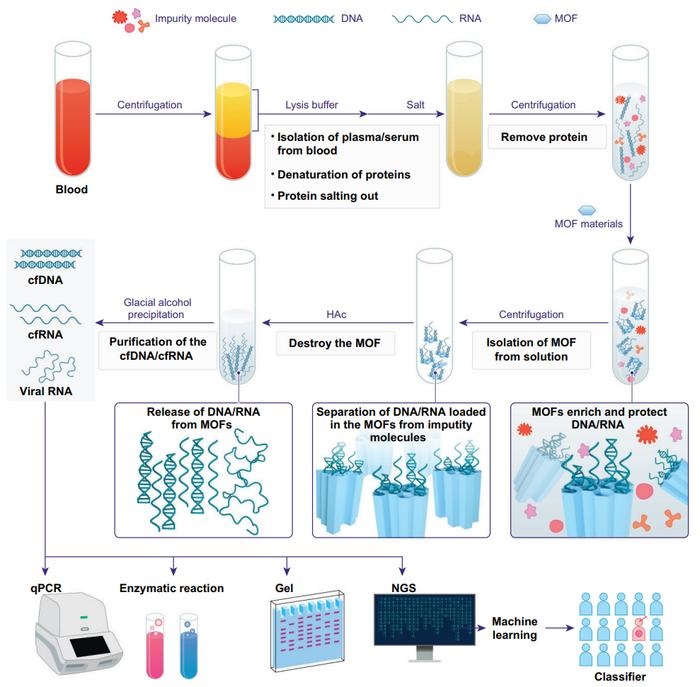
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal
Innovador dispositivo de extracción de sangre supera obstáculos comunes relacionados con la flebotomía
La incomodidad asociada con las extracciones de sangre tradicionales genera un problema importante: aproximadamente el 30 % de las pruebas de diagnóstico prescritas por los médicos nunca... Más
Dispositivo POC intraoperatorio distingue entre quistes ováricos benignos y malignos en 15 minutos
Los quistes ováricos representan un problema de salud importante para las mujeres en todo el mundo, y hasta el 10 % experimenta esta afección en algún momento de sus vidas.... Más
Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
La enfermedad de Parkinson y un grupo de trastornos neurodegenerativos relacionados conocidos como sinucleinopatías afectan a millones de personas en todo el mundo. Estas afecciones, incluida la... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)

.jpg)
.jpg)

