Biopsia líquida detecta la enfermedad residual en el cáncer de mama
|
Por el equipo editorial de LabMedica en español Actualizado el 08 Jan 2020 |
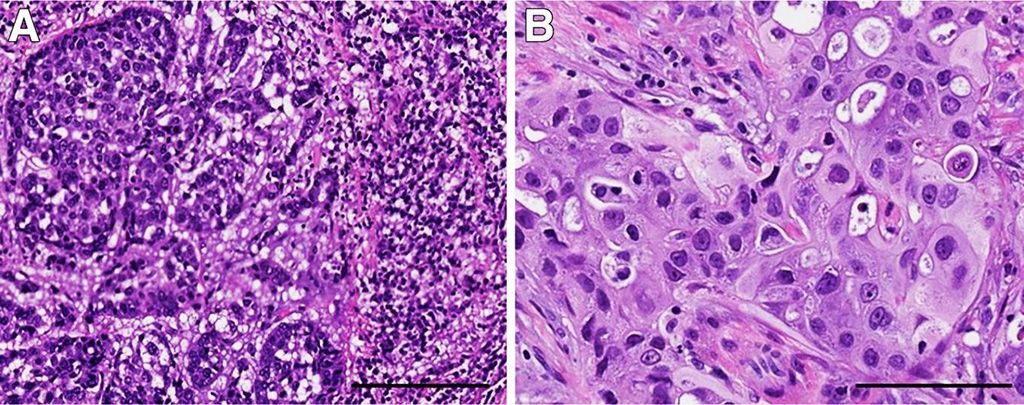
Imagen: Variantes morfológicas del cáncer de mama triple negativo (TNBC) con diferentes alteraciones genéticas. A: TNBC con características histológicas basales que contienen un infiltrado linfocítico estromal prominente; este tumor tenía amplificación de MYC. B: TNBC con diferenciación apocrina y una mutación en PI3KCA. Las células tumorales tienen abundante citoplasma eosinofílico, núcleos redondos y nucleolos prominentes (Fotografía cortesía de la Facultad de Medicina Geisel).
El concepto de ADN circulante o células tumorales para identificar pacientes con cáncer residual presente después de un tratamiento curativo putativo en etapa temprana, ha avanzado rápidamente en múltiples tipos de tumores desde algunas de las primeras pruebas prometedoras en cáncer colorrectal.
Los cánceres de seno triple negativos, a diferencia de otros tipos de cáncer de mama, conllevan un riesgo significativo de recurrencia incluso cuando se diagnostican en etapas tempranas. Además, carecen de la creciente lista de opciones de tratamiento específicas disponibles para otros subconjuntos moleculares y debido a esto, el estándar de atención se limita a la quimioterapia, la radiación y la cirugía.
Científicos de la Facultad de Medicina de la Universidad de Indiana (Indianápolis, IN, EUA) y sus colegas analizaron muestras de plasma retrospectivas que habían sido recolectadas de pacientes inscritos en el ensayo clínico Fase II BRE12-158, que estudió la terapia dirigida genómicamente versus la elección del tratamiento por parte del médico después de la quimioterapia preoperatoria en pacientes con cáncer de mama triple negativo de alto riesgo.
El ensayo incluyó a 196 mujeres en total, a 142 de ellas les realizaron la secuenciación de ADN tumoral circulante (ADNc) con la Prueba Líquida FoundationOne (Foundation Medicine, Cambridge, MA, EUA) y suficiente seguimiento clínico para estudiar. Las pruebas identificaron ADNc mutado en 90 de las pacientes, alrededor del 60%, con TP53 como el gen mutado más comúnmente, seguido de otros que se asocian comúnmente con el cáncer de mama.
A los 17,2 meses de seguimiento, las pacientes en las que se había detectado ADNc tenían una supervivencia libre de enfermedad distante (DDFS) significativamente inferior, en comparación con aquellas que no. El grupo que mostró mutaciones circulantes sobrevivió sin recurrencias distantes 32,5 meses en promedio, mientras que las pacientes sin ADNc no habían alcanzado una mediana. A los 24 meses, la tasa de DDFS fue del 56% para las pacientes con ADNc positivo, en comparación con el 81% para las pacientes con ADNc negativo. La combinación de ADNc y la detección de células tumorales circulantes aumentó esto aún más. Los pacientes con doble positivo (con ADNc y células tumorales circulantes presentes) tenían un DDFS a los dos años de solo el 52% en comparación con el 89% para los negativos dobles.
Milan Radovich, PhD, profesor asociado y primer autor del estudio, dijo: “Con la quimioterapia neoadyuvante, aproximadamente un tercio de los pacientes triple negativos logran un estado de respuesta patológica completa, en el que no hay evidencia de su tumor una vez que los cirujanos lo eliminan. Este subgrupo tiene resultados mucho mejores que los dos tercios que aún tienen enfermedad residual después de la quimioterapia neoadyuvante”. El estudio se presentó en el Simposio de Cáncer de Mama de San Antonio celebrado del 10 al 14 de diciembre de 2019 en San Antonio, TX, EUA.
Enlace relacionado:
Facultad de Medicina de la Universidad de Indiana
Foundation Medicine
Los cánceres de seno triple negativos, a diferencia de otros tipos de cáncer de mama, conllevan un riesgo significativo de recurrencia incluso cuando se diagnostican en etapas tempranas. Además, carecen de la creciente lista de opciones de tratamiento específicas disponibles para otros subconjuntos moleculares y debido a esto, el estándar de atención se limita a la quimioterapia, la radiación y la cirugía.
Científicos de la Facultad de Medicina de la Universidad de Indiana (Indianápolis, IN, EUA) y sus colegas analizaron muestras de plasma retrospectivas que habían sido recolectadas de pacientes inscritos en el ensayo clínico Fase II BRE12-158, que estudió la terapia dirigida genómicamente versus la elección del tratamiento por parte del médico después de la quimioterapia preoperatoria en pacientes con cáncer de mama triple negativo de alto riesgo.
El ensayo incluyó a 196 mujeres en total, a 142 de ellas les realizaron la secuenciación de ADN tumoral circulante (ADNc) con la Prueba Líquida FoundationOne (Foundation Medicine, Cambridge, MA, EUA) y suficiente seguimiento clínico para estudiar. Las pruebas identificaron ADNc mutado en 90 de las pacientes, alrededor del 60%, con TP53 como el gen mutado más comúnmente, seguido de otros que se asocian comúnmente con el cáncer de mama.
A los 17,2 meses de seguimiento, las pacientes en las que se había detectado ADNc tenían una supervivencia libre de enfermedad distante (DDFS) significativamente inferior, en comparación con aquellas que no. El grupo que mostró mutaciones circulantes sobrevivió sin recurrencias distantes 32,5 meses en promedio, mientras que las pacientes sin ADNc no habían alcanzado una mediana. A los 24 meses, la tasa de DDFS fue del 56% para las pacientes con ADNc positivo, en comparación con el 81% para las pacientes con ADNc negativo. La combinación de ADNc y la detección de células tumorales circulantes aumentó esto aún más. Los pacientes con doble positivo (con ADNc y células tumorales circulantes presentes) tenían un DDFS a los dos años de solo el 52% en comparación con el 89% para los negativos dobles.
Milan Radovich, PhD, profesor asociado y primer autor del estudio, dijo: “Con la quimioterapia neoadyuvante, aproximadamente un tercio de los pacientes triple negativos logran un estado de respuesta patológica completa, en el que no hay evidencia de su tumor una vez que los cirujanos lo eliminan. Este subgrupo tiene resultados mucho mejores que los dos tercios que aún tienen enfermedad residual después de la quimioterapia neoadyuvante”. El estudio se presentó en el Simposio de Cáncer de Mama de San Antonio celebrado del 10 al 14 de diciembre de 2019 en San Antonio, TX, EUA.
Enlace relacionado:
Facultad de Medicina de la Universidad de Indiana
Foundation Medicine
Últimas Diagnóstico Molecular noticias
- Prueba de sangre predice con precisión el riesgo de cáncer de pulmón y reduce la necesidad de escaneos de TC
- Firma única de autoanticuerpos ayuda a diagnosticar la esclerosis múltiple años antes de la aparición de síntomas
- Prueba de sangre podría detectar cánceres asociados al VPH 10 años antes del diagnóstico clínico
- Un diagnóstico de bajo costo en el punto de atención ampliará el acceso a pruebas de enfermedades de transmisión sexual
- Prueba de orina analiza 18 genes para identificar el cáncer de próstata de alto grado
- Prueba en orina detecta cáncer de cabeza y cuello
- Prueba de sangre detecta y monitorea cáncer pulmonar de células pequeñas agresivo
- Ensayo de aprendizaje automático basado en sangre detecta de forma no invasiva el cáncer de ovario
- Ensayo de PCR simple diferencia con precisión entre los subtipos de cáncer de pulmón de células pequeñas
- Enfoque revolucionario de análisis de células T permite detección temprana del cáncer
- Prueba genética única podría acelerar el diagnóstico de trastornos raros del desarrollo
- Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
- Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
- Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
- Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
- Prueba de biomarcadores líquidos detecta enfermedades neurodegenerativas antes de que aparezcan síntomas
Canales
Química Clínica
ver canal
Espectrómetro de masas impreso en 3D para el punto de atención supera a los modelos de última generación
La espectrometría de masas es una técnica precisa para identificar los componentes químicos de una muestra y tiene un potencial significativo para monitorear estados de salud de enfermedades... Más.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Prueba de sangre predice con precisión el riesgo de cáncer de pulmón y reduce la necesidad de escaneos de TC
El cáncer de pulmón es extremadamente difícil de detectar tempranamente debido a las limitaciones de las tecnologías de detección actuales, que son costosas, a veces... Más
Firma única de autoanticuerpos ayuda a diagnosticar la esclerosis múltiple años antes de la aparición de síntomas
Se cree que las enfermedades autoinmunes como la esclerosis múltiple (EM) ocurren en parte debido a respuestas inmunes inusuales a infecciones comunes. Los primeros síntomas de la EM, incluidos... Más
Prueba de sangre podría detectar cánceres asociados al VPH 10 años antes del diagnóstico clínico
Se sabe que el virus del papiloma humano (VPH) causa varios cánceres, incluidos los de genitales, ano, boca, garganta y cuello uterino. El cáncer orofaríngeo asociado al VPH (VPH+COF)... Más
Un diagnóstico de bajo costo en el punto de atención ampliará el acceso a pruebas de enfermedades de transmisión sexual
La gonorrea es la segunda infección bacteriana de transmisión sexual (ITS) más comúnmente reportada, con alrededor de 82 millones de casos en todo el mundo en 2020. La infección puede tener graves consecuencias... MásHematología
ver canal
Primera prueba NAT 4 en 1 para el cribado de arbovirus podría reducir el riesgo de infecciones transmitidas por transfusiones
Los arbovirus representan una amenaza emergente para la salud mundial, exacerbada por el cambio climático y el aumento de la conectividad mundial que está facilitando su propagación a nuevas regiones.... Más
Instrumento de próxima generación detecta trastornos de la hemoglobina en recién nacidos
Las hemoglobinopatías, las enfermedades hereditarias más extendidas a nivel mundial, afectan a alrededor del 7 % de la población como portadores, y el 2,7 % de los recién nacidos nacen con estas enfermedades.... Más
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásInmunología
ver canal
Análisis de sangre para diagnóstico de rechazo celular después de trasplante de órganos podría reemplazar las biopsias quirúrgicas
Los órganos trasplantados enfrentan constantemente el riesgo de ser rechazados por el sistema inmunológico del receptor, que los diferencia de los órganos no propios mediante... Más
Herramienta de IA ajusta con precisión los medicamentos contra el cáncer con los pacientes utilizando información de cada célula tumoral
Las estrategias actuales para emparejar a los pacientes con cáncer con tratamientos específicos a menudo dependen de la secuenciación masiva de ADN y ARN tumoral, que proporciona un perfil promedio de... Más
Pruebas genéticas combinadas con la detección de fármacos personalizadas en muestras de tumores podrían revolucionar el tratamiento del cáncer
El tratamiento del cáncer generalmente se adhiere a un estándar de atención: regímenes establecidos y validados estadísticamente que son efectivos para la mayoría de los pacientes. Sin embargo, la variabilidad... Más
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... MásMicrobiología
ver canal
Nuevos ensayos de hepatitis con marcado CE permite la detección temprana de infecciones
Según la Organización Mundial de la Salud (OMS), se estima que 354 millones de personas en todo el mundo padecen hepatitis B o C crónica. Estos virus son las principales causas de... Más
Prueba de PCR múltiplex identifica el 95 % de los patógenos que causan la sepsis en una hora
La sepsis contribuye a una de cada tres muertes hospitalarias en los Estados Unidos y, a nivel mundial, el shock séptico conlleva una tasa de mortalidad del 30 al 40 %. El diagnóstico temprano de la sepsis... Más
Prueba de bacterias bucales podría predecir la progresión del cáncer de colon
El cáncer de colon, una enfermedad relativamente común pero difícil de diagnosticar, requiere confirmación mediante una colonoscopia o cirugía. Recientemente, ha habido... Más.jpg)
Firma metabólica unica podría permitir el diagnóstico de sepsis dentro de una hora de la extracción de sangre
La sepsis es una afección potencialmente mortal provocada por una respuesta extrema del cuerpo a una infección. Requiere intervención médica inmediata para evitar una posible muerte o daños duraderos.... MásTecnología
ver canal
Nuevo sistema de diagnóstico de laboratorio en un chip iguala la precisión de las pruebas de PCR
Si bien las pruebas de PCR son el estándar de oro en cuanto a precisión para las pruebas de virología, tienen limitaciones como la complejidad, la necesidad de operadores de laboratorio capacitados y tiempos... Más
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más













