Se descubre una bacteria patógena en los cerebros de los pacientes con Alzheimer
|
Por el equipo editorial de LabMedica en español Actualizado el 13 Feb 2019 |
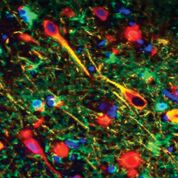
Imagen: Gingipains de Porphyromonas gingivalis en las neuronas del cerebro de un paciente con Alzheimer. Gingipains de P. gingivalis = rojo, neuronas = amarillo, astrocitos = verde (Fotografía cortesía de Cortexyme).
Los pacientes con enfermedad de Alzheimer (EA) muestran una neuroinflamación compatible con infección, incluida la activación de la microglía, la activación del inflamasoma, la activación del complemento y perfiles alterados de citoquinas.
Se han encontrado agentes infecciosos en el cerebro y se ha postulado que están involucrados con la EA, pero no se ha podido establecer evidencia sólida de causalidad. La reciente caracterización de amiloide-β (Aβ) como un péptido antimicrobiano ha renovado el interés en identificar una posible causa infecciosa de la EA.
Un equipo internacional de científicos, incluidos los de la Escuela de Odontología de la Universidad de Louisville (Louisville, KY, EUA) investigó la prevalencia de Porphyromonas gingivalis en el cerebro de pacientes con EA y para dilucidar posibles mecanismos de acción dependientes de P. gingivalis para la neurodegeneración y la patología de la EA. P. gingivalis se encuentra principalmente durante las infecciones gingivales y periodontales; sin embargo, también se puede encontrar en niveles bajos en el 25% de los individuos sanos sin enfermedad oral.
El equipo obtuvo tejidos cerebrales humanos postmortem y un análisis patológico independiente confirmó que cualquier patología amiloide se consideraba normal para la edad en los casos de control seleccionados para este estudio. Los microarrays de tejido cerebral humano (TMA) comprendieron un total de 58 muestras de núcleos de 2 mm de diámetro, 29 de individuos control sin demencia y 29 de casos de EA, cada uno en dos arrays. Los anticuerpos contra los gingipains se optimizaron inicialmente en cortes de tejido gingival incluidos en parafina y fijados con formalina, recolectados de pacientes con enfermedad periodontal. El análisis histológico se realizó en un microscopio motorizado Olympus BX61 (Olympus, Tokio, Japón). Se utilizaron varias técnicas moleculares para identificar otros factores en el estudio.
El equipo del estudio encontró las enzimas tóxicas del organismo, o gingipains, en las neuronas de los pacientes con EA. Las gingipains se secretan y se transportan a las superficies de la membrana bacteriana externa y se ha demostrado que son mediadoras de la toxicidad de P. gingivalis en una variedad de células. El equipo correlacionó los niveles de gingipains con la patología relacionada con dos marcadores: tau, una proteína necesaria para la función neuronal normal, y la ubiquitina, una pequeña etiqueta de proteína que marca las proteínas dañadas. En modelos animales, la infección oral por P. gingivalis condujo a la colonización cerebral y al aumento de la producción de beta amiloide (Aβ), un componente de las placas amiloides comúnmente asociadas con la EA.
En estudios preclínicos, los científicos demostraron que al inhibir el compuesto COR388, se redujo la carga bacteriana de una infección cerebral por P. gingivalis establecida, se bloqueó la producción de Aβ42, se redujo la neuroinflamación y se protegieron las neuronas en el hipocampo, la parte del cerebro que media la memoria y con frecuencia se atrofia a principios del desarrollo de la EA. El estudio fue publicado el 23 de enero de 2019 en la revista Science Advances.
Enlace relacionado:
Escuela de Odontología de la Universidad de Louisville
Olympus
Se han encontrado agentes infecciosos en el cerebro y se ha postulado que están involucrados con la EA, pero no se ha podido establecer evidencia sólida de causalidad. La reciente caracterización de amiloide-β (Aβ) como un péptido antimicrobiano ha renovado el interés en identificar una posible causa infecciosa de la EA.
Un equipo internacional de científicos, incluidos los de la Escuela de Odontología de la Universidad de Louisville (Louisville, KY, EUA) investigó la prevalencia de Porphyromonas gingivalis en el cerebro de pacientes con EA y para dilucidar posibles mecanismos de acción dependientes de P. gingivalis para la neurodegeneración y la patología de la EA. P. gingivalis se encuentra principalmente durante las infecciones gingivales y periodontales; sin embargo, también se puede encontrar en niveles bajos en el 25% de los individuos sanos sin enfermedad oral.
El equipo obtuvo tejidos cerebrales humanos postmortem y un análisis patológico independiente confirmó que cualquier patología amiloide se consideraba normal para la edad en los casos de control seleccionados para este estudio. Los microarrays de tejido cerebral humano (TMA) comprendieron un total de 58 muestras de núcleos de 2 mm de diámetro, 29 de individuos control sin demencia y 29 de casos de EA, cada uno en dos arrays. Los anticuerpos contra los gingipains se optimizaron inicialmente en cortes de tejido gingival incluidos en parafina y fijados con formalina, recolectados de pacientes con enfermedad periodontal. El análisis histológico se realizó en un microscopio motorizado Olympus BX61 (Olympus, Tokio, Japón). Se utilizaron varias técnicas moleculares para identificar otros factores en el estudio.
El equipo del estudio encontró las enzimas tóxicas del organismo, o gingipains, en las neuronas de los pacientes con EA. Las gingipains se secretan y se transportan a las superficies de la membrana bacteriana externa y se ha demostrado que son mediadoras de la toxicidad de P. gingivalis en una variedad de células. El equipo correlacionó los niveles de gingipains con la patología relacionada con dos marcadores: tau, una proteína necesaria para la función neuronal normal, y la ubiquitina, una pequeña etiqueta de proteína que marca las proteínas dañadas. En modelos animales, la infección oral por P. gingivalis condujo a la colonización cerebral y al aumento de la producción de beta amiloide (Aβ), un componente de las placas amiloides comúnmente asociadas con la EA.
En estudios preclínicos, los científicos demostraron que al inhibir el compuesto COR388, se redujo la carga bacteriana de una infección cerebral por P. gingivalis establecida, se bloqueó la producción de Aβ42, se redujo la neuroinflamación y se protegieron las neuronas en el hipocampo, la parte del cerebro que media la memoria y con frecuencia se atrofia a principios del desarrollo de la EA. El estudio fue publicado el 23 de enero de 2019 en la revista Science Advances.
Enlace relacionado:
Escuela de Odontología de la Universidad de Louisville
Olympus
Últimas Microbiología noticias
- Análisis de sangre predice sepsis e insuficiencia orgánica en niños
- Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
- Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
- Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
- Nuevo análisis para tuberculosis podría ampliar acceso a pruebas en países de ingresos bajos y medios
- Prueba rápida diagnostica enfermedades tropicales en horas para tratamiento con antibióticos más rápido
- Pruebas moleculares rápidas permiten tratamiento antibiótico más rápido y específico para neumonía
- Plataforma rápida de PSA proporciona resultados terapéuticos específicos días antes que el estándar de atención actual
- Nuevo método de análisis detecta patógenos en sangre de forma más rápida y precisa al fundir ADN
- Prueba rápida de sepsis ofrece resultados dos días más rápidos
- Diagnóstico rápido portátil por PCR podría detectar gonorrea y susceptibilidad a antibióticos
- Prueba CRISPR diagnostica mpox más rápido que método de PCR de laboratorio
- Prueba de PCR multiplexada para detección de patógenos y resistencia a antibióticos ayuda a brindar un tratamiento rápido de ITU
- Nuevo algoritmo detecta e identifica nuevos organismos bacterianos
- Analizador de mesa promete detección de ITU en 1 hora e indicación de sensibilidad a antibióticos
- Prueba rápida junto a la cama podría proteger a recién nacidos de enfermedades potencialmente mortales
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... Más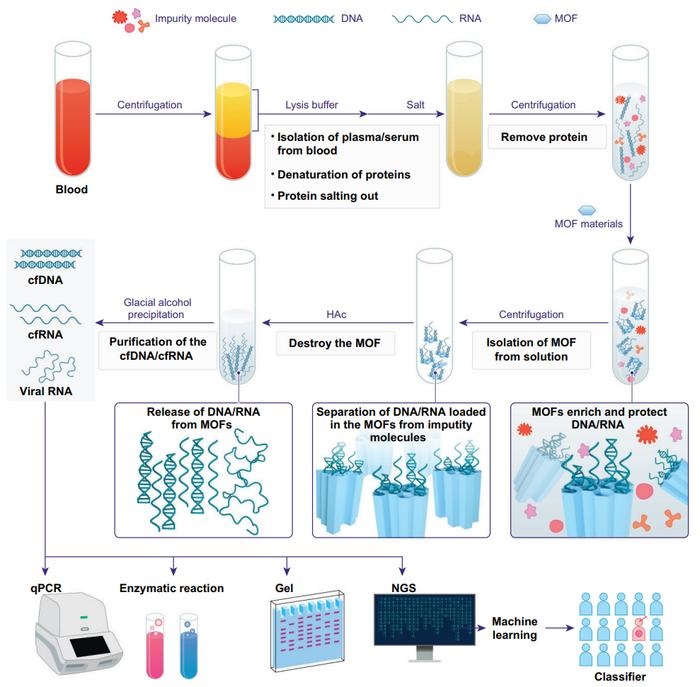
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más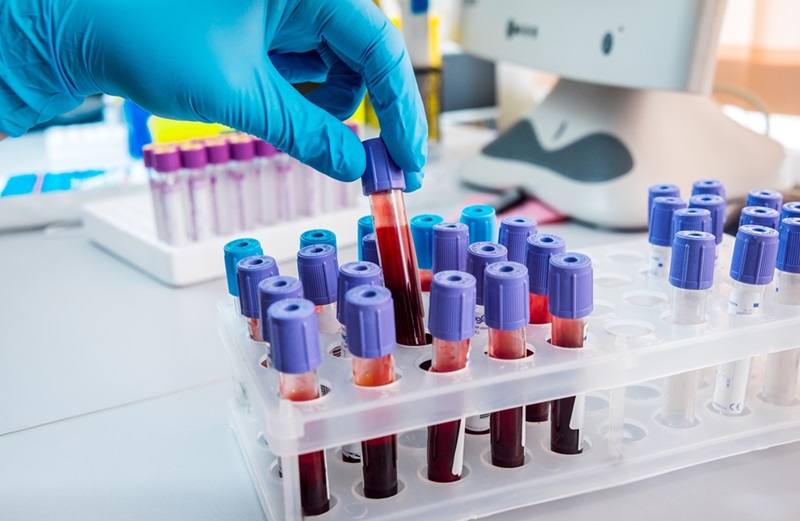
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)

.jpg)