Se identifica una mutación genética para la vulnerabilidad a la TB
|
Por el equipo editorial de LabMedica en español Actualizado el 23 Jan 2019 |
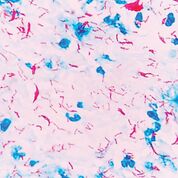
Imagen: Fotomicrografía de Mycobacterium tuberculosis usando la coloración de Ziehl-Neelsen en un frotis de esputo (Fotografía cortesía de la Universidad de Rockefeller).
Aproximadamente una de cada cinco personas en todo el mundo está infectada con Mycobacterium tuberculosis, la bacteria causante de la tuberculosis. De ellos, solo el 10%, como máximo, mostrarán síntomas, porque la mayoría de los sistemas inmunológicos tienen herramientas para combatir al microbio. Sin embargo, cuando estas herramientas están ausentes o son disfuncionales, la infección puede dañar los pulmones y otros órganos, e incluso causar la muerte.
Se han descubierto mutaciones genéticas que privan al sistema inmune de su capacidad para combatir gérmenes más omnipresentes de la misma familia bacteriana, las micobacterias. Se han dilucidado anomalías moleculares que hacen que las personas sean vulnerables a las infecciones por micobacterias. Esta evidencia apunta a estrategias para tratar o prevenir algunos casos de tuberculosis (TB).
Un gran equipo internacional de científicos liderado por la Universidad de Rockefeller (Nueva York, NY, EUA) recolectó muestras de ADN de pacientes con formas activas de la enfermedad. Al analizar estas muestras, el equipo descubrió que el riesgo de desarrollar TB aumenta en las personas que tienen dos copias de una variación particular del gen que codifica la enzima tirosina-proteína quinasa (TYK2).
El equipo informó que los pacientes con deficiencia completa de interleuquina (IL)-12Rβ2 o IL-23R autosómica recesiva, que carecen de respuestas a IL-12 o IL-23 solamente, todos ellos, presentan inesperadamente micobacteriosis sin candidiasis. Mostraron que las células αβ T, γδ T, B, NK, ILC1 e ILC2 de donantes sanos producen preferentemente IFN-γ en respuesta a la IL-12, mientras que las células NKT y MAIT producen preferentemente IFN-γ en respuesta a IL-23 . También demostraron que el desarrollo de células T CD4+ productoras de IFN-γ, incluidas, en particular, células TH1* específicas de micobacterias (CD45RA-CCR6+), depende tanto de IL-12 como de IL-23. Mostraron que los genes IL12RB1, IL12RB2 e IL23R tienen frecuencias similares de variantes deletéreas en la población general.
Jean-Laurent Casanova, MD, PhD, profesor y autor principal del estudio, dijo: “En los europeos, una de cada 600 personas tiene dos copias de esta variación de TYK2. Y en el resto de la población, la tasa está entre uno en 1.000 a uno en 10.000, que sigue siendo común. Aquí en Rockefeller, probablemente hay entre cuatro y seis personas que tienen esta predisposición genética a la TB. Sin embargo, eso no quiere decir que esas personas realmente desarrollarán la enfermedad y, de hecho, probablemente no lo harán. En Nueva York, alguien puede tener esta mutación y su riesgo de contraer TB es efectivamente cero. Pero si esa persona va a trabajar en un hospital de TB en África, entonces la probabilidad de contraer TB es alta, cien veces más alta de lo que sería para una persona sin la variante genética”. El estudio se publicó el 21 de diciembre de 2018 en la revista Science Immunology.
Enlace relacionado:
Universidad de Rockefeller
Se han descubierto mutaciones genéticas que privan al sistema inmune de su capacidad para combatir gérmenes más omnipresentes de la misma familia bacteriana, las micobacterias. Se han dilucidado anomalías moleculares que hacen que las personas sean vulnerables a las infecciones por micobacterias. Esta evidencia apunta a estrategias para tratar o prevenir algunos casos de tuberculosis (TB).
Un gran equipo internacional de científicos liderado por la Universidad de Rockefeller (Nueva York, NY, EUA) recolectó muestras de ADN de pacientes con formas activas de la enfermedad. Al analizar estas muestras, el equipo descubrió que el riesgo de desarrollar TB aumenta en las personas que tienen dos copias de una variación particular del gen que codifica la enzima tirosina-proteína quinasa (TYK2).
El equipo informó que los pacientes con deficiencia completa de interleuquina (IL)-12Rβ2 o IL-23R autosómica recesiva, que carecen de respuestas a IL-12 o IL-23 solamente, todos ellos, presentan inesperadamente micobacteriosis sin candidiasis. Mostraron que las células αβ T, γδ T, B, NK, ILC1 e ILC2 de donantes sanos producen preferentemente IFN-γ en respuesta a la IL-12, mientras que las células NKT y MAIT producen preferentemente IFN-γ en respuesta a IL-23 . También demostraron que el desarrollo de células T CD4+ productoras de IFN-γ, incluidas, en particular, células TH1* específicas de micobacterias (CD45RA-CCR6+), depende tanto de IL-12 como de IL-23. Mostraron que los genes IL12RB1, IL12RB2 e IL23R tienen frecuencias similares de variantes deletéreas en la población general.
Jean-Laurent Casanova, MD, PhD, profesor y autor principal del estudio, dijo: “En los europeos, una de cada 600 personas tiene dos copias de esta variación de TYK2. Y en el resto de la población, la tasa está entre uno en 1.000 a uno en 10.000, que sigue siendo común. Aquí en Rockefeller, probablemente hay entre cuatro y seis personas que tienen esta predisposición genética a la TB. Sin embargo, eso no quiere decir que esas personas realmente desarrollarán la enfermedad y, de hecho, probablemente no lo harán. En Nueva York, alguien puede tener esta mutación y su riesgo de contraer TB es efectivamente cero. Pero si esa persona va a trabajar en un hospital de TB en África, entonces la probabilidad de contraer TB es alta, cien veces más alta de lo que sería para una persona sin la variante genética”. El estudio se publicó el 21 de diciembre de 2018 en la revista Science Immunology.
Enlace relacionado:
Universidad de Rockefeller
Últimas Microbiología noticias
- Análisis de sangre predice sepsis e insuficiencia orgánica en niños
- Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
- Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
- Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
- Nuevo análisis para tuberculosis podría ampliar acceso a pruebas en países de ingresos bajos y medios
- Prueba rápida diagnostica enfermedades tropicales en horas para tratamiento con antibióticos más rápido
- Pruebas moleculares rápidas permiten tratamiento antibiótico más rápido y específico para neumonía
- Plataforma rápida de PSA proporciona resultados terapéuticos específicos días antes que el estándar de atención actual
- Nuevo método de análisis detecta patógenos en sangre de forma más rápida y precisa al fundir ADN
- Prueba rápida de sepsis ofrece resultados dos días más rápidos
- Diagnóstico rápido portátil por PCR podría detectar gonorrea y susceptibilidad a antibióticos
- Prueba CRISPR diagnostica mpox más rápido que método de PCR de laboratorio
- Prueba de PCR multiplexada para detección de patógenos y resistencia a antibióticos ayuda a brindar un tratamiento rápido de ITU
- Nuevo algoritmo detecta e identifica nuevos organismos bacterianos
- Analizador de mesa promete detección de ITU en 1 hora e indicación de sensibilidad a antibióticos
- Prueba rápida junto a la cama podría proteger a recién nacidos de enfermedades potencialmente mortales
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... Más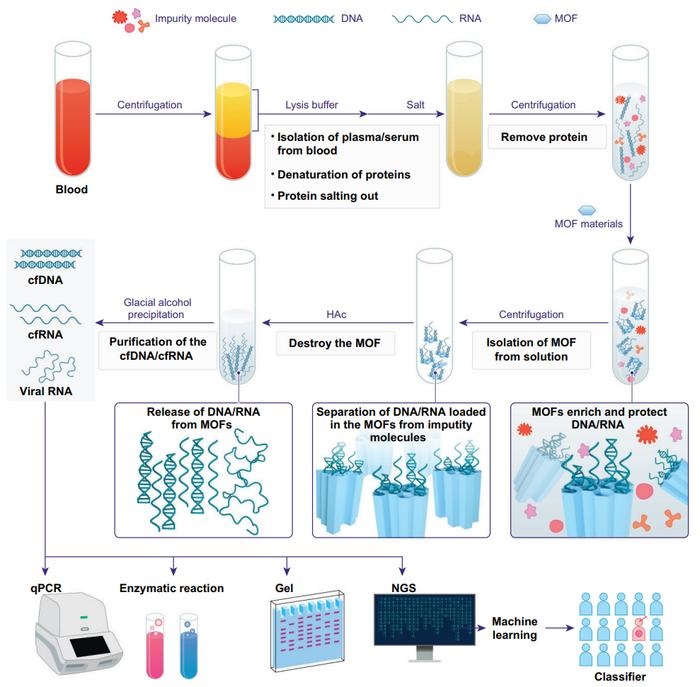
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más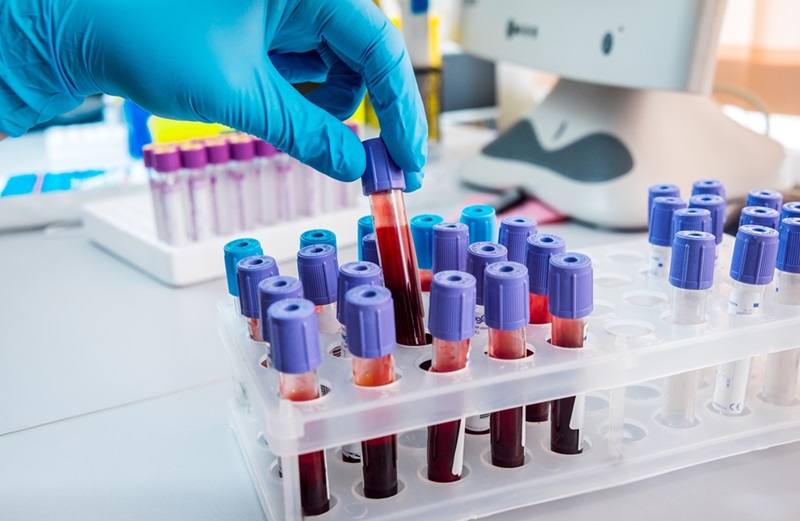
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal
Innovador dispositivo de extracción de sangre supera obstáculos comunes relacionados con la flebotomía
La incomodidad asociada con las extracciones de sangre tradicionales genera un problema importante: aproximadamente el 30 % de las pruebas de diagnóstico prescritas por los médicos nunca... Más
Dispositivo POC intraoperatorio distingue entre quistes ováricos benignos y malignos en 15 minutos
Los quistes ováricos representan un problema de salud importante para las mujeres en todo el mundo, y hasta el 10 % experimenta esta afección en algún momento de sus vidas.... Más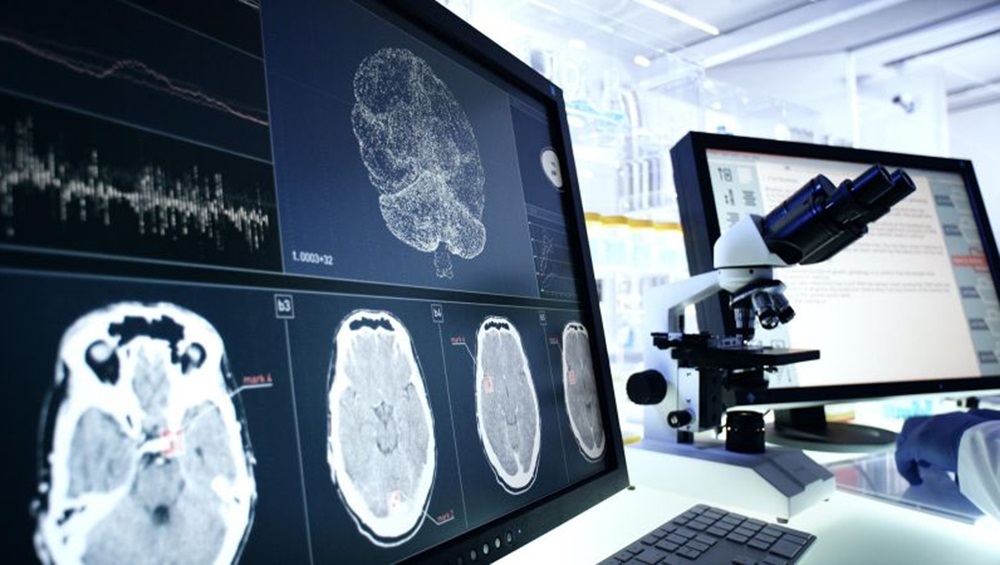
Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
La enfermedad de Parkinson y un grupo de trastornos neurodegenerativos relacionados conocidos como sinucleinopatías afectan a millones de personas en todo el mundo. Estas afecciones, incluida la... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)
.jpg)