Los depósitos de tejido residual son adecuados para los análisis proteómicos usando la espectrometría de masas
|
Por el equipo editorial de LabMedica en español Actualizado el 18 Sep 2018 |

Imagen: El espectrómetro de masas cuadrupolo-orbitrap híbrido Q Exact (Fotografía cortesía de Thermo Fisher Scientific).
La proteómica basada en la espectrometría de masas se ha convertido en una poderosa herramienta para la identificación y cuantificación de proteínas de una amplia variedad de muestras biológicas.
La mayoría de los estudios que utilizan muestras de tejido se han realizado en muestras incrustadas congeladas frescas u óptimas de corte (OCT) recogidas de forma prospectiva. Sin embargo, este tipo de muestras son a menudo difíciles de obtener, tienen un suministro limitado, y la información clínica y los resultados en los pacientes se retrasan inherentemente en comparación con las muestras almacenadas.
Científicos del Laboratorio Nacional del Noroeste del Pacífico (Richland, WA, EUA) y sus colegas analizaron 60 muestras de pacientes tomadas de depósitos de tejido residual de Vigilancia, Epidemiología y Resultados Finales (SEER) del NCI, que contienen muestras de más de 100.000 pacientes con cáncer, junto con información demográfica detallada, datos sobre las características del tumor, el tratamiento, la supervivencia y la causa de la muerte. Las 60 muestras variaron en su tiempo de almacenamiento de siete a 32 años.
El equipo utilizó un etiquetado masivo en tándem (TMT, por su sigla en inglés) de 10 plex y dividió cada muestra en seis fracciones; cada una de ellas fue procesada en un gradiente de nanoLC de 100 minutos antes del análisis en un instrumento Q-Exact Plus (Thermo Fisher Scientific, Waltham , MA, EUA). Para el análisis de fosfopéptidos, usaron el enriquecimiento mediante Cromatografía de Afinidad de Metal Inmovilizado (IMAC). Encontraron que las 60 muestras proporcionaron suficiente material para el análisis de expresión proteica de todo el proteoma y 18 de las 60 muestras proporcionaron suficiente material para el trabajo de fosfopéptidos.
Los investigadores identificaron y cuantificaron un total de 8.582 proteínas y 8.073 fosfopéptidos en todo el conjunto de muestras SEER, lo que indica que el tejido FFPE es susceptible de análisis proteómico mediante espectrometría de masas. Se redujeron las identificaciones de proteínas en comparación con las identificaciones posibles en muestras incrustadas de compuestos de temperatura óptima de corte (OCT). En comparación con las muestras de OCT, las identificaciones de péptidos, proteínas y fosfopéptidos se redujeron en un 50%, 20% y 76%, respectivamente.
Karin D, Rodland, PhD, experta en espectrometría de masas y autora principal del estudio, dijo: “Ha habido kits comerciales disponibles durante 12 a 15 años para extraer proteínas de bloques FFPE y en vista de ello, los rendimientos de proteína cuando se usan los bloques de FFPE no son tan malos. Pero con las tecnologías de espectrometría de masas de hace 12 a 15 años, la tasa de identificación era muy baja. Simplemente no se obtenía una buena cobertura [proteoma] usando los bloques FFPE. Y la suposición era que la reticulación con formalina causaba la pérdida de identificaciones. Sin embargo, las mejoras en la tecnología en la espectrometría de masas han proporcionado instrumentos con mayor sensibilidad y mejor resolución que son capaces de trabajar con cantidades más pequeñas de muestra”. El estudio fue publicado el 3 de agosto de 2018 en la revista Clinical Proteomics.
Enlace relacionado:
Laboratorio Nacional del Noroeste del Pacífico
Thermo Fisher Scientific
La mayoría de los estudios que utilizan muestras de tejido se han realizado en muestras incrustadas congeladas frescas u óptimas de corte (OCT) recogidas de forma prospectiva. Sin embargo, este tipo de muestras son a menudo difíciles de obtener, tienen un suministro limitado, y la información clínica y los resultados en los pacientes se retrasan inherentemente en comparación con las muestras almacenadas.
Científicos del Laboratorio Nacional del Noroeste del Pacífico (Richland, WA, EUA) y sus colegas analizaron 60 muestras de pacientes tomadas de depósitos de tejido residual de Vigilancia, Epidemiología y Resultados Finales (SEER) del NCI, que contienen muestras de más de 100.000 pacientes con cáncer, junto con información demográfica detallada, datos sobre las características del tumor, el tratamiento, la supervivencia y la causa de la muerte. Las 60 muestras variaron en su tiempo de almacenamiento de siete a 32 años.
El equipo utilizó un etiquetado masivo en tándem (TMT, por su sigla en inglés) de 10 plex y dividió cada muestra en seis fracciones; cada una de ellas fue procesada en un gradiente de nanoLC de 100 minutos antes del análisis en un instrumento Q-Exact Plus (Thermo Fisher Scientific, Waltham , MA, EUA). Para el análisis de fosfopéptidos, usaron el enriquecimiento mediante Cromatografía de Afinidad de Metal Inmovilizado (IMAC). Encontraron que las 60 muestras proporcionaron suficiente material para el análisis de expresión proteica de todo el proteoma y 18 de las 60 muestras proporcionaron suficiente material para el trabajo de fosfopéptidos.
Los investigadores identificaron y cuantificaron un total de 8.582 proteínas y 8.073 fosfopéptidos en todo el conjunto de muestras SEER, lo que indica que el tejido FFPE es susceptible de análisis proteómico mediante espectrometría de masas. Se redujeron las identificaciones de proteínas en comparación con las identificaciones posibles en muestras incrustadas de compuestos de temperatura óptima de corte (OCT). En comparación con las muestras de OCT, las identificaciones de péptidos, proteínas y fosfopéptidos se redujeron en un 50%, 20% y 76%, respectivamente.
Karin D, Rodland, PhD, experta en espectrometría de masas y autora principal del estudio, dijo: “Ha habido kits comerciales disponibles durante 12 a 15 años para extraer proteínas de bloques FFPE y en vista de ello, los rendimientos de proteína cuando se usan los bloques de FFPE no son tan malos. Pero con las tecnologías de espectrometría de masas de hace 12 a 15 años, la tasa de identificación era muy baja. Simplemente no se obtenía una buena cobertura [proteoma] usando los bloques FFPE. Y la suposición era que la reticulación con formalina causaba la pérdida de identificaciones. Sin embargo, las mejoras en la tecnología en la espectrometría de masas han proporcionado instrumentos con mayor sensibilidad y mejor resolución que son capaces de trabajar con cantidades más pequeñas de muestra”. El estudio fue publicado el 3 de agosto de 2018 en la revista Clinical Proteomics.
Enlace relacionado:
Laboratorio Nacional del Noroeste del Pacífico
Thermo Fisher Scientific
Últimas Química Clínica noticias
- Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
- Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
- Nuevo método de análisis de sangre detecta opioides potentes en menos de tres minutos
- Kit inalámbrico de prueba de hepatitis B completa detección y recopilación de datos en un solo paso
- Dispositivo sensible, indoloro, de bajo costo y sin radiación detecta cáncer de mama en orina
- Prueba de saliva detecta cáncer de mama en cinco segundos
- Sensores electroquímicos con recubrimiento de próxima generación avanzan en diagnóstico de precisión POC
- Dispositivo portátil, primero de su tipo, detecta con precisión fentanilo en orina en segundos
- Nueva matriz de sensores fluorescentes ilumina proteínas relacionadas con el Alzheimer para detección más temprana
- Analizador clínico automatizado basado en espectrometría de masas podría transformar pruebas de laboratorio
- Sensor de pH altamente sensible ayuda a detectar cánceres y virus transmitidos por vectores
- Sensor no invasivo monitorea cambios en composiciones de saliva para diagnosticar diabetes rápidamente
- Innovadores Inmunoensayos ayudan en evaluación del riesgo de preeclampsia
- La AACC publica pautas completas para pruebas de diabetes
- Prueba de orina para monitorear cambios en marcadores de salud renal puede predecir insuficiencia cardíaca de nueva aparición
- Analizador compacto de inmunoensayo y química clínica ayuda a laboratorios bajo y medio volumen a abordar los desafíos
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Ensayo de PCR simple diferencia con precisión entre los subtipos de cáncer de pulmón de células pequeñas
El cáncer de pulmón de células pequeñas (CPCP), una neoplasia maligna neuroendocrina que progresa rápidamente, presenta bajas tasas de supervivencia. A pesar de su heterogeneidad molecular y clínica, el... Más
Enfoque revolucionario de análisis de células T permite detección temprana del cáncer
La biopsia líquida, un método para diagnosticar el cáncer mediante análisis de sangre de rutina, es una herramienta potencial importante para la detección temprana del... MásHematología
ver canal
Instrumento de próxima generación detecta trastornos de la hemoglobina en recién nacidos
Las hemoglobinopatías, las enfermedades hereditarias más extendidas a nivel mundial, afectan a alrededor del 7 % de la población como portadores, y el 2,7 % de los recién nacidos nacen con estas enfermedades.... Más
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Innovadora plataforma de diagnóstico proporciona resultados de AST con velocidad sin precedentes
Una plataforma de diagnóstico innovadora que ofrece resultados de pruebas de susceptibilidad a los antibióticos (AST) con una velocidad sin precedentes puede convertirse en una herramienta importante para... Más
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... MásPatología
ver canal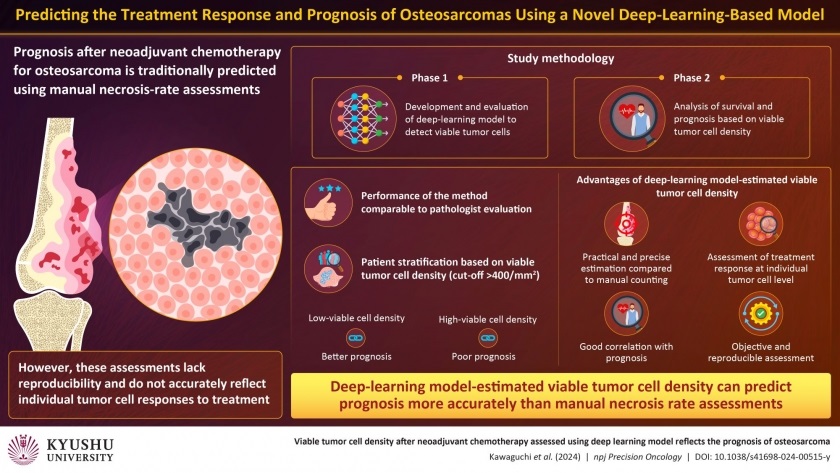
Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico... Más
Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
La comunidad médica mundial reconoce cada vez más que la biopsia líquida es un enfoque transformador para mejorar la atención al paciente con cáncer. Este innovador método de diagnóstico implica detectar... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)


.jpg)



