Prueba rápida nueva diagnostica simultáneamente la COVID-19 y predice el curso de la enfermedad
|
Por el equipo editorial de LabMedica en español Actualizado el 26 Jan 2022 |
Imagen: Nueva prueba rápida diagnostica simultáneamente la infección por COVID-19 y predice el curso de la enfermedad (Fotografía cortesía del Instituto Paul Scherrer/Mahir Dzambegovic)
Los investigadores han desarrollado una prueba rápida para la COVID-19 basada en un principio funcional novedoso, que promete resultados fiables y cuantificables sobre la enfermedad de un paciente y su curso.
La prueba desarrollada por investigadores del Instituto Paul Scherrer (PSI; Suiza) y la Universidad de Basilea (Basilea, Suiza), también puede proporcionar evidencia sobre otras enfermedades y variantes de COVID que pueden estar presentes. Sin embargo, antes de que pueda tener un uso generalizado, debe someterse a más pruebas y optimización.
Una de las principales deficiencias de las pruebas rápidas de antígenos es su falta de fiabilidad. Las pruebas solo dicen si el sujeto tiene la infección o no. No proporcionan ninguna información sobre el curso de la infección o la reacción inmunitaria de los pacientes. La nueva prueba desarrollada en PSI, que, a diferencia de las pruebas de antígenos, no detecta directamente los componentes del virus, sino los anticuerpos que produce el sistema inmunitario en respuesta a la infección, promete brindar un poder predictivo sustancialmente mayor que las pruebas rápidas. Es igual de económica, rápida y fácil de usar y también se puede utilizar para identificar simultáneamente una variedad de patógenos, como los responsables de la influenza.
El bloque de construcción central de la prueba es una pequeña placa rectangular de plexiglás común, similar a un portaobjetos de microscopio. Consta de una capa inferior de un milímetro de espesor y una capa superior de 0,2 milímetros de espesor. Los investigadores modelaron un relieve en la parte inferior utilizando litografía por haz de electrones, un proceso extremadamente preciso para moler materiales sólidos utilizados, por ejemplo, en la fabricación de chips de computadora. Una vez que se produjo la plantilla maestra de esta manera, los investigadores la combinaron con la llamada litografía de nanoimpresión, que acelera significativamente el proceso de fabricación y reduce su costo.
Con la capa más delgada de plexiglás como cubierta, la placa ahora tiene tres canales paralelos a través de los cuales puede fluir un líquido de un extremo al otro. Cada uno de estos tiene 300 micras (0,3 milímetros) de ancho y 3,4 micras de altura en la entrada. En la salida, los canales son cinco veces más anchos, pero de solo una micra de alto. A lo largo de un tramo intermedio, el canal se estrecha a unas pocas micras de ancho, y en un punto tiene solo 0,8 micras de alto, aproximadamente 100 veces más delgado que el cabello humano. Esto asegura un fuerte efecto capilar, como la acción familiar de los tejidos de conducción que transportan el agua desde las raíces hasta las copas de los árboles. No se requiere bomba. La fuerza resulta de la tensión interfacial entre el líquido y la superficie sólida. Prácticamente succiona el agua a través de los estrechos pasajes. Precisamente lo mismo sucede con los canales del plexiglás, excepto que, en lugar de agua, a través de él fluye una gota de sangre.
Lo que es crucial para la prueba es un pasaje en el que la altura del canal cae de 3,4 micras a 0,8. En lo que los investigadores llaman la región de captura, las partículas añadidas previamente a la sangre quedan atrapadas en lugares predefinidos, dependiendo de qué patógenos estén presentes en la sangre. Para la prueba, un paciente iría a un médico o a un centro de análisis. Allí, se toma una pequeña gota de sangre por punción digital, como en una prueba de azúcar en la sangre. Un líquido en el que se suspenden nanopartículas artificiales especiales se mezcla con la sangre. Su superficie tiene la misma estructura que las notorias proteínas Spike del virus SARS-CoV-2, a las que se acoplan los anticuerpos humanos cuando luchan contra la enfermedad.
Además, se agregan pequeñas partículas fluorescentes que se adhieren a los anticuerpos SARS-CoV-2 en humanos. Esto significa que si hay anticuerpos contra el SARS-CoV-2 en la sangre bajo análisis, las partículas fluorescentes primero se adhieren a ellos; juntos se unen a las estructuras similares a virus de las nanopartículas significativamente más grandes y se atascan, junto con ellas, en los lugares predefinidos correspondientes al diámetro de las nanopartículas. Aquí se acumulan las nanopartículas, con los anticuerpos humanos y sus apéndices brillantes acoplados a ellas. Si la placa se coloca bajo un microscopio de fluorescencia, la señal de luz es visible. Cuantos más anticuerpos haya formado el paciente, más brillante será; cuanto más clara sea la señal, más fuerte será la reacción inmunológica. Así es como se puede diagnosticar claramente la COVID-19. No hay riesgo de que el canal quede bloqueado por otras partículas en la sangre. Los virus en sí tienen solo alrededor de 0,12 micras de tamaño y fluyen sin resistencia. Solo los glóbulos rojos junto a las nanopartículas son más grandes que la parte más estrecha del canal.
La prueba abre aún más posibilidades más allá del diagnóstico de la COVID-19. Además, las nanopartículas de diferentes tamaños y con diferentes estructuras superficiales podrían mezclarse con la sangre para permitir la detección simultánea de otras enfermedades. En el estudio, los investigadores hicieron esto a través de partículas cuya superficie corresponde a virus de influenza A. En los experimentos, se iluminaron dos puntos en la región de captura: uno para la COVID-19 y otro para la influenza. Además, es posible identificar diferentes anticuerpos producidos por el sistema inmunitario en diferentes etapas de la enfermedad. Por ejemplo, se podrían usar partículas fluorescentes verdes que solo se adhieren a los anticuerpos que aparecen en la fase inicial de la infección y partículas fluorescentes rojas para los anticuerpos producidos por el sistema inmunitario en etapas posteriores. Además, la prueba debería ser aún más fácil de realizar.
“Trabajamos para que sea igual de fácil hacerlo con saliva en lugar de sangre”, dijo Thomas Mortelmans, candidato a doctorado en el Instituto Suizo de Nanociencia de la Universidad de Basilea y primer autor del estudio. “También queremos poder usar la cámara de un teléfono móvil en lugar de un microscopio para leer las señales. Los dispositivos modernos ahora son capaces de hacer esto”.
“Nuestra visión es una tecnología con la que podamos diagnosticar simultáneamente varias enfermedades y variantes de la COVID y la influenza de manera confiable, rápida y económica a través del teléfono móvil. Nuestro novedoso concepto es capaz de hacer esto realidad”, agregó Yasin Ekinci, jefe del Laboratorio. para Nanociencias y Tecnologías de rayos X en el PSI, quien fue responsable del proyecto para desarrollar la nueva prueba.
Enlace relacionado:
Instituto Paul Scherrer
Universidad de Basilea
La prueba desarrollada por investigadores del Instituto Paul Scherrer (PSI; Suiza) y la Universidad de Basilea (Basilea, Suiza), también puede proporcionar evidencia sobre otras enfermedades y variantes de COVID que pueden estar presentes. Sin embargo, antes de que pueda tener un uso generalizado, debe someterse a más pruebas y optimización.
Una de las principales deficiencias de las pruebas rápidas de antígenos es su falta de fiabilidad. Las pruebas solo dicen si el sujeto tiene la infección o no. No proporcionan ninguna información sobre el curso de la infección o la reacción inmunitaria de los pacientes. La nueva prueba desarrollada en PSI, que, a diferencia de las pruebas de antígenos, no detecta directamente los componentes del virus, sino los anticuerpos que produce el sistema inmunitario en respuesta a la infección, promete brindar un poder predictivo sustancialmente mayor que las pruebas rápidas. Es igual de económica, rápida y fácil de usar y también se puede utilizar para identificar simultáneamente una variedad de patógenos, como los responsables de la influenza.
El bloque de construcción central de la prueba es una pequeña placa rectangular de plexiglás común, similar a un portaobjetos de microscopio. Consta de una capa inferior de un milímetro de espesor y una capa superior de 0,2 milímetros de espesor. Los investigadores modelaron un relieve en la parte inferior utilizando litografía por haz de electrones, un proceso extremadamente preciso para moler materiales sólidos utilizados, por ejemplo, en la fabricación de chips de computadora. Una vez que se produjo la plantilla maestra de esta manera, los investigadores la combinaron con la llamada litografía de nanoimpresión, que acelera significativamente el proceso de fabricación y reduce su costo.
Con la capa más delgada de plexiglás como cubierta, la placa ahora tiene tres canales paralelos a través de los cuales puede fluir un líquido de un extremo al otro. Cada uno de estos tiene 300 micras (0,3 milímetros) de ancho y 3,4 micras de altura en la entrada. En la salida, los canales son cinco veces más anchos, pero de solo una micra de alto. A lo largo de un tramo intermedio, el canal se estrecha a unas pocas micras de ancho, y en un punto tiene solo 0,8 micras de alto, aproximadamente 100 veces más delgado que el cabello humano. Esto asegura un fuerte efecto capilar, como la acción familiar de los tejidos de conducción que transportan el agua desde las raíces hasta las copas de los árboles. No se requiere bomba. La fuerza resulta de la tensión interfacial entre el líquido y la superficie sólida. Prácticamente succiona el agua a través de los estrechos pasajes. Precisamente lo mismo sucede con los canales del plexiglás, excepto que, en lugar de agua, a través de él fluye una gota de sangre.
Lo que es crucial para la prueba es un pasaje en el que la altura del canal cae de 3,4 micras a 0,8. En lo que los investigadores llaman la región de captura, las partículas añadidas previamente a la sangre quedan atrapadas en lugares predefinidos, dependiendo de qué patógenos estén presentes en la sangre. Para la prueba, un paciente iría a un médico o a un centro de análisis. Allí, se toma una pequeña gota de sangre por punción digital, como en una prueba de azúcar en la sangre. Un líquido en el que se suspenden nanopartículas artificiales especiales se mezcla con la sangre. Su superficie tiene la misma estructura que las notorias proteínas Spike del virus SARS-CoV-2, a las que se acoplan los anticuerpos humanos cuando luchan contra la enfermedad.
Además, se agregan pequeñas partículas fluorescentes que se adhieren a los anticuerpos SARS-CoV-2 en humanos. Esto significa que si hay anticuerpos contra el SARS-CoV-2 en la sangre bajo análisis, las partículas fluorescentes primero se adhieren a ellos; juntos se unen a las estructuras similares a virus de las nanopartículas significativamente más grandes y se atascan, junto con ellas, en los lugares predefinidos correspondientes al diámetro de las nanopartículas. Aquí se acumulan las nanopartículas, con los anticuerpos humanos y sus apéndices brillantes acoplados a ellas. Si la placa se coloca bajo un microscopio de fluorescencia, la señal de luz es visible. Cuantos más anticuerpos haya formado el paciente, más brillante será; cuanto más clara sea la señal, más fuerte será la reacción inmunológica. Así es como se puede diagnosticar claramente la COVID-19. No hay riesgo de que el canal quede bloqueado por otras partículas en la sangre. Los virus en sí tienen solo alrededor de 0,12 micras de tamaño y fluyen sin resistencia. Solo los glóbulos rojos junto a las nanopartículas son más grandes que la parte más estrecha del canal.
La prueba abre aún más posibilidades más allá del diagnóstico de la COVID-19. Además, las nanopartículas de diferentes tamaños y con diferentes estructuras superficiales podrían mezclarse con la sangre para permitir la detección simultánea de otras enfermedades. En el estudio, los investigadores hicieron esto a través de partículas cuya superficie corresponde a virus de influenza A. En los experimentos, se iluminaron dos puntos en la región de captura: uno para la COVID-19 y otro para la influenza. Además, es posible identificar diferentes anticuerpos producidos por el sistema inmunitario en diferentes etapas de la enfermedad. Por ejemplo, se podrían usar partículas fluorescentes verdes que solo se adhieren a los anticuerpos que aparecen en la fase inicial de la infección y partículas fluorescentes rojas para los anticuerpos producidos por el sistema inmunitario en etapas posteriores. Además, la prueba debería ser aún más fácil de realizar.
“Trabajamos para que sea igual de fácil hacerlo con saliva en lugar de sangre”, dijo Thomas Mortelmans, candidato a doctorado en el Instituto Suizo de Nanociencia de la Universidad de Basilea y primer autor del estudio. “También queremos poder usar la cámara de un teléfono móvil en lugar de un microscopio para leer las señales. Los dispositivos modernos ahora son capaces de hacer esto”.
“Nuestra visión es una tecnología con la que podamos diagnosticar simultáneamente varias enfermedades y variantes de la COVID y la influenza de manera confiable, rápida y económica a través del teléfono móvil. Nuestro novedoso concepto es capaz de hacer esto realidad”, agregó Yasin Ekinci, jefe del Laboratorio. para Nanociencias y Tecnologías de rayos X en el PSI, quien fue responsable del proyecto para desarrollar la nueva prueba.
Enlace relacionado:
Instituto Paul Scherrer
Universidad de Basilea
Últimas COVID-19 noticias
- Inmunosensor nuevo allana el camino para pruebas rápidas POC para COVID-19 y enfermedades infecciosas emergentes
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Prueba nueva COVID + Influenza + VSR ayudará a estar preparados para la ‘tripledemia’
- IA elimina las conjeturas de las pruebas de flujo lateral
- Prueba de antígeno del SARS-CoV-2 más rápida, jamás diseñada, permite realizar pruebas de COVID-19 no invasivas en cualquier entorno
- Pruebas rápidas de antígeno detectan las variantes ómicron, delta del SARS-CoV-2
- Prueba en sangre realizada durante la infección inicial predice el riesgo de COVID prolongada
- Investigadores afirman que hay que crear “reservistas” de laboratorio para responder más rápidamente a la próxima pandemia
- Estudio encuentra que los profesionales sanitarios mostraron mayor interés en tecnologías POC durante la pandemia
- Plataforma de análisis de bajo costo para la COVID-19 combina sensibilidad de la PCR y velocidad de pruebas de antígeno
- Prueba de sangre por punción digital identifica inmunidad a la COVID-19
- Kit de prueba rápida determina inmunidad contra la COVID-19 y sus variantes
Canales
Química Clínica
ver canal
Herramienta química a nanoescala 'brillantemente luminosa' mejora detección de enfermedades
Miles de moléculas brillantes disponibles comercialmente, conocidas como fluoróforos, se utilizan comúnmente en imágenes médicas, detección de enfermedades, marcado... Más
Prueba de detección portátil económica transforma detección de enfermedades renales
Millones de personas padecen enfermedad renal, que a menudo permanece sin diagnosticar hasta que alcanza una etapa crítica. Esta epidemia silenciosa no solo disminuye la calidad de vida de los afectados,... MásDiagnóstico Molecular
ver canal
Nueva herramienta genética analiza sangre del cordón umbilical para predecir enfermedades
Los niños experimentan problemas metabólicos a edades cada vez más tempranas, lo que los expone a un mayor riesgo de sufrir graves problemas de salud en el futuro. Existe una creciente... Más
Biomarcador del líquido cefalorraquídeo para enfermedad de Parkinson ofrece diagnóstico temprano y preciso
La enfermedad de Parkinson es una enfermedad neurodegenerativa que suele diagnosticarse en una etapa avanzada basándose en síntomas clínicos, principalmente trastornos motores.... MásHematología
ver canal
Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
La citopenia clonal de significado incierto (CCSI) es un trastorno sanguíneo común en adultos mayores, caracterizado por mutaciones en las células sanguíneas y un recuento ... Más
Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
En los Estados Unidos, aproximadamente el 15 % de las embarazadas son RhD negativas. Sin embargo, en aproximadamente el 40 % de estos casos, el feto también es RhD negativo, lo que hace innecesaria la... MásInmunología
ver canal
Prueba de células madre predice resultado del tratamiento en cáncer de ovario resistente al platino
El cáncer de ovario epitelial suele responder inicialmente a la quimioterapia, pero con el tiempo, el tumor desarrolla resistencia a la terapia, lo que provoca su recrecimiento. Esta resistencia... Más
Análisis de sangre con aprendizaje automático predice respuesta a inmunoterapia en pacientes con linfoma
La terapia de células T con receptores de antígenos quiméricos (CAR) se ha convertido en uno de los avances recientes más prometedores en el tratamiento de los cánceres... MásMicrobiología
ver canal
Dispositivo portátil ofrece resultados de tuberculosis económico y rápido
La tuberculosis (TB) sigue siendo la enfermedad infecciosa más mortal a nivel mundial, afectando a aproximadamente 10 millones de personas al año. En 2021, alrededor de 4,2 millones de casos... Más
Método basado en IA mejora diagnóstico de infecciones resistentes a fármacos
Las infecciones resistentes a los medicamentos, en particular las causadas por bacterias mortales como la tuberculosis y el estafilococo, se están convirtiendo rápidamente en una emergencia... MásPatología
ver canal
Kits de ensayo de enzima DUB sensibles y específicos requieren configuración mínima sin preparación del sustrato
La ubiquitinación y la desubiquitinación son dos procesos fisiológicos importantes en el sistema ubiquitina-proteasoma, responsable de la degradación de proteínas en... Más
Primer modelo de IA para diagnóstico de cáncer de tiroides con precisión superior al 90 %
El cáncer de tiroides es uno de los cánceres más comunes en todo el mundo, y su manejo preciso generalmente se basa en dos sistemas principales: (1) la 8va edición del Comité... MásTecnología
ver canal
Tecnología de microchip desechable podría detectar selectivamente VIH en muestras de sangre completa
A finales de 2023, aproximadamente 40 millones de personas en todo el mundo vivían con VIH, y alrededor de 630.000 personas murieron por enfermedades relacionadas con el sida ese mismo año.... Más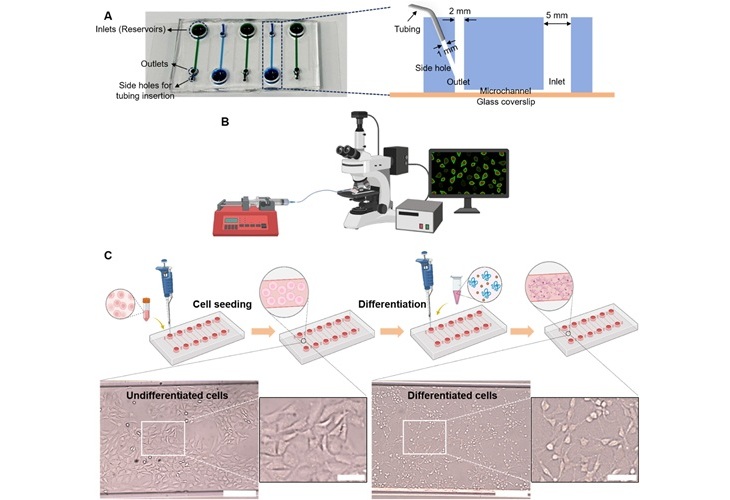
Dispositivo microfluídico Dolor en un Chip determina tipos de dolor crónico desde muestras de sangre
El dolor crónico es una afección generalizada que sigue siendo difícil de controlar, y los métodos clínicos existentes para su tratamiento se basan en gran medida en... MásIndustria
ver canal
Cepheid y Oxford Nanopore se unen para desarrollar soluciones con secuenciación automatizada
Cepheid (Sunnyvale, CA, EUA), una empresa líder en diagnóstico molecular, y Oxford Nanopore Technologies (Oxford, Reino Unido), la empresa detrás de una nueva generación de... Más