Secuenciación genómica identifica la enfermedad precursora del mieloma con riesgo de progresión
|
Por el equipo editorial de LabMedica en español Actualizado el 08 Jun 2021 |

Imagen: El clasificador BD FACSAria III está equipado con cinco láseres, 17 canales de fluorescencia y dos canales para dispersión frontal y dispersión lateral (Fotografía cortesía de BD Biosciences)
El mieloma múltiple (MM) es la segunda neoplasia maligna hematológica más común y está constantemente precedida por la expansión asintomática de las células plasmáticas clonales, denominada gammapatía monoclonal de significado indeterminado (MGUS) o mieloma latente (SMM).
Estas dos condiciones precursoras se encuentran en el 2% -3% de la población general mayor de 40 años. Solo una pequeña fracción de MGUS finalmente progresará a MM, mientras que ~ 60% de las personas con SMM progresará dentro de los 10 años posteriores al diagnóstico inicial. Actualmente, la diferenciación entre MGUS y SMM se basa en medidas indirectas y marcadores sustitutos de carga de enfermedad.
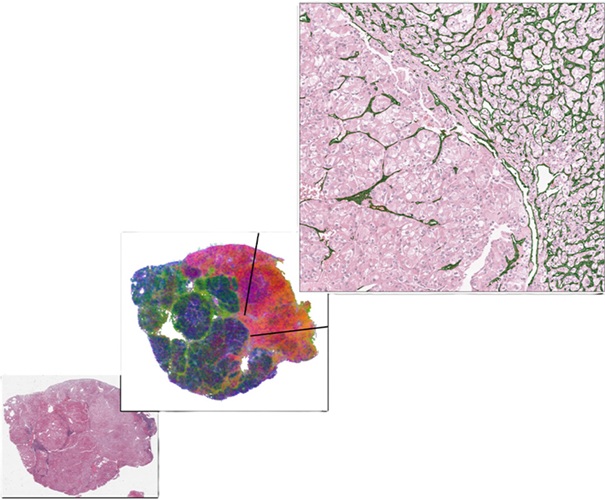
Los hematólogos y oncólogos del Centro de Cáncer Memorial Sloan Kettering (Nueva York, NY, EUA) y sus colegas, interrogaron los datos de la secuencia del genoma de 80 casos de mieloma múltiple, 18 MGUS y 14 SMM, incluido un solo caso de SMM clasificado como de alto riesgo según un modelo de pronóstico disponible. El equipo comparó las características del genoma en 17 casos precursores que progresaron a mieloma múltiple en dos años y 15 casos precursores estables, descubriendo un conjunto de “eventos genómicos que definen el mieloma” que incluían cromotripsis, aneuploidía, mutaciones del gen conductor, enzima de edición de ARNm de apolipoproteína B, perfiles, mutacionales de tipo polipéptido catalítico (APOBEC) e inserciones en plantilla.
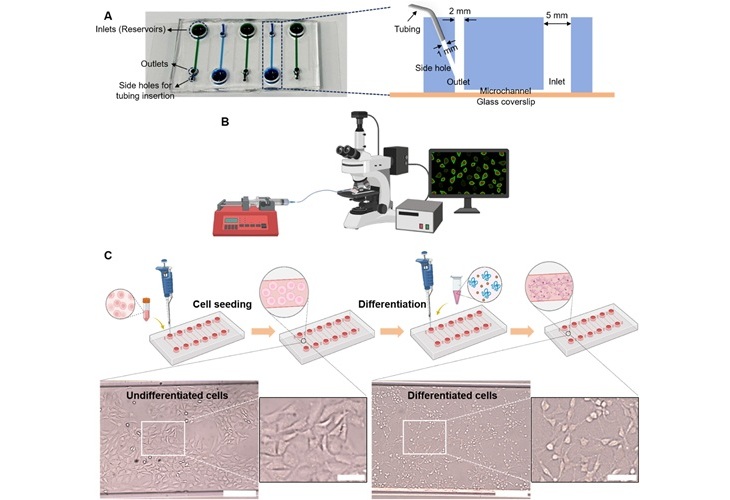
Para todas las muestras, se aislaron células plasmáticas de médula ósea (BMPC) de aspirados de médula ósea y se clasificaron en un instrumento BD FACSAria III (BD Biosciences, San José, CA, EUA). Para el ADN de control emparejado de cada paciente, se utilizaron células T de médula ósea o células mononucleares de sangre periférica. Las células T se aislaron de los aspirados de MO y se clasificaron también usando BD FACSAria III. La secuenciación estándar de entrada del genoma completo se ejecutó en un NovaSeq 6000 en una ejecución de extremos emparejados de 150 pb/150 pb (Illumina, San Diego, CA, EUA).
Los científicos informaron que los casos clínicamente estables de MGUS y SMM se caracterizan por un panorama genómico diferente y por diferencias en la adquisición temporal de eventos genómicos que definen el mieloma en comparación con las entidades progresivas. Por el contrario, informaron los investigadores, el conjunto más clínicamente estable de gammapatías precursoras carecía de tales alteraciones. También tendieron a aparecer en individuos diagnosticados con GMSI o SMM algo más tarde en la vida (entre alrededor de 28 y 65 años), en comparación con las condiciones precursoras en aquellos con enfermedad progresiva, que fueron diagnosticados entre las edades de cinco y 46 años.
Los autores concluyeron que, a pesar de su tamaño de muestra limitado, su estudio proporciona una prueba de principio de que la secuenciación del genoma completo (WGS) tiene el potencial de diferenciar con exactitud las condiciones precursoras estables y progresivas en estados clínicos de baja carga de enfermedad. La aplicación de esta tecnología en la clínica tiene el potencial de alterar significativamente el manejo de pacientes individuales, pero requerirá confirmación en estudios más amplios. El estudio fue publicado el 25 de marzo de 2021 en la revista Nature Communications.
Enlace relacionado:
Centro de Cáncer Memorial Sloan Kettering
Illumina
Estas dos condiciones precursoras se encuentran en el 2% -3% de la población general mayor de 40 años. Solo una pequeña fracción de MGUS finalmente progresará a MM, mientras que ~ 60% de las personas con SMM progresará dentro de los 10 años posteriores al diagnóstico inicial. Actualmente, la diferenciación entre MGUS y SMM se basa en medidas indirectas y marcadores sustitutos de carga de enfermedad.
Los hematólogos y oncólogos del Centro de Cáncer Memorial Sloan Kettering (Nueva York, NY, EUA) y sus colegas, interrogaron los datos de la secuencia del genoma de 80 casos de mieloma múltiple, 18 MGUS y 14 SMM, incluido un solo caso de SMM clasificado como de alto riesgo según un modelo de pronóstico disponible. El equipo comparó las características del genoma en 17 casos precursores que progresaron a mieloma múltiple en dos años y 15 casos precursores estables, descubriendo un conjunto de “eventos genómicos que definen el mieloma” que incluían cromotripsis, aneuploidía, mutaciones del gen conductor, enzima de edición de ARNm de apolipoproteína B, perfiles, mutacionales de tipo polipéptido catalítico (APOBEC) e inserciones en plantilla.
Para todas las muestras, se aislaron células plasmáticas de médula ósea (BMPC) de aspirados de médula ósea y se clasificaron en un instrumento BD FACSAria III (BD Biosciences, San José, CA, EUA). Para el ADN de control emparejado de cada paciente, se utilizaron células T de médula ósea o células mononucleares de sangre periférica. Las células T se aislaron de los aspirados de MO y se clasificaron también usando BD FACSAria III. La secuenciación estándar de entrada del genoma completo se ejecutó en un NovaSeq 6000 en una ejecución de extremos emparejados de 150 pb/150 pb (Illumina, San Diego, CA, EUA).
Los científicos informaron que los casos clínicamente estables de MGUS y SMM se caracterizan por un panorama genómico diferente y por diferencias en la adquisición temporal de eventos genómicos que definen el mieloma en comparación con las entidades progresivas. Por el contrario, informaron los investigadores, el conjunto más clínicamente estable de gammapatías precursoras carecía de tales alteraciones. También tendieron a aparecer en individuos diagnosticados con GMSI o SMM algo más tarde en la vida (entre alrededor de 28 y 65 años), en comparación con las condiciones precursoras en aquellos con enfermedad progresiva, que fueron diagnosticados entre las edades de cinco y 46 años.
Los autores concluyeron que, a pesar de su tamaño de muestra limitado, su estudio proporciona una prueba de principio de que la secuenciación del genoma completo (WGS) tiene el potencial de diferenciar con exactitud las condiciones precursoras estables y progresivas en estados clínicos de baja carga de enfermedad. La aplicación de esta tecnología en la clínica tiene el potencial de alterar significativamente el manejo de pacientes individuales, pero requerirá confirmación en estudios más amplios. El estudio fue publicado el 25 de marzo de 2021 en la revista Nature Communications.
Enlace relacionado:
Centro de Cáncer Memorial Sloan Kettering
Illumina
Últimas Hematología noticias
- Primera prueba de monitorización de heparina POC proporciona resultados rápidos

- Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
- Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
- Recuento de leucocitos predice gravedad de síntomas de COVID-19
- Tecnología de recuento de plaquetas ayudará a prevenir errores de diagnóstico
- Sistema de hemostasia POC podría prevenir muertes maternas
- Nueva prueba evalúa capacidad de los glóbulos rojos para transportar oxígeno midiendo su forma
- Pruebas de hemograma completo personalizadas ayudarían a diagnosticar enfermedades en etapa temprana
- Prueba no invasiva determina estado RhD fetal a partir del plasma materno
- Tecnología de teléfonos inteligentes mide de forma no invasiva niveles de hemoglobina en sangre en POC

- Sistema de diagnóstico de hemograma completo y sepsis busca resultados más rápidos, tempranos y fáciles
- Nuevo grupo sanguíneo descubierto ayudará a identificar y tratar a pacientes
- Puntuación de plaquetas sanguíneas detecta el riesgo de ataque cardíaco y accidente cerebrovascular
- Sistema automatizado de sobremesa lleva pruebas de sangre a cualquier persona, en cualquier lugar
- Nuevos analizadores de hematología ofrecen resultados combinados de VSG y CBC/DIFF en 60 segundos
- Instrumento de próxima generación detecta trastornos de la hemoglobina en recién nacidos
Canales
Química Clínica
ver canal
Análisis de sangre con IA detecta cáncer de ovario
El cáncer de ovario se ubica como la quinta causa principal de muerte por cáncer en mujeres, debido principalmente a diagnósticos en etapas tardías. Si bien más del 90... Más
Ensayo automatizado y descentralizado de NGS deADNlc identifica alteraciones en tumores sólidos avanzados
Los análisis actuales de ADN libre circulante (ADNlc) suelen estar centralizados, lo que requiere un manejo y transporte especializados de las muestras. La introducción de un sistema de ... MásDiagnóstico Molecular
ver canal
Innovadora prueba de diagnóstico molecular señala con precisión principal causa genética de EPOC
La enfermedad pulmonar obstructiva crónica (EPOC) y la deficiencia de alfa-1 antitripsina (DAAT) son afecciones que pueden causar dificultades respiratorias, pero difieren en su origen y herencia.... Más
Prueba diagnóstica de sangre detecta espondiloartritis axial
La espondiloartritis axial (EspAax) es una enfermedad autoinmune inflamatoria crónica que suele afectar a las personas durante sus años más productivos, y cuyos síntomas suelen manifestarse antes de los 45 años.... MásInmunología
ver canal
Prueba de células madre predice resultado del tratamiento en cáncer de ovario resistente al platino
El cáncer de ovario epitelial suele responder inicialmente a la quimioterapia, pero con el tiempo, el tumor desarrolla resistencia a la terapia, lo que provoca su recrecimiento. Esta resistencia... Más
Análisis de sangre con aprendizaje automático predice respuesta a inmunoterapia en pacientes con linfoma
La terapia de células T con receptores de antígenos quiméricos (CAR) se ha convertido en uno de los avances recientes más prometedores en el tratamiento de los cánceres... MásMicrobiología
ver canal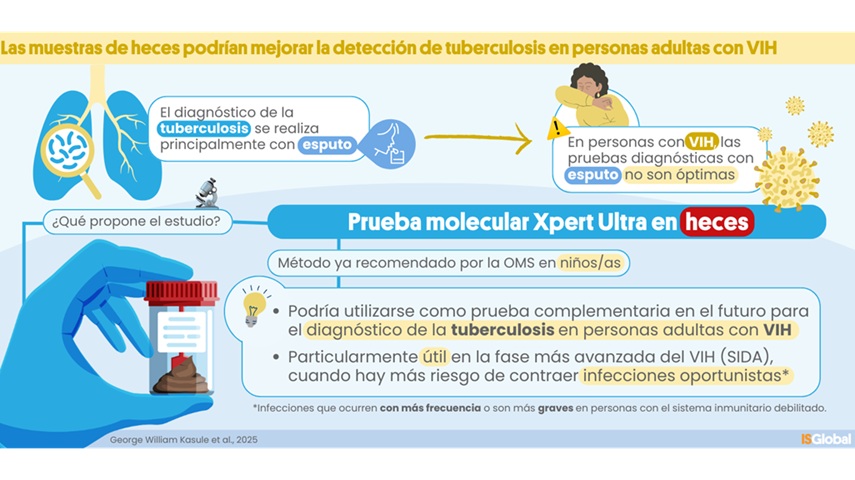
Prueba molecular de heces muestra potencial para diagnosticar tuberculosis en adultos con VIH
La tuberculosis (TB), causada por la bacteria Mycobacterium tuberculosis, provocó 1,25 millones de muertes en 2023, de las cuales el 13 % se produjeron en personas con VIH. El principal método... Más
Nueva prueba diagnostica meningitis bacteriana con rapidez y precisión
La meningitis bacteriana es una afección potencialmente mortal: uno de cada seis pacientes fallece y la mitad de los supervivientes experimentan síntomas persistentes. Por lo tanto, un d... MásPatología
ver canal
Innovador algoritmo de triaje del dolor torácico transforma la atención cardíaca
Las enfermedades cardiovasculares son responsables de un tercio de las muertes en todo el mundo, y el dolor torácico es la segunda causa más común de visitas a urgencias.... Más
Enfoque de biopsia líquida basado en IA revolucionará detección del cáncer cerebral
Detectar cánceres cerebrales sigue siendo extremadamente difícil, ya que muchos pacientes solo reciben un diagnóstico en etapas avanzadas, tras la aparición de síntomas... MásTecnología
ver canal
Algoritmos predictivos avanzados identifican pacientes con cáncer no diagnosticado
Dos algoritmos predictivos avanzados recientemente desarrollados aprovechan el estado de salud de una persona y los resultados de análisis de sangre básicos para predecir con precisión... Más
Algoritmo de firma de luz permite diagnósticos médicos más rápidos y precisos
Cada material o molécula interactúa con la luz de forma única, creando un patrón distintivo, similar a una huella dactilar. La espectroscopia óptica, que consiste en... MásIndustria
ver canal
Cepheid y Oxford Nanopore se unen para desarrollar soluciones con secuenciación automatizada
Cepheid (Sunnyvale, CA, EUA), una empresa líder en diagnóstico molecular, y Oxford Nanopore Technologies (Oxford, Reino Unido), la empresa detrás de una nueva generación de... Más