Soluciones de YHLO para la detección de anticuerpos antifosfolípidos podría ayudar a prevenir los coágulos sanguíneos potencialmente mortales en la COVID-19
|
Por el equipo editorial de LabMedica en español Actualizado el 22 Apr 2021 |
Ilustración
Shenzhen YHLO Biotech Co., Ltd. (Shenzhen, China) ofrece una gama de soluciones para la detección de anticuerpos antifosfolípidos (aPL), que podrían ayudar a prevenir coágulos sanguíneos potencialmente mortales en la COVID-19.
Se ha descubierto que la trombosis es una de las complicaciones más frecuentes en pacientes con enfermedad grave por coronavirus 2019 (COVID-19). Los estudios de los Países Bajos y Francia sugieren que los coágulos sanguíneos surgen en un 20-30% de los pacientes con COVID-19 con enfermedades críticas. La coagulación de la sangre es peligrosa ya que puede causar un déficit de oxígeno en la sangre y provocar la muerte celular en las partes obstruidas del cuerpo, contribuyendo a la alta mortalidad de la COVID-19. La evidencia acumulada apoya la hipótesis de que los anticuerpos aPL podrían ser responsables de los coágulos de sangre en los pacientes con COVID-19, al menos hasta cierto punto.
Los aPL son autoanticuerpos dirigidos contra las proteínas de unión a fosfolípidos en la membrana de las células, especialmente las células epiteliales en las paredes internas de los vasos sanguíneos. La activación de los aPL causa trombosis en los enfoques clásicos: el estrechamiento de los vasos sanguíneos a través de la acumulación de placa en las paredes de los vasos y la agregación plaquetaria. Las manifestaciones clínicas que incluyen coágulos de sangre en las piernas y abortos espontáneos repetidos debido a la presencia y activación de los aPL se denominan síndrome antifosfolípido (SAF). Se sospecha razonablemente que el coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) activa los desencadenante e induce una trombosis similar a la del SAF. Los aPL asociados al SAF más reconocidos son los anticuerpos anticardiolipina (aCL, que incluyen IgG, IgM e IgA) y los anticuerpos anti-β2-glicoproteína I (aβ2GPI, que incluyen IgG, IgM e IgA). Según el consenso de expertos internacionales, 12 semanas de presencia persistente de niveles altos de aCL IgG, aCL IgM, aβ2GPI o/y aβ2GPI IgM, junto con trombosis vascular sugieren un diagnóstico definitivo de SAF.
La trombosis de COVID-19 no solo comparte manifestaciones clínicas similares con el SAF, lo que es más importante, se han encontrado anticuerpos aPL en aproximadamente el 50% de los pacientes hospitalizados con COIVD-19. Según un estudio de la Universidad de Michigan, entre 172 pacientes hospitalizados con COVID-19, el 23% eran positivos para aCL IgM y el 52% eran positivos para cualquier anticuerpo aPL. Sin embargo, un estudio anterior del Hospital del Colegio Médico de la Unión de Pekín (PUMCH) había encontrado que los aβ2GPI IgA (28,8%) y los aCL IgA (25,8%) eran las primeras y segundas proporciones más altas de anticuerpos aPL individuales presentes en 66 pacientes con COVID-19 en estado crítico (admitidos en la UCI). Los resultados de la investigación de variantes se podrían deber a las diferencias en la gravedad de las condiciones de la COVID-19 y la heterogeneidad inherente de los anticuerpos aPL entre los individuos.
Otros estudios han revelado la asociación entre los niveles de concentración de anticuerpos aPL y la predisposición a eventos trombóticos en pacientes con COVID-19. Investigadores de la Universidad de Michigan inyectaron modelos de ratones con IgG purificada de siete sueros de pacientes con COVID-19 y un suero de pacientes con SAF catastrófico (CSAF). Los trombos en ratones tratados con anticuerpos aPL de alto nivel o sueros CSAF se encontraron entonces significativamente mayores que los de los ratones tratados con anticuerpos aPL de bajo nivel. Mediante el análisis de las correlaciones entre las manifestaciones clínicas y los perfiles de anticuerpos aPL y los niveles de concentración, el equipo de investigación de PUMCH también demostró que ser positivo para múltiples anticuerpos aPL o tener títulos de anticuerpos aPL de moderados a altos es más útil para predecir la posibilidad de eventos trombóticos en los pacientes con COVID-19 que ser positivo para un solo anticuerpo aPL o tener niveles de concentración bajos. En las conclusiones, los autores de ambos artículos sugieren un cribado amplio de anticuerpos aPL en todos los pacientes con COVID-19 para mejorar la estratificación del riesgo.
La persistencia de anticuerpos aPL en los pacientes con COVID-19 es otra gran preocupación para científicos y médicos relevantes. Aunque se cree que la mayoría de los anticuerpos aPL asociados a virus son transitorios, una revisión reciente de 163 casos publicados de anticuerpos aPL asociados a virus encontró eventos trombóticos en 116 casos, lo que sugiere que los anticuerpos aPL transitorios también pueden tener potencial protrombótico. Además, en la investigación mencionada anteriormente en PUMCH, los investigadores indagaron sobre los cambios dinámicos de los anticuerpos aPL en seis pacientes COVID-19 y encontraron la persistencia de anticuerpos aPL en cuatro de los pacientes al menos dentro de los 47 días posteriores al inicio de la enfermedad, entre los cuales un paciente mostró persistencia de aβ2GPI IgG en el día 80 posterior al inicio de la enfermedad a pesar de las intervenciones con recambio plasmático, y otro paciente mantuvo niveles altos de anticuerpos múltiples aPL durante aproximadamente dos semanas. Solo en dos pacientes los anticuerpos aPL desaparecieron en 47 días. Estos resultados sugieren que los niveles de anticuerpos aPL fluctúan y exhiben diferentes patrones dinámicos entre diferentes pacientes con COVID-19. Para algunos pacientes, los anticuerpos aPL pueden persistir más tiempo y requieren detecciones de monitoreo adicionales. Para ayudar a guiar la toma de decisiones médicas, se recomienda que los pacientes se vuelvan a realizar la prueba de anticuerpos aPL al menos una vez, después de 12 semanas si la serie inicial de pruebas de anticuerpos aPL fue positiva.
A pesar de la disputa sobre qué anticuerpos aPL son más prevalentes en pacientes con COVID-19, los investigadores de la Universidad de Michigan y PUMCH coinciden en la alta prevalencia de anticuerpos aPL en pacientes con afecciones graves de COVID-19 y la presencia de anticuerpos aPL contribuye a las formaciones de coágulos de sangre. Se especula que la detección de anticuerpos aPL es un posible enfoque para prevenir los coágulos sanguíneos en pacientes con COVID-19 y mejorar la estratificación del riesgo y la personalización del tratamiento. Teniendo en cuenta la posibilidad de una exacerbación del SAF causada por la infección por SARS-CoV-2, es hora de aumentar nuestra conciencia sobre la atención médica de los pacientes con SAF y las detecciones de estos anticuerpos. En comparación con la población general, los pacientes persistentemente positivos para anticuerpos aPL tienen un mayor riesgo de coágulos de sangre durante la hospitalización. Por lo tanto, en caso de hospitalización relacionada con COVID-19, es importante que los pacientes persistentemente positivos para anticuerpos aPL discutan las estrategias de prevención de coágulos de sangre con sus médicos. Los pacientes con SAF deben seguir todas las precauciones estándar, incluido el distanciamiento social, usar máscaras al aire libre, lavarse las manos con frecuencia y evitar el contacto con personas enfermas para prevenir la COVID-19.
Las soluciones de YHLO para la detección de anticuerpos aPL que podrían ayudar a prevenir coágulos sanguíneos potencialmente mortales en la COVID-19 incluyen pruebas para la detección de Cardiolipina IgG, Cardiolipina IgM, Cardiolipina IgA, Anti-Cardiolipina, β2-Glicoproteína I IgG, β2- Glicoproteína I IgA, β2-Glicoproteína I IgM y Anti-β2-Glicoproteína I. Las pruebas de detección relacionadas con el SARS-CoV-2 de YHLO incluyen iFlash-2019-nCoV Ag, iFlash-2019-nCoV Nab, iFlash-2019-nCoV IgG, iFlash- 2019-nCoV IgM e iFlash-2019-nCoV IgA. YHLO también ofrece pruebas para la detección de otras infecciones como Anti-TP, Anti-VHC, HBsAg, Anti-HBs, HBeAg, Anti-HBe, Anti-HBc y HIV Combo.
Enlace relacionado:
Se ha descubierto que la trombosis es una de las complicaciones más frecuentes en pacientes con enfermedad grave por coronavirus 2019 (COVID-19). Los estudios de los Países Bajos y Francia sugieren que los coágulos sanguíneos surgen en un 20-30% de los pacientes con COVID-19 con enfermedades críticas. La coagulación de la sangre es peligrosa ya que puede causar un déficit de oxígeno en la sangre y provocar la muerte celular en las partes obstruidas del cuerpo, contribuyendo a la alta mortalidad de la COVID-19. La evidencia acumulada apoya la hipótesis de que los anticuerpos aPL podrían ser responsables de los coágulos de sangre en los pacientes con COVID-19, al menos hasta cierto punto.
Los aPL son autoanticuerpos dirigidos contra las proteínas de unión a fosfolípidos en la membrana de las células, especialmente las células epiteliales en las paredes internas de los vasos sanguíneos. La activación de los aPL causa trombosis en los enfoques clásicos: el estrechamiento de los vasos sanguíneos a través de la acumulación de placa en las paredes de los vasos y la agregación plaquetaria. Las manifestaciones clínicas que incluyen coágulos de sangre en las piernas y abortos espontáneos repetidos debido a la presencia y activación de los aPL se denominan síndrome antifosfolípido (SAF). Se sospecha razonablemente que el coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) activa los desencadenante e induce una trombosis similar a la del SAF. Los aPL asociados al SAF más reconocidos son los anticuerpos anticardiolipina (aCL, que incluyen IgG, IgM e IgA) y los anticuerpos anti-β2-glicoproteína I (aβ2GPI, que incluyen IgG, IgM e IgA). Según el consenso de expertos internacionales, 12 semanas de presencia persistente de niveles altos de aCL IgG, aCL IgM, aβ2GPI o/y aβ2GPI IgM, junto con trombosis vascular sugieren un diagnóstico definitivo de SAF.
La trombosis de COVID-19 no solo comparte manifestaciones clínicas similares con el SAF, lo que es más importante, se han encontrado anticuerpos aPL en aproximadamente el 50% de los pacientes hospitalizados con COIVD-19. Según un estudio de la Universidad de Michigan, entre 172 pacientes hospitalizados con COVID-19, el 23% eran positivos para aCL IgM y el 52% eran positivos para cualquier anticuerpo aPL. Sin embargo, un estudio anterior del Hospital del Colegio Médico de la Unión de Pekín (PUMCH) había encontrado que los aβ2GPI IgA (28,8%) y los aCL IgA (25,8%) eran las primeras y segundas proporciones más altas de anticuerpos aPL individuales presentes en 66 pacientes con COVID-19 en estado crítico (admitidos en la UCI). Los resultados de la investigación de variantes se podrían deber a las diferencias en la gravedad de las condiciones de la COVID-19 y la heterogeneidad inherente de los anticuerpos aPL entre los individuos.
Otros estudios han revelado la asociación entre los niveles de concentración de anticuerpos aPL y la predisposición a eventos trombóticos en pacientes con COVID-19. Investigadores de la Universidad de Michigan inyectaron modelos de ratones con IgG purificada de siete sueros de pacientes con COVID-19 y un suero de pacientes con SAF catastrófico (CSAF). Los trombos en ratones tratados con anticuerpos aPL de alto nivel o sueros CSAF se encontraron entonces significativamente mayores que los de los ratones tratados con anticuerpos aPL de bajo nivel. Mediante el análisis de las correlaciones entre las manifestaciones clínicas y los perfiles de anticuerpos aPL y los niveles de concentración, el equipo de investigación de PUMCH también demostró que ser positivo para múltiples anticuerpos aPL o tener títulos de anticuerpos aPL de moderados a altos es más útil para predecir la posibilidad de eventos trombóticos en los pacientes con COVID-19 que ser positivo para un solo anticuerpo aPL o tener niveles de concentración bajos. En las conclusiones, los autores de ambos artículos sugieren un cribado amplio de anticuerpos aPL en todos los pacientes con COVID-19 para mejorar la estratificación del riesgo.
La persistencia de anticuerpos aPL en los pacientes con COVID-19 es otra gran preocupación para científicos y médicos relevantes. Aunque se cree que la mayoría de los anticuerpos aPL asociados a virus son transitorios, una revisión reciente de 163 casos publicados de anticuerpos aPL asociados a virus encontró eventos trombóticos en 116 casos, lo que sugiere que los anticuerpos aPL transitorios también pueden tener potencial protrombótico. Además, en la investigación mencionada anteriormente en PUMCH, los investigadores indagaron sobre los cambios dinámicos de los anticuerpos aPL en seis pacientes COVID-19 y encontraron la persistencia de anticuerpos aPL en cuatro de los pacientes al menos dentro de los 47 días posteriores al inicio de la enfermedad, entre los cuales un paciente mostró persistencia de aβ2GPI IgG en el día 80 posterior al inicio de la enfermedad a pesar de las intervenciones con recambio plasmático, y otro paciente mantuvo niveles altos de anticuerpos múltiples aPL durante aproximadamente dos semanas. Solo en dos pacientes los anticuerpos aPL desaparecieron en 47 días. Estos resultados sugieren que los niveles de anticuerpos aPL fluctúan y exhiben diferentes patrones dinámicos entre diferentes pacientes con COVID-19. Para algunos pacientes, los anticuerpos aPL pueden persistir más tiempo y requieren detecciones de monitoreo adicionales. Para ayudar a guiar la toma de decisiones médicas, se recomienda que los pacientes se vuelvan a realizar la prueba de anticuerpos aPL al menos una vez, después de 12 semanas si la serie inicial de pruebas de anticuerpos aPL fue positiva.
A pesar de la disputa sobre qué anticuerpos aPL son más prevalentes en pacientes con COVID-19, los investigadores de la Universidad de Michigan y PUMCH coinciden en la alta prevalencia de anticuerpos aPL en pacientes con afecciones graves de COVID-19 y la presencia de anticuerpos aPL contribuye a las formaciones de coágulos de sangre. Se especula que la detección de anticuerpos aPL es un posible enfoque para prevenir los coágulos sanguíneos en pacientes con COVID-19 y mejorar la estratificación del riesgo y la personalización del tratamiento. Teniendo en cuenta la posibilidad de una exacerbación del SAF causada por la infección por SARS-CoV-2, es hora de aumentar nuestra conciencia sobre la atención médica de los pacientes con SAF y las detecciones de estos anticuerpos. En comparación con la población general, los pacientes persistentemente positivos para anticuerpos aPL tienen un mayor riesgo de coágulos de sangre durante la hospitalización. Por lo tanto, en caso de hospitalización relacionada con COVID-19, es importante que los pacientes persistentemente positivos para anticuerpos aPL discutan las estrategias de prevención de coágulos de sangre con sus médicos. Los pacientes con SAF deben seguir todas las precauciones estándar, incluido el distanciamiento social, usar máscaras al aire libre, lavarse las manos con frecuencia y evitar el contacto con personas enfermas para prevenir la COVID-19.
Las soluciones de YHLO para la detección de anticuerpos aPL que podrían ayudar a prevenir coágulos sanguíneos potencialmente mortales en la COVID-19 incluyen pruebas para la detección de Cardiolipina IgG, Cardiolipina IgM, Cardiolipina IgA, Anti-Cardiolipina, β2-Glicoproteína I IgG, β2- Glicoproteína I IgA, β2-Glicoproteína I IgM y Anti-β2-Glicoproteína I. Las pruebas de detección relacionadas con el SARS-CoV-2 de YHLO incluyen iFlash-2019-nCoV Ag, iFlash-2019-nCoV Nab, iFlash-2019-nCoV IgG, iFlash- 2019-nCoV IgM e iFlash-2019-nCoV IgA. YHLO también ofrece pruebas para la detección de otras infecciones como Anti-TP, Anti-VHC, HBsAg, Anti-HBs, HBeAg, Anti-HBe, Anti-HBc y HIV Combo.
Enlace relacionado:
Últimas COVID-19 noticias
- Inmunosensor nuevo allana el camino para pruebas rápidas POC para COVID-19 y enfermedades infecciosas emergentes
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Prueba nueva COVID + Influenza + VSR ayudará a estar preparados para la ‘tripledemia’
- IA elimina las conjeturas de las pruebas de flujo lateral
- Prueba de antígeno del SARS-CoV-2 más rápida, jamás diseñada, permite realizar pruebas de COVID-19 no invasivas en cualquier entorno
- Pruebas rápidas de antígeno detectan las variantes ómicron, delta del SARS-CoV-2
- Prueba en sangre realizada durante la infección inicial predice el riesgo de COVID prolongada
- Investigadores afirman que hay que crear “reservistas” de laboratorio para responder más rápidamente a la próxima pandemia
- Estudio encuentra que los profesionales sanitarios mostraron mayor interés en tecnologías POC durante la pandemia
- Plataforma de análisis de bajo costo para la COVID-19 combina sensibilidad de la PCR y velocidad de pruebas de antígeno
- Prueba de sangre por punción digital identifica inmunidad a la COVID-19
- Kit de prueba rápida determina inmunidad contra la COVID-19 y sus variantes
Canales
Química Clínica
ver canal
Simple prueba cutánea podría revolucionar el diagnóstico de esofagitis eosinofílica pediátrica
La esofagitis eosinofílica (EE) es una enfermedad crónica, causada por alérgenos alimentarios, que se caracteriza por inflamación y daño del revestimiento esofágico.... Más
Herramienta de diagnóstico portátil utiliza bioluminiscencia para detectar virus POC
Los diagnósticos en el punto de atención se han convertido en herramientas cruciales en muchos hogares, permitiendo a las personas medir la glucemia, realizar pruebas de embarazo e incluso... Más
Prueba de madurez pulmonar con IA identifica recién nacidos con mayor riesgo de dificultad respiratoria
Cada año, aproximadamente 300.000 bebés nacen en Estados Unidos entre las 32 y 36 semanas de gestación, según datos nacionales de salud. Este grupo presenta un riesgo elevado de dificultad respiratoria,... MásDiagnóstico Molecular
ver canal
Microbios intestinales podrían permitir detección temprana y tratamiento del cáncer de páncreas
El cáncer de páncreas sigue siendo una de las enfermedades más graves y desafiantes en oncología debido a su dificultad para detectarlo y a sus limitadas opciones de tratamiento.... Más
Prueba altamente sensible y específica permite detección temprana del cáncer colorrectal
Una prueba diagnóstica altamente sensible y específica para la detección temprana y el tratamiento del cáncer colorrectal podría permitir el tratamiento en las etapas... MásHematología
ver canal
Prueba de cartucho desechable ofrece resultados de hemograma rápidos y precisos
El hemograma completo (HC) es una de las pruebas de laboratorio más solicitadas, crucial para diagnosticar enfermedades, monitorear terapias y realizar exámenes de salud rutinarios.... Más
Primera prueba de monitorización de heparina POC proporciona resultados rápidos
La dosificación de heparina requiere un manejo cuidadoso para evitar complicaciones hemorrágicas y de coagulación. En situaciones de alto riesgo, como la oxigenación por membrana... MásInmunología
ver canal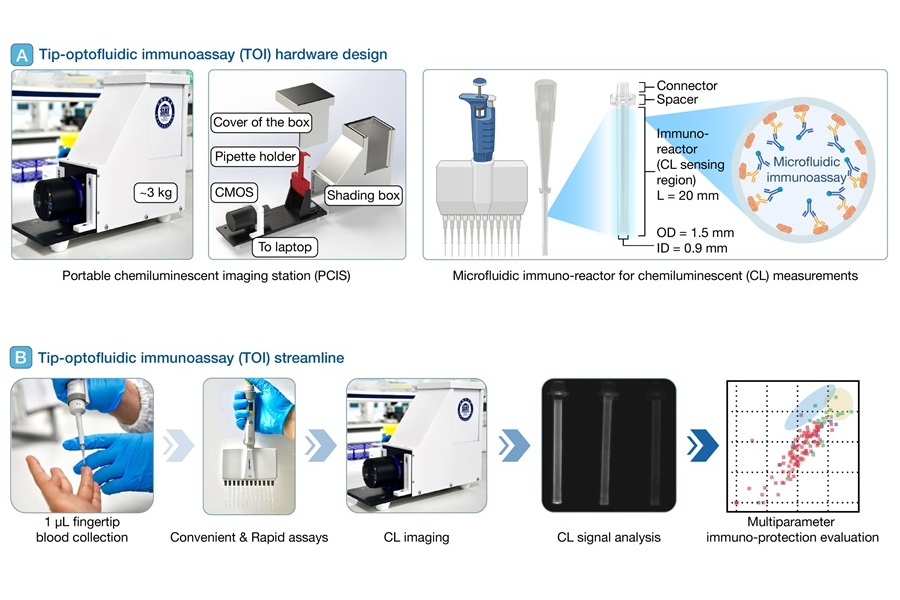
Plataforma de diagnóstico POC realiza análisis inmunológico con una gota de sangre del dedo
A medida que surgen nuevas variantes de la COVID-19 y las personas acumulan historiales complejos de vacunación e infección, existe una necesidad urgente de herramientas de diagnóstico... Más
Cambio de tratamiento guiado por biopsia líquida mejora resultados en pacientes con cáncer de mama
El tratamiento estándar para pacientes con cáncer de mama avanzado con receptor de estrógeno (RE) positivo y HER2 negativo, un subtipo impulsado por los receptores de estrógeno... Más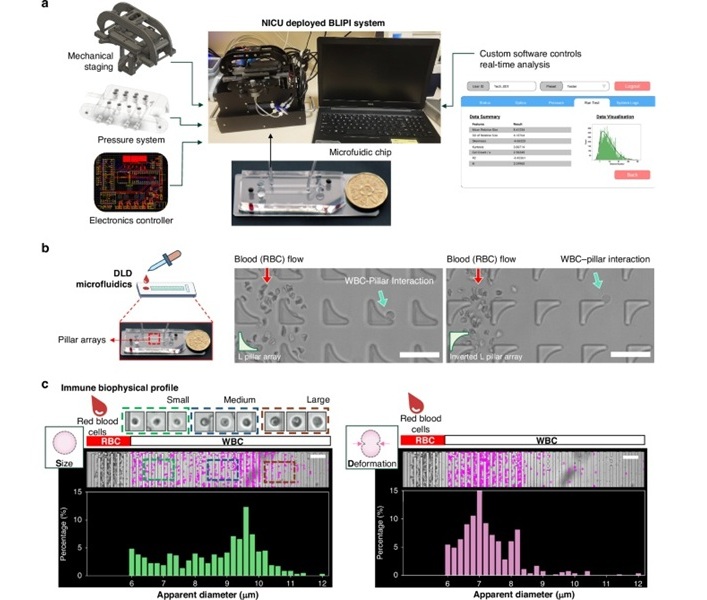
Dispositivo innovador analiza función inmunitaria de recién nacidos con una gota de sangre
Los bebés prematuros son muy susceptibles a enfermedades graves y potencialmente mortales, como la sepsis y la enterocolitis necrosante (ECN). La sepsis neonatal, una infección del torrente sanguíneo que... Más
Prueba de células madre predice resultado del tratamiento en cáncer de ovario resistente al platino
El cáncer de ovario epitelial suele responder inicialmente a la quimioterapia, pero con el tiempo, el tumor desarrolla resistencia a la terapia, lo que provoca su recrecimiento. Esta resistencia... MásMicrobiología
ver canal
Prueba de diagnóstico rápido reduce mortalidad por sepsis 39 %
La sepsis sigue siendo una de las afecciones más desafiantes y mortales en la atención médica contemporánea, representando casi un tercio de todas las muertes hospitalarias... Más
Análisis de hemocultivo mejora gestión diagnóstica mediante selección de panel específico
Cada año, alrededor de 250.000 personas en los EUA son diagnosticadas con infecciones del torrente sanguíneo (ITS). La sepsis causada por estas infecciones conlleva una tasa de mortalidad... MásPatología
ver canal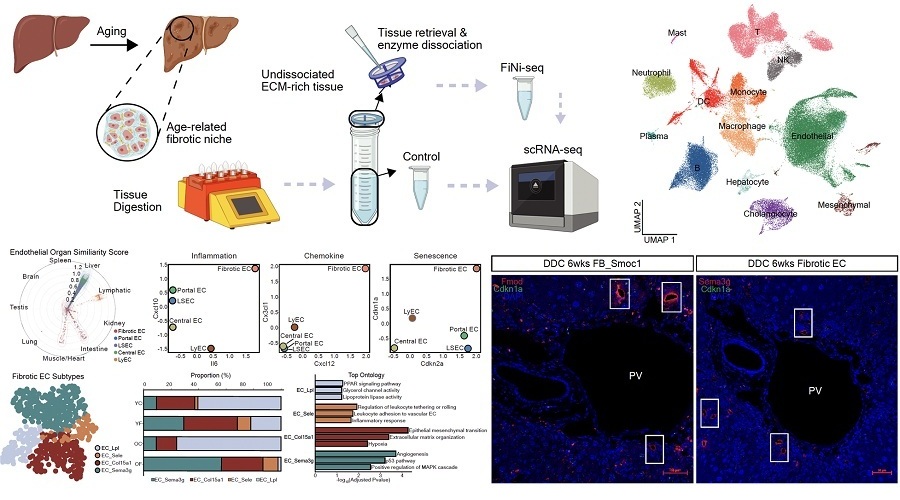
Nueva plataforma tecnológica predice enfermedades mediante detección temprana de señales de envejecimiento en tejido hepático
El envejecimiento y las enfermedades crónicas se caracterizan por la lenta acumulación de sutiles alteraciones tisulares durante largos periodos. Sin embargo, captar cuantitativamente estos... Más
Modelo de IA detecta más de 170 tipos de cáncer
El diagnóstico de tumores cerebrales puede ser especialmente difícil cuando el tumor se localiza en una región donde las biopsias presentan un alto riesgo. En estos casos, donde no... MásTecnología
ver canal
Encuesta revela que gestión mejorada de datos de laboratorio e IA son cruciales para laboratorios del futuro
Los datos desempeñan un papel fundamental en la transformación de los laboratorios digitales actuales, actuando como un desafío clave y como un catalizador para la innovación,... Más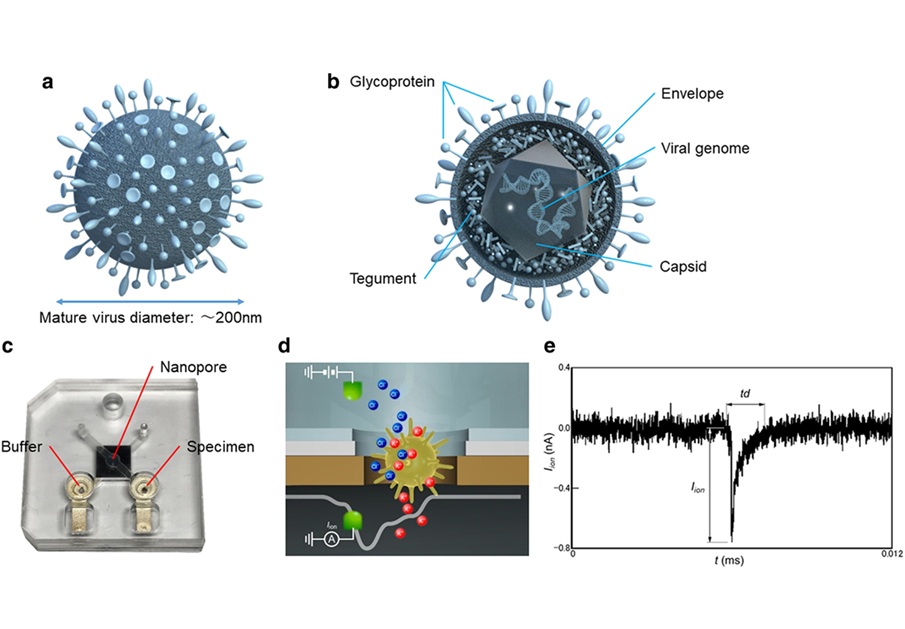
Prueba no basada en ADN con IA identifica infecciones virales
La confirmación de infecciones virales suele implicar pruebas de secuenciación de ADN, que tardan horas y pueden no estar disponibles in situ. Además, estas pruebas no pueden diferenciar... MásIndustria
ver canal
Universidad de Aston y BG Research se asocian para comercializar diagnóstico médico innovador
La tecnología que puede diagnosticar rápidamente enfermedades infecciosas de alto impacto dará un gran paso hacia su comercialización gracias a una nueva asociación.... Más