Metabolismo del triptófano está mal regulado en los individuos con anemia de Fanconi
|
Por el equipo editorial de LabMedica en español Actualizado el 20 Jan 2021 |
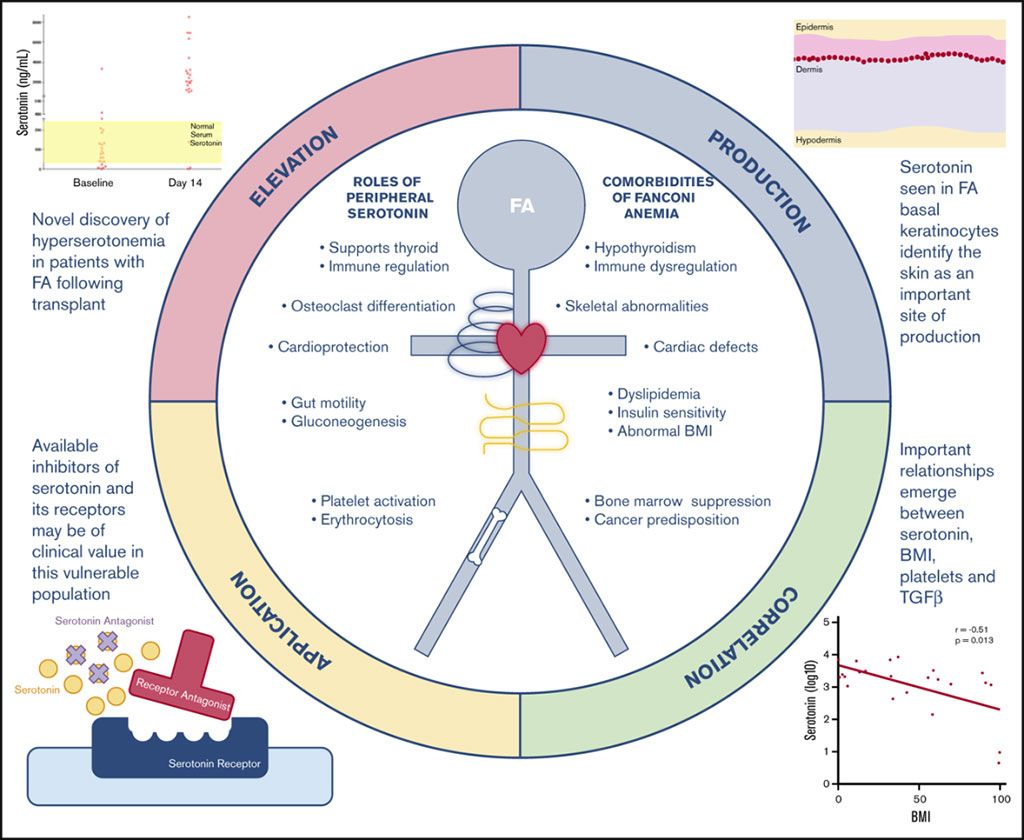
Imagen: El metabolismo del triptófano está mal regulado en personas con anemia de Fanconi (Fotografía cortesía del Centro Médico del Hospital Infantil de Cincinnati).
La anemia de Fanconi (AF) es un trastorno genético complejo que se asocia frecuentemente con insuficiencia medular progresiva y una fuerte predisposición a neoplasias malignas tempranas, en particular carcinomas escamocelulares y carcinomas hepatocelulares.
El triptófano es un aminoácido esencial necesario para la síntesis de proteínas. El metabolismo del triptófano se ha relacionado estrechamente con alteraciones en el microbioma, y la mala regulación de la vía del triptófano tiene implicaciones significativas para la regulación inmunológica del huésped, la inflamación intestinal y la salud en general.
Los hematólogos del Centro Médico del Hospital Infantil de Cincinnati (Cincinnati, OH, EUA) y sus asociados, recolectaron muestras de sangre y heces de 23 pacientes con AF (52% mujeres y rango de edad de 5 a 27 años) y 29 pacientes con otros diagnósticos (31% mujeres y rango de edad 1-18 años). El equipo estudió el metabolismo del triptófano en la AF examinando el triptófano y sus metabolitos antes y durante el estrés del trasplante de células madre hematopoyéticas (TCMH). El triptófano se puede convertir en serotonina y quinurenina.
Los niveles plasmáticos de triptófano y de sus metabolitos se midieron utilizando un ensayo inmunoabsorbente ligado a enzimas (ELISA): triptófano (Abnova, Taipéi, Taiwán); serotonina y melatonina (Enzo, Farmingdale, NY, EUA); quinurenina (BlueGene Biotech, Shanghái, China); factor de crecimiento transformante β1 (TGF-β1, R&D Systems, Minneapolis, MN, EUA).
Se aisló el ARN total de células mononucleares de sangre periférica (PBMC) y se midió la expresión de indolamina 2,3-dioxigenasa, triptófano hidroxilasa 1 y transportador de serotonina, mediante RT-qPCR en un sistema de PCR en tiempo real 7300 de Applied Biosystems (Thermo Fisher Scientific, Waltham, MA, EUA). El equipo también realizó inmunoquímica usando un microscopio Olympus BX53 (Olympus América, Waltham, MA, EUA). También se realizó análisis con resonancia magnética nuclear en las muestras de plasma.
Los científicos informaron que los niveles de serotonina estaban marcadamente elevados 14 días después del TCMH en individuos con AF, en contraste con los individuos sin AF. Los niveles de quinurenina se redujeron significativamente en los individuos con AF, en comparación con los individuos sin AF, antes y después del TCMH. La mayor parte de la serotonina periférica se produce en el intestino. Sin embargo, los niveles de serotonina en las heces disminuyeron en las personas con AF después del trasplante, de manera similar a las personas sin AF. En cambio, el equipo detectó la producción de serotonina en la piel en personas con AF, mientras que no se observó ninguna producción en personas sin AF.
Los niveles de serotonina y TGF-β se correlacionaron estrechamente con el recuento de plaquetas antes y después del TCMH en personas sin AF. En la AF, ni la serotonina basal ni el TGF-β se correlacionaron con el recuento basal de plaquetas (plaquetas derivadas del huésped), solo el TGF-β se correlacionó 14 días después del trasplante (plaquetas derivadas del banco de sangre).
Los autores concluyeron que sus hallazgos sugieren que la inhibición de la serotonina es una nueva vía para disminuir una multitud de riesgos clínicos y fenotipos de enfermedades en la AF, que ahora requerirán una caracterización detallada del metabolismo de la serotonina local y sistémica. El estudio fue publicado el 7 de enero de 2021 en la revista Blood Advances.
Enlace relacionado:
Centro Médico del Hospital Infantil de Cincinnati
Abnova
Enzo
BlueGene Biotech
R&D Systems
Olympus America
El triptófano es un aminoácido esencial necesario para la síntesis de proteínas. El metabolismo del triptófano se ha relacionado estrechamente con alteraciones en el microbioma, y la mala regulación de la vía del triptófano tiene implicaciones significativas para la regulación inmunológica del huésped, la inflamación intestinal y la salud en general.
Los hematólogos del Centro Médico del Hospital Infantil de Cincinnati (Cincinnati, OH, EUA) y sus asociados, recolectaron muestras de sangre y heces de 23 pacientes con AF (52% mujeres y rango de edad de 5 a 27 años) y 29 pacientes con otros diagnósticos (31% mujeres y rango de edad 1-18 años). El equipo estudió el metabolismo del triptófano en la AF examinando el triptófano y sus metabolitos antes y durante el estrés del trasplante de células madre hematopoyéticas (TCMH). El triptófano se puede convertir en serotonina y quinurenina.
Los niveles plasmáticos de triptófano y de sus metabolitos se midieron utilizando un ensayo inmunoabsorbente ligado a enzimas (ELISA): triptófano (Abnova, Taipéi, Taiwán); serotonina y melatonina (Enzo, Farmingdale, NY, EUA); quinurenina (BlueGene Biotech, Shanghái, China); factor de crecimiento transformante β1 (TGF-β1, R&D Systems, Minneapolis, MN, EUA).
Se aisló el ARN total de células mononucleares de sangre periférica (PBMC) y se midió la expresión de indolamina 2,3-dioxigenasa, triptófano hidroxilasa 1 y transportador de serotonina, mediante RT-qPCR en un sistema de PCR en tiempo real 7300 de Applied Biosystems (Thermo Fisher Scientific, Waltham, MA, EUA). El equipo también realizó inmunoquímica usando un microscopio Olympus BX53 (Olympus América, Waltham, MA, EUA). También se realizó análisis con resonancia magnética nuclear en las muestras de plasma.
Los científicos informaron que los niveles de serotonina estaban marcadamente elevados 14 días después del TCMH en individuos con AF, en contraste con los individuos sin AF. Los niveles de quinurenina se redujeron significativamente en los individuos con AF, en comparación con los individuos sin AF, antes y después del TCMH. La mayor parte de la serotonina periférica se produce en el intestino. Sin embargo, los niveles de serotonina en las heces disminuyeron en las personas con AF después del trasplante, de manera similar a las personas sin AF. En cambio, el equipo detectó la producción de serotonina en la piel en personas con AF, mientras que no se observó ninguna producción en personas sin AF.
Los niveles de serotonina y TGF-β se correlacionaron estrechamente con el recuento de plaquetas antes y después del TCMH en personas sin AF. En la AF, ni la serotonina basal ni el TGF-β se correlacionaron con el recuento basal de plaquetas (plaquetas derivadas del huésped), solo el TGF-β se correlacionó 14 días después del trasplante (plaquetas derivadas del banco de sangre).
Los autores concluyeron que sus hallazgos sugieren que la inhibición de la serotonina es una nueva vía para disminuir una multitud de riesgos clínicos y fenotipos de enfermedades en la AF, que ahora requerirán una caracterización detallada del metabolismo de la serotonina local y sistémica. El estudio fue publicado el 7 de enero de 2021 en la revista Blood Advances.
Enlace relacionado:
Centro Médico del Hospital Infantil de Cincinnati
Abnova
Enzo
BlueGene Biotech
R&D Systems
Olympus America
Últimas Inmunología noticias
- Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
- Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
- Técnicas de vanguardia para investigar respuesta inmune en infecciones mortales por estreptococo A
- Novedosos inmunoensayos permiten diagnóstico temprano del síndrome antifosfolípido
- Nueva prueba podría predecir éxito de inmunoterapia para una gama más amplia de cánceres
- Pruebas simples de proteínas en sangre predicen resultados de CAR T para pacientes con linfoma
- Tecnología de chip clasificador de células podría allanar el camino para elaboración de perfiles inmunológicos POC
- Chip monitorea células cancerosas en muestras de sangre para evaluar eficacia del tratamiento
- Enfoques de inmunohematología automatizados pueden resolver incompatibilidad de trasplantes
- IA aprovecha genética tumoral para predecir respuesta del paciente a quimioterapia
- Primer dispositivo de monitoreo de leucocitos portátil y no invasivo del mundo elimina necesidad de extracción de sangre
- Prueba predictiva de células T detecta respuesta inmune a virus incluso antes de que se formen anticuerpos
- Analizador de inmunoensayo fluorescente portátil para pruebas POC rápidas transforma diagnósticos clínicos
- Detección multiparamétrica de autoanticuerpos ayuda a diagnosticar miositis
- Analizador CLIA todo en uno transforma el panorama del diagnóstico clínico
- Primera prueba de biomarcadores en sangre para predecir respuesta al tratamiento en pacientes con cáncer
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Ensayo de PCR simple diferencia con precisión entre los subtipos de cáncer de pulmón de células pequeñas
El cáncer de pulmón de células pequeñas (CPCP), una neoplasia maligna neuroendocrina que progresa rápidamente, presenta bajas tasas de supervivencia. A pesar de su heterogeneidad molecular y clínica, el... Más
Enfoque revolucionario de análisis de células T permite detección temprana del cáncer
La biopsia líquida, un método para diagnosticar el cáncer mediante análisis de sangre de rutina, es una herramienta potencial importante para la detección temprana del... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Innovadora plataforma de diagnóstico proporciona resultados de AST con velocidad sin precedentes
Una plataforma de diagnóstico innovadora que ofrece resultados de pruebas de susceptibilidad a los antibióticos (AST) con una velocidad sin precedentes puede convertirse en una herramienta importante para... Más
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... MásPatología
ver canal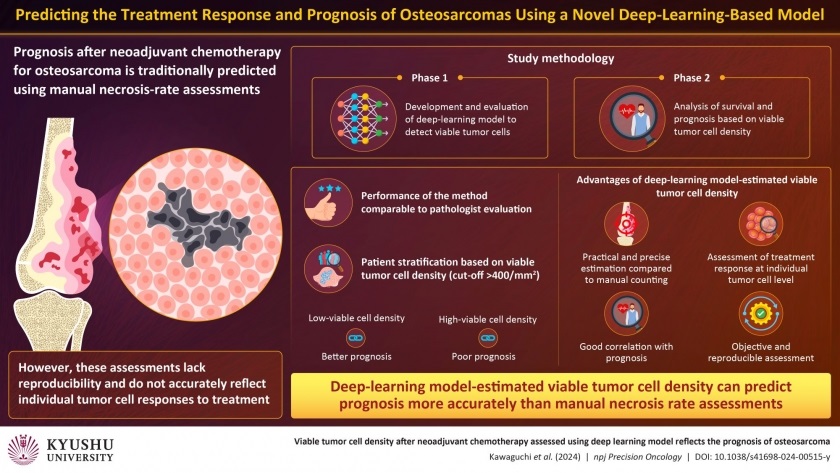
Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico... Más
Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
La comunidad médica mundial reconoce cada vez más que la biopsia líquida es un enfoque transformador para mejorar la atención al paciente con cáncer. Este innovador método de diagnóstico implica detectar... MásTecnología
ver canal
Nuevo sistema de diagnóstico de laboratorio en un chip iguala la precisión de las pruebas de PCR
Si bien las pruebas de PCR son el estándar de oro en cuanto a precisión para las pruebas de virología, tienen limitaciones como la complejidad, la necesidad de operadores de laboratorio capacitados y tiempos... Más
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)


.jpg)



