La FDA publica una guía para facilitar el desarrollo oportuno de vacunas contra la COVID-19 seguras y efectivas
|
Por el equipo editorial de LabMedica en español Actualizado el 03 Jul 2020 |

Ilustración
La Administración de Medicamentos y Alimentos de los EUA (FDA Silver Spring, MD, EUA) emitió una guía con recomendaciones para aquellos que desarrollan vacunas COVID-19 con el fin último de obtener la licencia.
La guía de la FDA, que tiene como objetivo ayudar a facilitar el desarrollo oportuno de vacunas seguras y efectivas para prevenir la COVID-19, refleja el consejo que la agencia ha brindado en los últimos meses a empresas, investigadores y otros, describe sus recomendaciones actuales con respecto a los datos necesarios para facilitar la fabricación, el desarrollo clínico y la aprobación de una vacuna contra la COVID-19. La guía, “Desarrollo y Licencias de vacunas para prevenir la COVID-19”, proporciona una visión general de las consideraciones clave para satisfacer los requisitos de química, fabricación y control, datos clínicos y no clínicos a través del desarrollo y la licencia, y para la evaluación de seguridad posterior a la licencia. Dada la comprensión actual de la inmunología del SARS-CoV-2, la agencia ha enfatizado que el objetivo de los programas de desarrollo en este momento debe ser apoyar la aprobación tradicional de la FDA mediante la realización de estudios para evaluar directamente la capacidad de la vacuna para proteger a los humanos de la infección y/o enfermedad del SARS-CoV -2.
La FDA recomienda encarecidamente la inclusión de diversas poblaciones en todas las fases del desarrollo clínico, incluidas las poblaciones más afectadas por la COVID-19, específicamente las minorías raciales y étnicas, así como la representación adecuada en ensayos de fase tardía de personas de edad avanzada y personas con comorbilidades médicas. La FDA también invita a los patrocinadores a incluir estudios en sus planes de desarrollo que brinden datos para respaldar el uso durante el embarazo y que también planifiquen evaluaciones pediátricas de seguridad y efectividad. La guía también analiza la importancia de garantizar que los tamaños de los ensayos clínicos sean lo suficientemente grandes como para demostrar la seguridad y la eficacia de una vacuna. Transmite que la FDA esperaría que una vacuna COVID-19 prevenga la enfermedad o disminuya su gravedad en al menos el 50% de las personas vacunadas.
Además, los sistemas de vigilancia existentes continuarán monitoreando de cerca la seguridad de todas las vacunas, incluida una vacuna contra la COVID-19 después de la aprobación de la FDA. La FDA también podría requerir estudios posteriores a la comercialización para evaluar aún más los riesgos graves conocidos o potenciales. La guía también señala que, a medida que se aprenda más sobre la inmunología del SARS-CoV-2 y las respuestas inmunitarias de la vacuna se puede considerar la vía de aprobación acelerada de la FDA para obtener la licencia de la vacuna. Sin embargo, la identificación de una respuesta inmune u otra medida que sea razonablemente probable para predecir el beneficio clínico sería necesaria para que una vacuna candidata específica use esta vía. Debido a la actual emergencia de salud pública, la guía también aborda consideraciones con respecto a la Autorización de Uso en Emergencias (AUE) de una vacuna en investigación, dejando en claro que una evaluación con respecto a cualquier AUE potencial para una vacuna COVID-19 se haría caso por caso considerando la población objetivo, las características del producto y la totalidad de la evidencia científica relevante disponible, incluidos los datos de estudios clínicos preclínicos y humanos sobre la seguridad y eficacia del producto.
“Reconocemos la necesidad urgente de desarrollar una vacuna segura y efectiva para prevenir la COVID-19 y continuar trabajando en colaboración con la industria, los investigadores, así como con socios federales, nacionales e internacionales para acelerar estos esfuerzos. Si bien la FDA se compromete a agilizar este trabajo, no atajaremos nuestras decisiones y dejaremos en claro a través de esta guía qué datos se deben enviar para cumplir con nuestros estándares reglamentarios. Esto es particularmente importante, ya que sabemos que algunas personas son escépticas de los esfuerzos de desarrollo de vacunas”, dijo el comisionado de la FDA, Stephen M. Hahn, M.D.
“En esta crisis particular en la que hay tanto en juego, necesitamos ayudar a acelerar el desarrollo de la vacuna tanto como podamos sin sacrificar nuestros estándares de calidad, seguridad y eficacia. Creemos firmemente que la transparencia con respecto al pensamiento actual de la FDA sobre los datos científicos necesarios para respaldar la aprobación de vacunas contra la COVID-19 seguras y efectivas ayudará a construir la confianza del público en el proceso de evaluación de la FDA, que será fundamental para garantizar su uso”, dijo Peter Marks , MD, Ph.D., director del Centro de Evaluación e Investigación Biológica de la FDA. “En este momento, ni la FDA ni la comunidad científica pueden predecir qué tan rápido se generarán los datos de los ensayos clínicos de vacunas. Una vez que se generan los datos, la agencia se compromete a evaluarlos exhaustiva y rápidamente. Pero no se equivoque: la FDA solo aprobará o pondrá a disposición una vacuna COVID-19 si determinamos que cumple con los altos estándares que la gente espera de la agencia”.
Enlace relacionado:
Administración de Medicamentos y Alimentos de los EUA
La guía de la FDA, que tiene como objetivo ayudar a facilitar el desarrollo oportuno de vacunas seguras y efectivas para prevenir la COVID-19, refleja el consejo que la agencia ha brindado en los últimos meses a empresas, investigadores y otros, describe sus recomendaciones actuales con respecto a los datos necesarios para facilitar la fabricación, el desarrollo clínico y la aprobación de una vacuna contra la COVID-19. La guía, “Desarrollo y Licencias de vacunas para prevenir la COVID-19”, proporciona una visión general de las consideraciones clave para satisfacer los requisitos de química, fabricación y control, datos clínicos y no clínicos a través del desarrollo y la licencia, y para la evaluación de seguridad posterior a la licencia. Dada la comprensión actual de la inmunología del SARS-CoV-2, la agencia ha enfatizado que el objetivo de los programas de desarrollo en este momento debe ser apoyar la aprobación tradicional de la FDA mediante la realización de estudios para evaluar directamente la capacidad de la vacuna para proteger a los humanos de la infección y/o enfermedad del SARS-CoV -2.
La FDA recomienda encarecidamente la inclusión de diversas poblaciones en todas las fases del desarrollo clínico, incluidas las poblaciones más afectadas por la COVID-19, específicamente las minorías raciales y étnicas, así como la representación adecuada en ensayos de fase tardía de personas de edad avanzada y personas con comorbilidades médicas. La FDA también invita a los patrocinadores a incluir estudios en sus planes de desarrollo que brinden datos para respaldar el uso durante el embarazo y que también planifiquen evaluaciones pediátricas de seguridad y efectividad. La guía también analiza la importancia de garantizar que los tamaños de los ensayos clínicos sean lo suficientemente grandes como para demostrar la seguridad y la eficacia de una vacuna. Transmite que la FDA esperaría que una vacuna COVID-19 prevenga la enfermedad o disminuya su gravedad en al menos el 50% de las personas vacunadas.
Además, los sistemas de vigilancia existentes continuarán monitoreando de cerca la seguridad de todas las vacunas, incluida una vacuna contra la COVID-19 después de la aprobación de la FDA. La FDA también podría requerir estudios posteriores a la comercialización para evaluar aún más los riesgos graves conocidos o potenciales. La guía también señala que, a medida que se aprenda más sobre la inmunología del SARS-CoV-2 y las respuestas inmunitarias de la vacuna se puede considerar la vía de aprobación acelerada de la FDA para obtener la licencia de la vacuna. Sin embargo, la identificación de una respuesta inmune u otra medida que sea razonablemente probable para predecir el beneficio clínico sería necesaria para que una vacuna candidata específica use esta vía. Debido a la actual emergencia de salud pública, la guía también aborda consideraciones con respecto a la Autorización de Uso en Emergencias (AUE) de una vacuna en investigación, dejando en claro que una evaluación con respecto a cualquier AUE potencial para una vacuna COVID-19 se haría caso por caso considerando la población objetivo, las características del producto y la totalidad de la evidencia científica relevante disponible, incluidos los datos de estudios clínicos preclínicos y humanos sobre la seguridad y eficacia del producto.
“Reconocemos la necesidad urgente de desarrollar una vacuna segura y efectiva para prevenir la COVID-19 y continuar trabajando en colaboración con la industria, los investigadores, así como con socios federales, nacionales e internacionales para acelerar estos esfuerzos. Si bien la FDA se compromete a agilizar este trabajo, no atajaremos nuestras decisiones y dejaremos en claro a través de esta guía qué datos se deben enviar para cumplir con nuestros estándares reglamentarios. Esto es particularmente importante, ya que sabemos que algunas personas son escépticas de los esfuerzos de desarrollo de vacunas”, dijo el comisionado de la FDA, Stephen M. Hahn, M.D.
“En esta crisis particular en la que hay tanto en juego, necesitamos ayudar a acelerar el desarrollo de la vacuna tanto como podamos sin sacrificar nuestros estándares de calidad, seguridad y eficacia. Creemos firmemente que la transparencia con respecto al pensamiento actual de la FDA sobre los datos científicos necesarios para respaldar la aprobación de vacunas contra la COVID-19 seguras y efectivas ayudará a construir la confianza del público en el proceso de evaluación de la FDA, que será fundamental para garantizar su uso”, dijo Peter Marks , MD, Ph.D., director del Centro de Evaluación e Investigación Biológica de la FDA. “En este momento, ni la FDA ni la comunidad científica pueden predecir qué tan rápido se generarán los datos de los ensayos clínicos de vacunas. Una vez que se generan los datos, la agencia se compromete a evaluarlos exhaustiva y rápidamente. Pero no se equivoque: la FDA solo aprobará o pondrá a disposición una vacuna COVID-19 si determinamos que cumple con los altos estándares que la gente espera de la agencia”.
Enlace relacionado:
Administración de Medicamentos y Alimentos de los EUA
Últimas COVID-19 noticias
- Inmunosensor nuevo allana el camino para pruebas rápidas POC para COVID-19 y enfermedades infecciosas emergentes
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Prueba nueva COVID + Influenza + VSR ayudará a estar preparados para la ‘tripledemia’
- IA elimina las conjeturas de las pruebas de flujo lateral
- Prueba de antígeno del SARS-CoV-2 más rápida, jamás diseñada, permite realizar pruebas de COVID-19 no invasivas en cualquier entorno
- Pruebas rápidas de antígeno detectan las variantes ómicron, delta del SARS-CoV-2
- Prueba en sangre realizada durante la infección inicial predice el riesgo de COVID prolongada
- Investigadores afirman que hay que crear “reservistas” de laboratorio para responder más rápidamente a la próxima pandemia
- Estudio encuentra que los profesionales sanitarios mostraron mayor interés en tecnologías POC durante la pandemia
- Plataforma de análisis de bajo costo para la COVID-19 combina sensibilidad de la PCR y velocidad de pruebas de antígeno
- Prueba de sangre por punción digital identifica inmunidad a la COVID-19
- Kit de prueba rápida determina inmunidad contra la COVID-19 y sus variantes
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... Más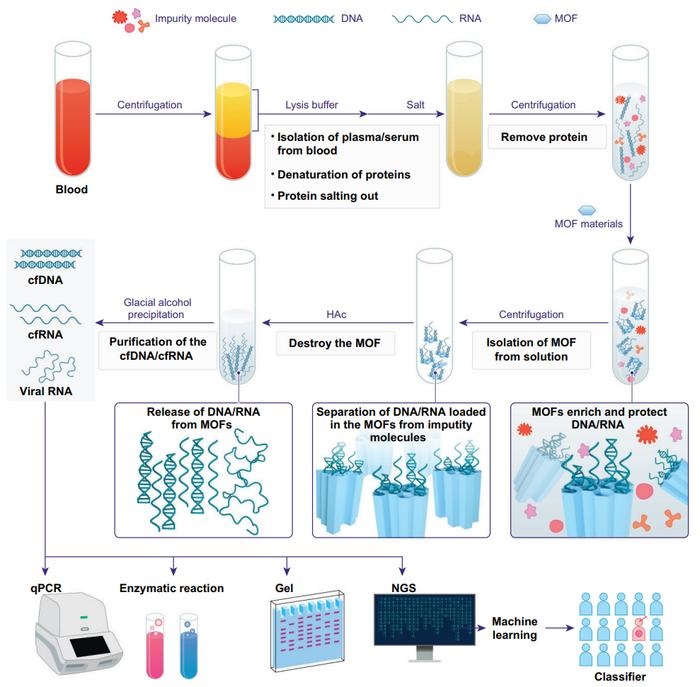
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más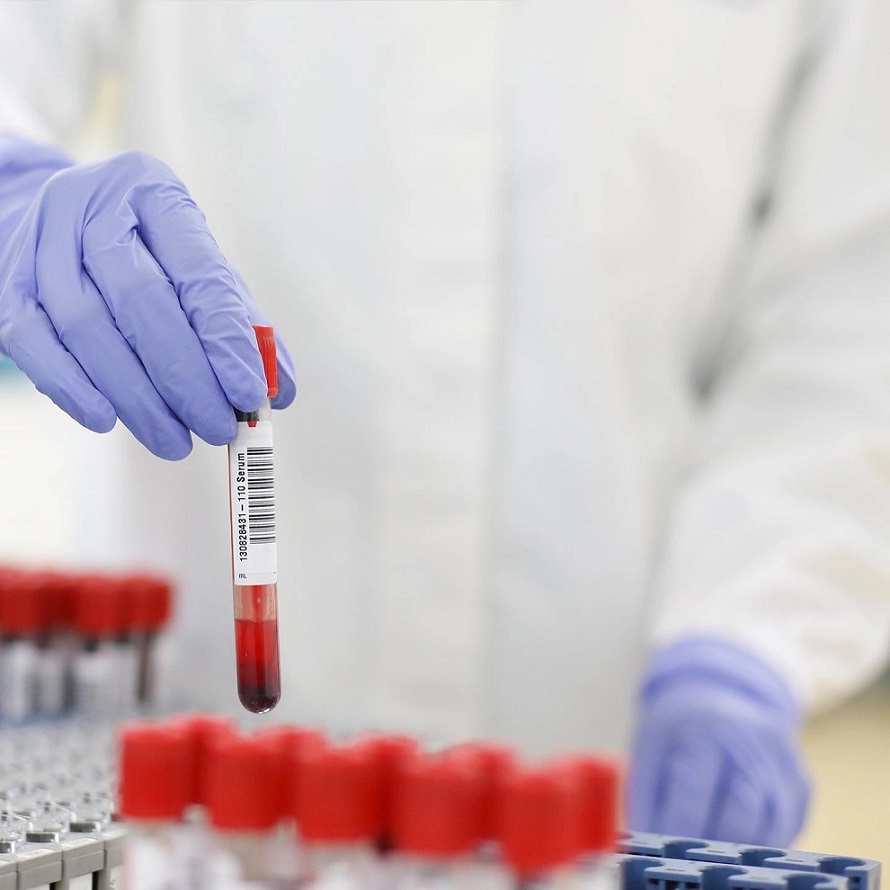
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más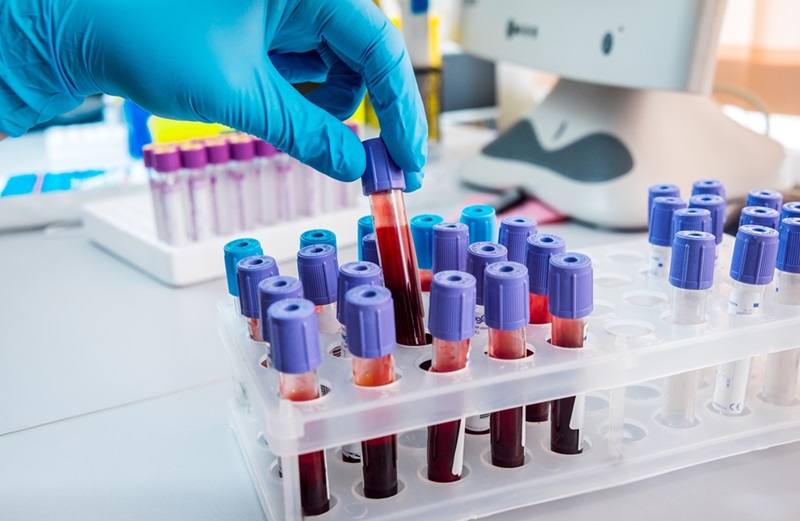
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal
Innovador dispositivo de extracción de sangre supera obstáculos comunes relacionados con la flebotomía
La incomodidad asociada con las extracciones de sangre tradicionales genera un problema importante: aproximadamente el 30 % de las pruebas de diagnóstico prescritas por los médicos nunca... Más
Dispositivo POC intraoperatorio distingue entre quistes ováricos benignos y malignos en 15 minutos
Los quistes ováricos representan un problema de salud importante para las mujeres en todo el mundo, y hasta el 10 % experimenta esta afección en algún momento de sus vidas.... Más
Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
La enfermedad de Parkinson y un grupo de trastornos neurodegenerativos relacionados conocidos como sinucleinopatías afectan a millones de personas en todo el mundo. Estas afecciones, incluida la... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más













.jpg)

.jpg)
.jpg)