Imagenología no invasiva detecta el cáncer a nivel molecular
|
Por el equipo editorial de LabMedica en español Actualizado el 26 Aug 2019 |
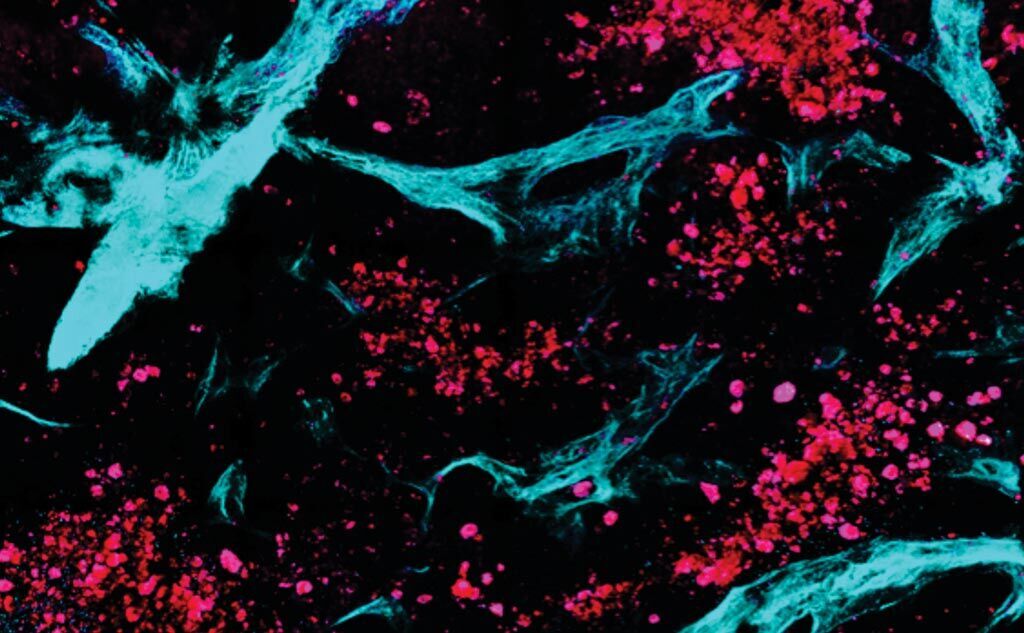
Imagen: Los científicos combinaron la microscopía multifotónica con algoritmos automáticos de análisis de imágenes y estadísticas para diferenciar entre el tejido sano y el enfermo. En esta imagen, recopilada de una manera no invasiva, completamente libre de etiquetas, el colágeno se colorea de verde mientras que los grupos de células metastásicas ováricas se presentan en rojo (Fotografía cortesía de la Universidad de Tufts).
Para los pacientes con cáncer, la presencia de metástasis dicta la evaluación de estadificación que, a su vez, define la ruta de tratamiento adecuada seleccionada. Para los tumores malignos ginecológicos, como el carcinoma de ovario, es de gran importancia diferenciar entre el estado de la enfermedad localizada y metastásica, ya que afecta drásticamente el tratamiento.
Para el diagnóstico in situ, en tiempo real, las nuevas modalidades de imagenología que ofrecen información metabólica y estructural a nivel celular y subcelular pueden ser de gran ayuda, especialmente porque estas modalidades se incorporan progresivamente en sondas y microendoscopios que permiten el acceso intravital a órganos que se encuentran más profundos en el cuerpo.
Científicos biomédicos de la Universidad de Tufts (Medford, MA, EUA) y sus colegas, recolectaron muestras de ocho pacientes a quienes les realizaron una laparotomía abierta como parte de la atención médica de rutina. Después de la finalización de todos los procedimientos intraabdominales de la operación, se recogieron ocho biopsias de peritoneo parietal sano y, si estaba presente, de cuatro metástasis peritoneales de cada paciente. Todas las lesiones fueron evaluadas por un patólogo utilizando histología estándar de hematoxilina y eosina.
Se tomaron imágenes de los tejidos empleando un microscopio de escaneo láser multifotónico, para generar fluorescencia intrínseca e imágenes de segunda generación armónicas (SHG) a 755 nm y 900 nm de excitación, respectivamente, con emisión de señal recolectada a 460 ± 20 y 525 ± 25 nm. La luz láser se centró en la muestra utilizando un objetivo de 25x (0,9 AN/inmersión en agua), y se emplearon filtros de densidad neutra para lograr una potencia de 25-35 mW. Se evaluaron al menos dos o tres campos aleatorios por tejido, alcanzando un total de 30 y 11 imágenes para los grupos de tejido de biopsia sano y metastásico, respectivamente (512 × 512 píxeles; campo de visión de 600 micras; resolución de 1,17 micras por píxel). Las imágenes se enfocaron dentro de una profundidad de ∼20-100 micras desde la superficie mesotelial de los tejidos.
El equipo descubrió que los tejidos sanos mostraban grandes variaciones en las características de contraste y correlación en función de la distancia, correspondiente a fluctuaciones repetitivas y de mayor intensidad local. Las imágenes de tejido metastásico mostraron un contraste disminuido y valores relacionados con la correlación, representando patrones de intensidad más uniformes y fibras más pequeñas, lo que indica la destrucción del estroma sano por la infiltración cancerosa. Analizando 41 imágenes adquiridas de las biopsias, la técnica clasificó correctamente 40 de 41 imágenes (una exactitud del 97,5%). Un total de 11 muestras se clasificaron correctamente como metastásicas (100% de sensibilidad) y 29 de 30 se clasificaron correctamente como sanas (96,6% de especificidad).
Dimitra Pouli, MD, PhD, residente de patología y coautora del estudio, dijo: “El método utilizado en este trabajo identifica de manera completamente libre de etiquetas las características celulares y tisulares a nivel microscópico, esencialmente actuando como una biopsia sin cuchillo”. El estudio se publicó en la edición de agosto de 2019 de la revista Biomedical Optics Express.
Enlace relacionado:
Universidad de Tufts
Para el diagnóstico in situ, en tiempo real, las nuevas modalidades de imagenología que ofrecen información metabólica y estructural a nivel celular y subcelular pueden ser de gran ayuda, especialmente porque estas modalidades se incorporan progresivamente en sondas y microendoscopios que permiten el acceso intravital a órganos que se encuentran más profundos en el cuerpo.
Científicos biomédicos de la Universidad de Tufts (Medford, MA, EUA) y sus colegas, recolectaron muestras de ocho pacientes a quienes les realizaron una laparotomía abierta como parte de la atención médica de rutina. Después de la finalización de todos los procedimientos intraabdominales de la operación, se recogieron ocho biopsias de peritoneo parietal sano y, si estaba presente, de cuatro metástasis peritoneales de cada paciente. Todas las lesiones fueron evaluadas por un patólogo utilizando histología estándar de hematoxilina y eosina.
Se tomaron imágenes de los tejidos empleando un microscopio de escaneo láser multifotónico, para generar fluorescencia intrínseca e imágenes de segunda generación armónicas (SHG) a 755 nm y 900 nm de excitación, respectivamente, con emisión de señal recolectada a 460 ± 20 y 525 ± 25 nm. La luz láser se centró en la muestra utilizando un objetivo de 25x (0,9 AN/inmersión en agua), y se emplearon filtros de densidad neutra para lograr una potencia de 25-35 mW. Se evaluaron al menos dos o tres campos aleatorios por tejido, alcanzando un total de 30 y 11 imágenes para los grupos de tejido de biopsia sano y metastásico, respectivamente (512 × 512 píxeles; campo de visión de 600 micras; resolución de 1,17 micras por píxel). Las imágenes se enfocaron dentro de una profundidad de ∼20-100 micras desde la superficie mesotelial de los tejidos.
El equipo descubrió que los tejidos sanos mostraban grandes variaciones en las características de contraste y correlación en función de la distancia, correspondiente a fluctuaciones repetitivas y de mayor intensidad local. Las imágenes de tejido metastásico mostraron un contraste disminuido y valores relacionados con la correlación, representando patrones de intensidad más uniformes y fibras más pequeñas, lo que indica la destrucción del estroma sano por la infiltración cancerosa. Analizando 41 imágenes adquiridas de las biopsias, la técnica clasificó correctamente 40 de 41 imágenes (una exactitud del 97,5%). Un total de 11 muestras se clasificaron correctamente como metastásicas (100% de sensibilidad) y 29 de 30 se clasificaron correctamente como sanas (96,6% de especificidad).
Dimitra Pouli, MD, PhD, residente de patología y coautora del estudio, dijo: “El método utilizado en este trabajo identifica de manera completamente libre de etiquetas las características celulares y tisulares a nivel microscópico, esencialmente actuando como una biopsia sin cuchillo”. El estudio se publicó en la edición de agosto de 2019 de la revista Biomedical Optics Express.
Enlace relacionado:
Universidad de Tufts
Últimas Tecnología noticias
- Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
- Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
- Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
- Primera tecnología de su tipo para detectar glucosa en saliva humana
- Dispositivo electroquímico identifica personas con mayor riesgo de osteoporosis mediante una sola gota de sangre
- Nueva prueba no invasiva detecta infección por malaria sin muestra de sangre
- Dispositivos de detección optofluídicos portátiles podrían realizar simultáneamente una variedad de pruebas médicas
- Solución de software para punto de atención ayuda a manejar escenarios de pruebas POC dispares en ubicaciones de prueba de pacientes
- Biosensor electrónico detecta biomarcadores en muestras de sangre completa sin agregar reactivos
- Prueba innovadora detecta marcadores biológicos relacionados con una variedad mayor de cánceres
- Kit de detección rápida POC determina la salud intestinal a partir de muestras de suero sanguíneo y heces
- Dispositivo convierte teléfono inteligente en microscopio de fluorescencia por solo 50 dólares
- Lector de tubos portátil habilitado para Wi-Fi diseñado para una fácil portabilidad
- Novedosa plataforma de pruebas de diagnóstico asegura el tiempo de respuesta a situaciones de pandemia emergentes
- Transistor revolucionario podría permitir dispositivos portátiles para medir el sodio y el potasio en la sangre
- Sensor portátil de bajo costo detecta metales pesados en el sudor
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... Más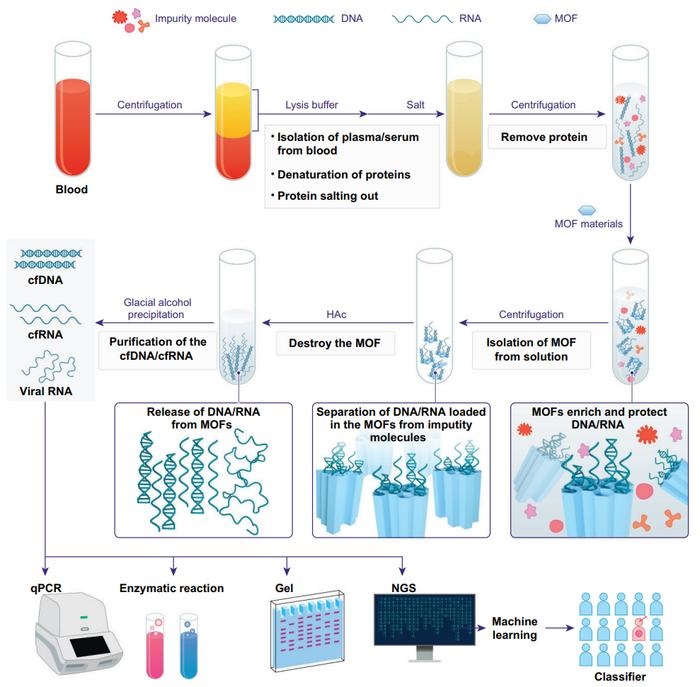
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)

.jpg)