Enfermedad de Alzheimer asintomática se puede detectar con el análisis del transcriptoma
|
Por el equipo editorial de LabMedica en español Actualizado el 07 Aug 2019 |
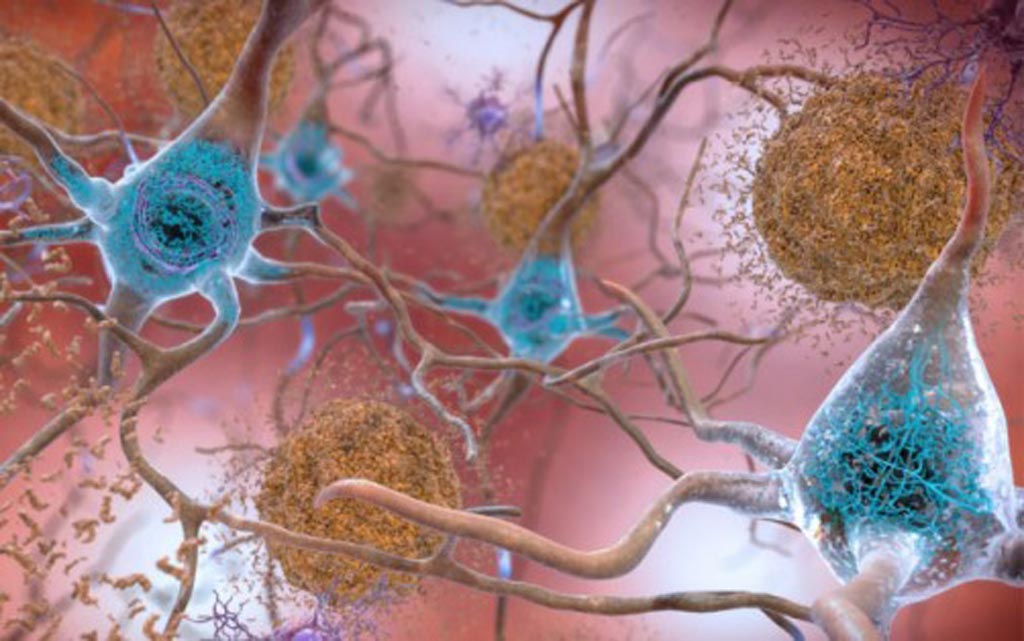
Imagen: En los cerebros afectados por la enfermedad de Alzheimer, los niveles anormales de la proteína beta-amiloide se agrupan para formar placas (vistas en marrón) que se acumulan entre las neuronas y alteran la función celular. Las acumulaciones anormales de la proteína tau forman ovillos (vistos en azul) dentro de las neuronas, dañando la comunicación sináptica entre las células nerviosas (Fotografía cortesía del Instituto Nacional sobre el Envejecimiento, EE. UU.).
Se usó el análisis de transcriptoma como un método para detectar individuos con enfermedad de Alzheimer (EA) que aún no mostraban síntomas del trastorno.
Actualmente no hay buenos métodos para detectar pacientes con EA asintomáticos a pesar del hecho de que pueden compartir cargas neuropatológicas similares a las de los individuos sintomáticos, mientras experimentan tasas significativamente diferentes de deterioro cognitivo.
Para desarrollar un método para diagnosticar a los pacientes con EA asintomáticos, los investigadores de la Universidad de California, San Diego (EUA) utilizaron el transcriptoma como un indicador del estado funcional y seleccionaron 414 perfiles de expresión de individuos con EA sintomáticos y de controles no dementes emparejados por edad de un estudio neuropatológico comunitario. Debido a que incluye todas las transcripciones de mARN en la célula, el transcriptoma refleja los genes que se expresan activamente en un momento dado. A diferencia del genoma, que se fija aproximadamente para una línea celular dada (excluyendo mutaciones), el transcriptoma puede variar con las condiciones ambientales externas.
Los resultados de la encuesta de transcriptoma revelaron que al combinar interactomas de proteínas específicas del tejido cerebral (un interactoma es el conjunto completo de interacciones moleculares en una célula particular) con las redes de genes, los investigadores pudieron identificar grupos compuestos de genes funcionalmente distintos que revelaron cambios extensos en los niveles de expresión en la EA. La expresión global para los grupos que corresponden en general a la transmisión sináptica, el metabolismo, el ciclo celular, la supervivencia y la respuesta inmune se reguló negativamente, mientras que el grupo regulado al alza incluyó procesos en gran medida no caracterizados.
Estos resultados resaltaron la utilidad de integrar interacciones de proteínas con perturbaciones genéticas para generar un marco integral para caracterizar las alteraciones en la red molecular aplicadas a la EA.
“Uno de los grandes problemas en la investigación de la EA es identificar a los pacientes en riesgo en el momento adecuado”, dijo el autor principal, el Dr. Robert Rissman, profesor de neurociencias en la Universidad de California en San Diego. “Comprender las redes de genes que pueden cambiar en los grupos específicos de pacientes puede ayudar a racionalizar los esfuerzos de reclutamiento de ensayos clínicos y reducir los costos y el tiempo para inscribir ensayos. Con el campo cambiando cada vez más hacia la enfermedad presintomática, necesitamos expandir nuestra comprensión de los mecanismos moleculares que subyacen en todo el espectro de la enfermedad”.
El estudio de análisis de transcriptoma se publicó en la edición del 23 de julio de 2019 de la revista Cell Reports.
Enlace relacionado:
Universidad de California, San Diego
Actualmente no hay buenos métodos para detectar pacientes con EA asintomáticos a pesar del hecho de que pueden compartir cargas neuropatológicas similares a las de los individuos sintomáticos, mientras experimentan tasas significativamente diferentes de deterioro cognitivo.
Para desarrollar un método para diagnosticar a los pacientes con EA asintomáticos, los investigadores de la Universidad de California, San Diego (EUA) utilizaron el transcriptoma como un indicador del estado funcional y seleccionaron 414 perfiles de expresión de individuos con EA sintomáticos y de controles no dementes emparejados por edad de un estudio neuropatológico comunitario. Debido a que incluye todas las transcripciones de mARN en la célula, el transcriptoma refleja los genes que se expresan activamente en un momento dado. A diferencia del genoma, que se fija aproximadamente para una línea celular dada (excluyendo mutaciones), el transcriptoma puede variar con las condiciones ambientales externas.
Los resultados de la encuesta de transcriptoma revelaron que al combinar interactomas de proteínas específicas del tejido cerebral (un interactoma es el conjunto completo de interacciones moleculares en una célula particular) con las redes de genes, los investigadores pudieron identificar grupos compuestos de genes funcionalmente distintos que revelaron cambios extensos en los niveles de expresión en la EA. La expresión global para los grupos que corresponden en general a la transmisión sináptica, el metabolismo, el ciclo celular, la supervivencia y la respuesta inmune se reguló negativamente, mientras que el grupo regulado al alza incluyó procesos en gran medida no caracterizados.
Estos resultados resaltaron la utilidad de integrar interacciones de proteínas con perturbaciones genéticas para generar un marco integral para caracterizar las alteraciones en la red molecular aplicadas a la EA.
“Uno de los grandes problemas en la investigación de la EA es identificar a los pacientes en riesgo en el momento adecuado”, dijo el autor principal, el Dr. Robert Rissman, profesor de neurociencias en la Universidad de California en San Diego. “Comprender las redes de genes que pueden cambiar en los grupos específicos de pacientes puede ayudar a racionalizar los esfuerzos de reclutamiento de ensayos clínicos y reducir los costos y el tiempo para inscribir ensayos. Con el campo cambiando cada vez más hacia la enfermedad presintomática, necesitamos expandir nuestra comprensión de los mecanismos moleculares que subyacen en todo el espectro de la enfermedad”.
El estudio de análisis de transcriptoma se publicó en la edición del 23 de julio de 2019 de la revista Cell Reports.
Enlace relacionado:
Universidad de California, San Diego
Últimas Patología noticias
- Innovador dispositivo de extracción de sangre supera obstáculos comunes relacionados con la flebotomía
- Dispositivo POC intraoperatorio distingue entre quistes ováricos benignos y malignos en 15 minutos
- Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
- Herramienta bioinformática para identificar alteraciones cromosómicas en células tumorales puede mejorar diagnóstico del cáncer
- Dispositivo del tamaño de una moneda aísla rápidamente plasma sanguíneo para diagnósticos clínicos más rápidos y precisos
- IA predice propagación del cáncer al cerebro a partir de imágenes de biopsia de pulmón
- Tecnología de microagujas mejorada acelera extracción de muestra de líquido intersticial para diagnóstico de enfermedades
- IA supera a patólogos expertos en predicción de propagación del cáncer de pulmón
- Primer prototipo para aplicar IA al diagnóstico colorrectal
- Nueva prueba identifica cánceres de ovario agresivos más temprano
- Instrumento compacto de detección fotoacústica mejora diagnóstico biomédico de tejidos
- Dispositivo de esponja en cápsula no endoscópica ayuda a detectar cáncer de esófago
- Sistema de citología digital ofrece tecnología de próxima generación para prueba de Papanicolaou
- Red neuronal reconoce cáncer de mama en muestras histológicas con 100 % de precisión
- Modelo de aprendizaje automático calcula éxito de quimioterapia en pacientes con cáncer de hueso
- Herramienta de IA analiza rápidamente actividades genéticas en imágenes médicas para resaltar cánceres ocultos
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... Más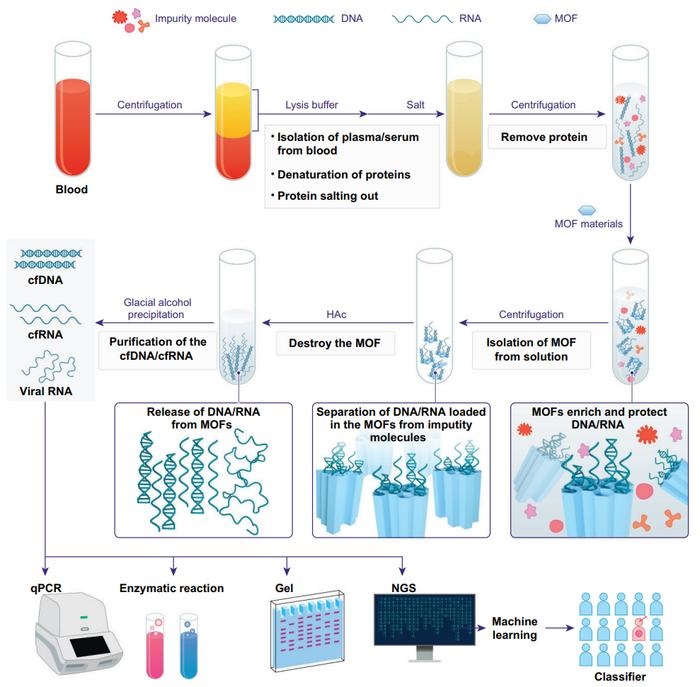
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)

.jpg)