Modelo de aprendizaje automático calcula éxito de quimioterapia en pacientes con cáncer de hueso
Actualizado el 17 Jan 2024
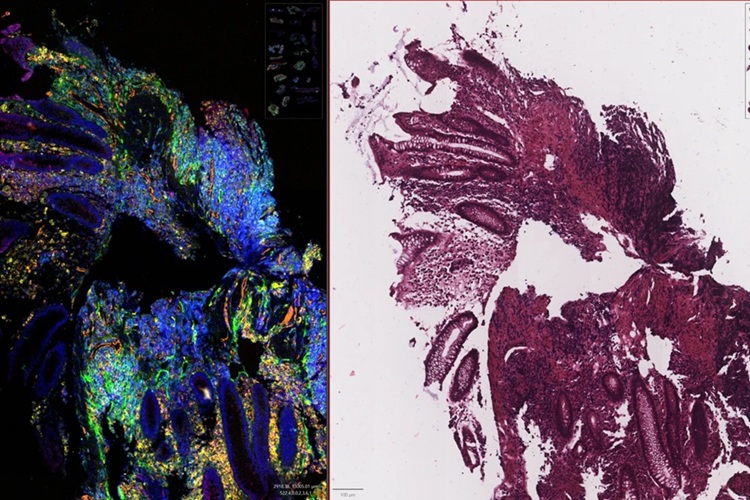
El cálculo del porcentaje de necrosis (PN), la proporción de un tumor considerado inactivo o "muerto" después de la quimioterapia, sirve como un predictor vital de los resultados de supervivencia en el osteosarcoma, un tipo de cáncer de huesos. Por ejemplo, una PN del 99 % significa que el 99 % del tumor está muerto, lo que indica la respuesta positiva del paciente a la quimioterapia y perspectivas de supervivencia potencialmente mejores. Los patólogos suelen evaluar la PN examinando, interpretando y marcando meticulosamente imágenes de portaobjetos completos (WSI), que son secciones transversales detalladas de muestras (como tejido óseo) preparadas para un examen microscópico. Sin embargo, este método tradicional no sólo requiere mucho tiempo y experiencia especializada, sino que también sufre una variabilidad significativa entre los observadores. Esto significa que dos patólogos podrían informar estimaciones de PN diferentes de la misma WSI. Ahora, un modelo de aprendizaje automático creado y entrenado para calcular el PN ha demostrado que su cálculo fue 85 % correcto en comparación con los resultados de un patólogo musculoesquelético, y la precisión mejoró al 99 % al excluir un valor atípico.
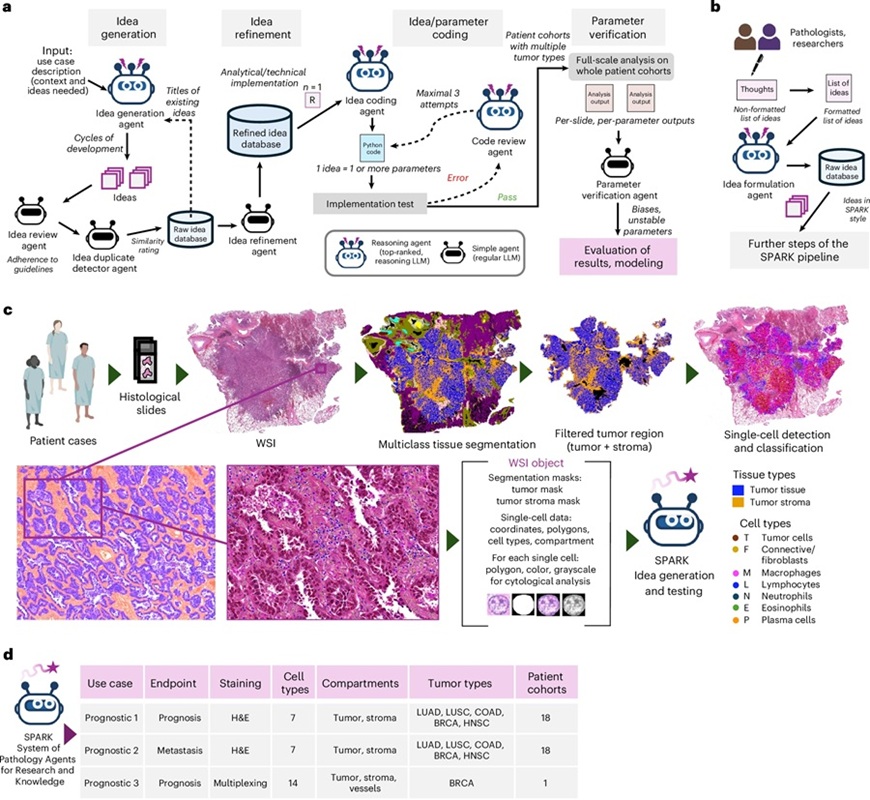
Un equipo de investigación de Johns Hopkins Medicine (Baltimore, MD, EUA) está desarrollando un modelo de aprendizaje automático "débilmente supervisado", que no requiere muchos datos anotados para su entrenamiento. Al hacerlo, un patólogo sólo necesitaría proporcionar WSI parcialmente anotados, lo que aliviaría significativamente su carga de trabajo. Para desarrollar el modelo de aprendizaje automático, el equipo comenzó recopilando WSI de pacientes con osteosarcoma intramedular (que se origina dentro del hueso) tratados con quimioterapia y cirugía entre 2011 y 2021. Luego, un patólogo musculoesquelético etiquetó parcialmente tres tipos de tejido en estas WSI: tumor activo, tumor muerto y tejido no tumoral y también proporcionó una estimación de PN para cada caso. Estos datos formaron la base para el entrenamiento del modelo.
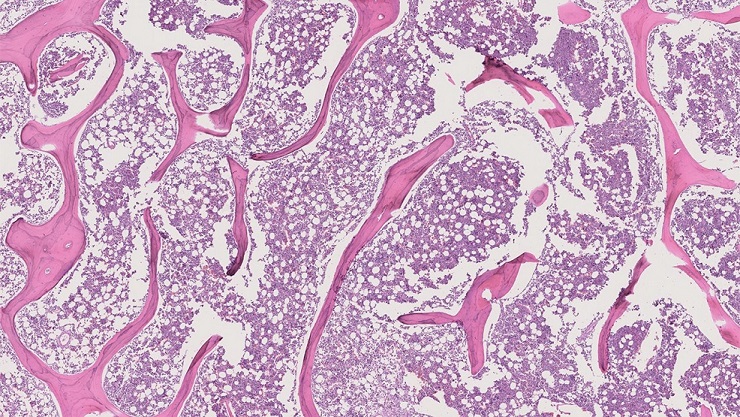
El modelo fue entrenado para reconocer y categorizar patrones de imágenes. Las WSI se segregaron en miles de parches más pequeños, se dividieron en grupos según las etiquetas del patólogo y luego alimentaron al modelo. Este proceso tuvo como objetivo proporcionar al modelo un marco de referencia más sólido en lugar de simplemente alimentarlo con una gran WSI. Al finalizar el entrenamiento, el modelo se probó junto con el patólogo musculoesquelético en seis WSI de dos pacientes. Los resultados demostraron una correlación del 85 % en los cálculos de PN y el etiquetado de tejidos entre el modelo y el patólogo. Sin embargo, el modelo tuvo dificultades para etiquetar el cartílago con precisión, lo que generó un valor atípico como resultado de la abundancia de cartílago en una WSI. Cuando se eliminó este valor atípico, la correlación se elevó al 99 %. El trabajo futuro se centrará en incorporar tejido cartilaginoso en el entrenamiento del modelo y ampliar la gama de WSI para abarcar varios tipos de osteosarcoma, no solo el intramedular.
"Si este modelo fuera validado y producido, podría ayudar a acelerar la evaluación de la efectividad de la quimioterapia en un paciente y, por lo tanto, brindarle una estimación del pronóstico con anterioridad", dijo la Dra. Christa LiBrizzi, coprimera autora del estudio y residente del Departamento de Cirugía Ortopédica de Johns Hopkins Medicine. "Eso reduciría los costos de atención médica, así como la carga laboral de los patólogos musculoesqueléticos".
Enlaces relacionados:
Johns Hopkins Medicine