Se identifica la base genética de las cardiomiopatías de inicio infantil
|
Por el equipo editorial de LabMedica en español Actualizado el 28 Nov 2018 |
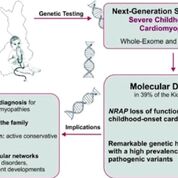
Imagen: Un diagrama de la cohorte KidCMP de niños con cardiomiopatías graves de los últimos 21 años que fueron analizados genéticamente (Fotografía cortesía de Catalina Vasilescu/Universidad de Helsinki).
La medicina personalizada es uno de los objetivos de los estudios médicos actuales, donde la comprensión de la causa genética y el mecanismo de la enfermedad en cada individuo promoverán formas de tratamiento a la medida. Los investigadores dieron un paso importante en esta dirección al descifrar las causas genéticas en los niños y sus implicaciones para las decisiones de tratamiento.
La degeneración del músculo cardíaco (cardiomiopatía) es la causa más común de disfunción cardíaca grave y arritmias cardíacas potencialmente mortales en los niños. Estos trastornos graves a menudo conducen a considerar la posibilidad de un trasplante de corazón. Sin embargo, su causa real, la base genética, ha sido mal caracterizada.
Un esfuerzo de colaboración de cardiólogos pediátricos del Hospital Universitario de Helsinki (Helsinki, Finlandia) y de la Universidad de Helsinki (Helsinki, Finlandia) logró reunir una cohorte con KidCMP, única a nivel mundial, de 66 niños con cardiomiopatías severas de los últimos 21 años, y las analizaron genéticamente. La cohorte KidCMP presenta trastornos de aparición temprana y graves notables: la edad media de diagnóstico fue de 0,33 años y en 17 pacientes se practicó un trasplante cardíaco. Para el diagnóstico genético, se utilizaron la secuenciación de la próxima generación y la validación posterior utilizando métodos genéticos, de biología celular y computacionales.
El equipo identificó las variantes patógenas en el 39% de los pacientes: 46% de novo, 34% de herencia recesiva y 20% de herencia dominante. Informaron miocardiopatías dilatadas infantiles, subyacentes al gen NRAP así como fenotipos nuevos de genes conocidos de producir enfermedades del corazón. Algunos diagnósticos genéticos tienen implicaciones inmediatas para el tratamiento: CALM1 con arritmias que ponen en peligro la vida y TAZ con buen pronóstico cardíaco. Los genes de la enfermedad convergen en causas metabólicas (PRKAG2, MRPL44, AARS2, HADHB, DNAJC19, PPA2, TAZ, BAG3), vías MAPK (HRAS, PTPN11, RAF1, TAB2), vías de desarrollo (NEK8 y TBX20), vías de señalización de calcio (JPH2, CALM1, CACNA1C), y la vía del ciclo de contracción sarcomérica (TNNC1, TNNI3, ACTC1, MYH7, NRAP).
Los autores concluyeron que las cardiomiopatías infantiles suelen ser causadas por mutaciones raras específicas de la familia, más comúnmente de novo, lo que indica que la secuenciación de próxima generación de tríos es el método de elección en su diagnóstico. Los diagnósticos genéticos pueden sugerir estrategias de intervención y predecir el pronóstico, ofreciendo herramientas valiosas para la priorización de pacientes para trasplante versus tratamiento conservador.
Tiina Ojala, MD, PhD, cardióloga pediátrica y autora principal del estudio, dijo: “Todos los niños tenían enfermedades potencialmente mortales desde el principio y algunos defectos genéticos predecían un trastorno principalmente progresivo que requería trasplante cardíaco. Sin embargo, si se tratan de forma intensiva, algunos defectos genéticos predecían un curso de recuperación, sin necesidad de trasplante”. El estudio fue publicado en la edición de noviembre de 2018 de la revista Journal of the American College of Cardiology.
Enlace relacionado:
Hospital Universitario de Helsinki
Universidad de Helsinki
La degeneración del músculo cardíaco (cardiomiopatía) es la causa más común de disfunción cardíaca grave y arritmias cardíacas potencialmente mortales en los niños. Estos trastornos graves a menudo conducen a considerar la posibilidad de un trasplante de corazón. Sin embargo, su causa real, la base genética, ha sido mal caracterizada.
Un esfuerzo de colaboración de cardiólogos pediátricos del Hospital Universitario de Helsinki (Helsinki, Finlandia) y de la Universidad de Helsinki (Helsinki, Finlandia) logró reunir una cohorte con KidCMP, única a nivel mundial, de 66 niños con cardiomiopatías severas de los últimos 21 años, y las analizaron genéticamente. La cohorte KidCMP presenta trastornos de aparición temprana y graves notables: la edad media de diagnóstico fue de 0,33 años y en 17 pacientes se practicó un trasplante cardíaco. Para el diagnóstico genético, se utilizaron la secuenciación de la próxima generación y la validación posterior utilizando métodos genéticos, de biología celular y computacionales.
El equipo identificó las variantes patógenas en el 39% de los pacientes: 46% de novo, 34% de herencia recesiva y 20% de herencia dominante. Informaron miocardiopatías dilatadas infantiles, subyacentes al gen NRAP así como fenotipos nuevos de genes conocidos de producir enfermedades del corazón. Algunos diagnósticos genéticos tienen implicaciones inmediatas para el tratamiento: CALM1 con arritmias que ponen en peligro la vida y TAZ con buen pronóstico cardíaco. Los genes de la enfermedad convergen en causas metabólicas (PRKAG2, MRPL44, AARS2, HADHB, DNAJC19, PPA2, TAZ, BAG3), vías MAPK (HRAS, PTPN11, RAF1, TAB2), vías de desarrollo (NEK8 y TBX20), vías de señalización de calcio (JPH2, CALM1, CACNA1C), y la vía del ciclo de contracción sarcomérica (TNNC1, TNNI3, ACTC1, MYH7, NRAP).
Los autores concluyeron que las cardiomiopatías infantiles suelen ser causadas por mutaciones raras específicas de la familia, más comúnmente de novo, lo que indica que la secuenciación de próxima generación de tríos es el método de elección en su diagnóstico. Los diagnósticos genéticos pueden sugerir estrategias de intervención y predecir el pronóstico, ofreciendo herramientas valiosas para la priorización de pacientes para trasplante versus tratamiento conservador.
Tiina Ojala, MD, PhD, cardióloga pediátrica y autora principal del estudio, dijo: “Todos los niños tenían enfermedades potencialmente mortales desde el principio y algunos defectos genéticos predecían un trastorno principalmente progresivo que requería trasplante cardíaco. Sin embargo, si se tratan de forma intensiva, algunos defectos genéticos predecían un curso de recuperación, sin necesidad de trasplante”. El estudio fue publicado en la edición de noviembre de 2018 de la revista Journal of the American College of Cardiology.
Enlace relacionado:
Hospital Universitario de Helsinki
Universidad de Helsinki
Últimas Patología noticias
- Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
- Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
- Innovador dispositivo de extracción de sangre supera obstáculos comunes relacionados con la flebotomía
- Dispositivo POC intraoperatorio distingue entre quistes ováricos benignos y malignos en 15 minutos
- Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
- Herramienta bioinformática para identificar alteraciones cromosómicas en células tumorales puede mejorar diagnóstico del cáncer
- Dispositivo del tamaño de una moneda aísla rápidamente plasma sanguíneo para diagnósticos clínicos más rápidos y precisos
- IA predice propagación del cáncer al cerebro a partir de imágenes de biopsia de pulmón
- Tecnología de microagujas mejorada acelera extracción de muestra de líquido intersticial para diagnóstico de enfermedades
- IA supera a patólogos expertos en predicción de propagación del cáncer de pulmón
- Primer prototipo para aplicar IA al diagnóstico colorrectal
- Nueva prueba identifica cánceres de ovario agresivos más temprano
- Instrumento compacto de detección fotoacústica mejora diagnóstico biomédico de tejidos
- Dispositivo de esponja en cápsula no endoscópica ayuda a detectar cáncer de esófago
- Sistema de citología digital ofrece tecnología de próxima generación para prueba de Papanicolaou
- Red neuronal reconoce cáncer de mama en muestras histológicas con 100 % de precisión
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal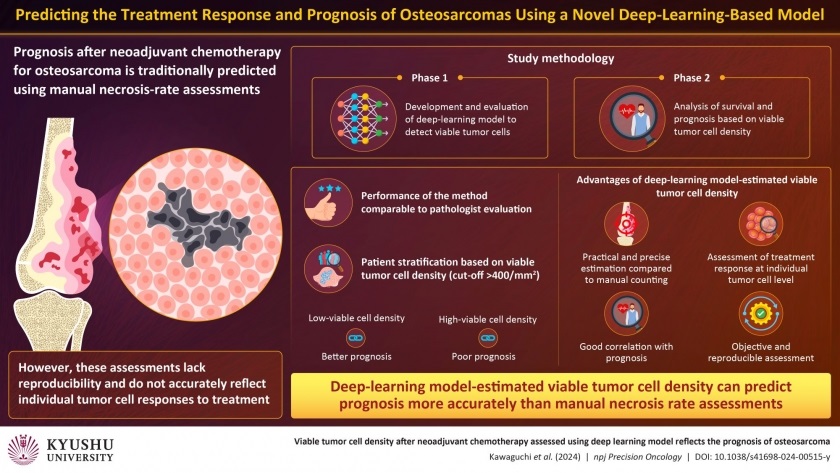
Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico... Más
Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
La comunidad médica mundial reconoce cada vez más que la biopsia líquida es un enfoque transformador para mejorar la atención al paciente con cáncer. Este innovador método de diagnóstico implica detectar... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más











.jpg)

.jpg)