Marcadores plasmáticos predicen carga de amiloide cerebral en Alzheimer
|
Por el equipo editorial de LabMedica en español Actualizado el 07 Mar 2018 |

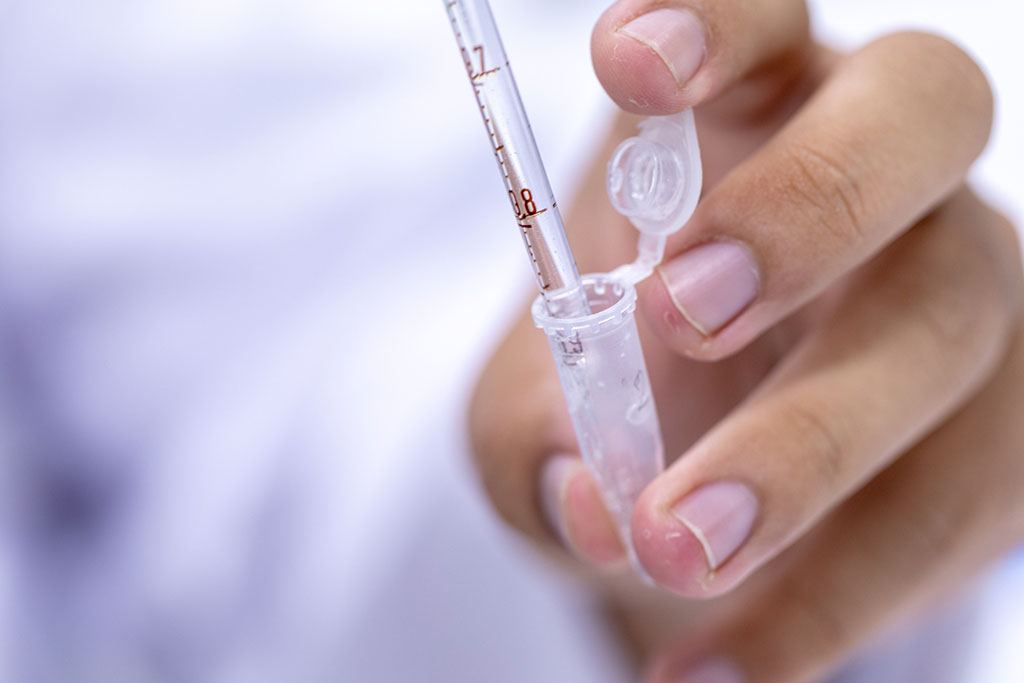
Imagen: El espectrómetro de masas con tiempo de vuelo de desorción/ionización láser asistido por matriz (MALDI) (Fotografía cortesía de JEOL).
La agregación y acumulación de beta-amiloide (Aβ), particularmente Aβ42, están implicadas en la patogénesis de la enfermedad de Alzheimer (EA) con una producción exagerada en los casos de EA autosómica dominante y alteración de la depuración en presencia de amiloidosis que contribuye a la causa de la EA.
El análisis del líquido cefalorraquídeo y otras mediciones de la amiloidosis, como los estudios de tomografía por emisión de positrones con unión del amiloide, están limitados por el costo y la disponibilidad. Existe la necesidad de un biomarcador beta-amiloide (Aβ) más práctico para determinar los depósitos de amiloide en el sistema nervioso central.
Un equipo internacional de científicos que trabajan con el Centro Nacional Japonés de Geriatría y Gerontología (Obu, Japón) utilizó la inmunoprecipitación seguida de la espectrometría de masas por desorción/ionización láser asistida por matriz (MALDI) para medir los niveles de los tres marcadores, APP669-711, Aβ42 y Aβ40 en dos cohortes: un conjunto de descubrimiento consistente en 121 pacientes japoneses y un conjunto de validación consistente en 252 pacientes australianos. Ambos conjuntos incluyeron una mezcla de individuos cognitivamente normales, individuos con deterioro cognitivo leve e individuos con enfermedad de Alzheimer diagnosticada clínicamente con demencia. Todos los pacientes también tenían datos de imágenes de tomografía por emisión de positrones (TEP) Aβ, proporcionando una evaluación de sus cargas cerebrales de Aβ. A un subconjunto de pacientes australianos también se les tomaron medidas de los niveles de Aβ en el líquido cefalorraquídeo.
El equipo evaluó las relaciones de los tres marcadores para desarrollar un marcador compuesto de sangre correspondiente a los niveles cerebrales de Aβ evaluados por la TEP y las mediciones de líquido cefalorraquídeo (LCR). Utilizaron relaciones en oposición a las mediciones absolutas para tener en cuenta la variación individual en los niveles sanguíneos de Aβ42 en los individuos. Un compuesto de las tres proporciones de proteínas plasmáticas se correspondía bien con los niveles de Aβ42 en el LCR en los pacientes y los niveles de Aβ42 en el cerebro, determinados usando la TEP. Utilizando las mediciones de TEP como el estándar de oro, los investigadores encontraron que sus mediciones de plasma tenían un desempeño comparable a las mediciones en el LCR, con ambas mostrando una exactitud del 80,4% y áreas bajo la curva de 83,8% y 87,4% para las mediciones de sangre y LCR, respectivamente. Utilizando las mediciones de LCR como el estándar de oro, los marcadores de plasma compuestos mostraron una exactitud del 80,4% y un AUC de 87,6.
Los autores concluyeron que sus resultados demostraron la utilidad clínica potencial de los biomarcadores plasmáticos para predecir la carga de beta-amiloide cerebral a nivel individual. Estos biomarcadores plasmáticos también tienen ventajas de costo-beneficio y escalabilidad sobre las técnicas actuales, lo que posibilita un acceso clínico más amplio y un cribado eficiente de la población. El estudio fue publicado el 31 de enero de 2018 en la revista Nature.
El análisis del líquido cefalorraquídeo y otras mediciones de la amiloidosis, como los estudios de tomografía por emisión de positrones con unión del amiloide, están limitados por el costo y la disponibilidad. Existe la necesidad de un biomarcador beta-amiloide (Aβ) más práctico para determinar los depósitos de amiloide en el sistema nervioso central.
Un equipo internacional de científicos que trabajan con el Centro Nacional Japonés de Geriatría y Gerontología (Obu, Japón) utilizó la inmunoprecipitación seguida de la espectrometría de masas por desorción/ionización láser asistida por matriz (MALDI) para medir los niveles de los tres marcadores, APP669-711, Aβ42 y Aβ40 en dos cohortes: un conjunto de descubrimiento consistente en 121 pacientes japoneses y un conjunto de validación consistente en 252 pacientes australianos. Ambos conjuntos incluyeron una mezcla de individuos cognitivamente normales, individuos con deterioro cognitivo leve e individuos con enfermedad de Alzheimer diagnosticada clínicamente con demencia. Todos los pacientes también tenían datos de imágenes de tomografía por emisión de positrones (TEP) Aβ, proporcionando una evaluación de sus cargas cerebrales de Aβ. A un subconjunto de pacientes australianos también se les tomaron medidas de los niveles de Aβ en el líquido cefalorraquídeo.
El equipo evaluó las relaciones de los tres marcadores para desarrollar un marcador compuesto de sangre correspondiente a los niveles cerebrales de Aβ evaluados por la TEP y las mediciones de líquido cefalorraquídeo (LCR). Utilizaron relaciones en oposición a las mediciones absolutas para tener en cuenta la variación individual en los niveles sanguíneos de Aβ42 en los individuos. Un compuesto de las tres proporciones de proteínas plasmáticas se correspondía bien con los niveles de Aβ42 en el LCR en los pacientes y los niveles de Aβ42 en el cerebro, determinados usando la TEP. Utilizando las mediciones de TEP como el estándar de oro, los investigadores encontraron que sus mediciones de plasma tenían un desempeño comparable a las mediciones en el LCR, con ambas mostrando una exactitud del 80,4% y áreas bajo la curva de 83,8% y 87,4% para las mediciones de sangre y LCR, respectivamente. Utilizando las mediciones de LCR como el estándar de oro, los marcadores de plasma compuestos mostraron una exactitud del 80,4% y un AUC de 87,6.
Los autores concluyeron que sus resultados demostraron la utilidad clínica potencial de los biomarcadores plasmáticos para predecir la carga de beta-amiloide cerebral a nivel individual. Estos biomarcadores plasmáticos también tienen ventajas de costo-beneficio y escalabilidad sobre las técnicas actuales, lo que posibilita un acceso clínico más amplio y un cribado eficiente de la población. El estudio fue publicado el 31 de enero de 2018 en la revista Nature.
Últimas Química Clínica noticias
- Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
- Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
- Nuevo método de análisis de sangre detecta opioides potentes en menos de tres minutos
- Kit inalámbrico de prueba de hepatitis B completa detección y recopilación de datos en un solo paso
- Dispositivo sensible, indoloro, de bajo costo y sin radiación detecta cáncer de mama en orina
- Prueba de saliva detecta cáncer de mama en cinco segundos
- Sensores electroquímicos con recubrimiento de próxima generación avanzan en diagnóstico de precisión POC
- Dispositivo portátil, primero de su tipo, detecta con precisión fentanilo en orina en segundos
- Nueva matriz de sensores fluorescentes ilumina proteínas relacionadas con el Alzheimer para detección más temprana
- Analizador clínico automatizado basado en espectrometría de masas podría transformar pruebas de laboratorio
- Sensor de pH altamente sensible ayuda a detectar cánceres y virus transmitidos por vectores
- Sensor no invasivo monitorea cambios en composiciones de saliva para diagnosticar diabetes rápidamente
- Innovadores Inmunoensayos ayudan en evaluación del riesgo de preeclampsia
- La AACC publica pautas completas para pruebas de diabetes
- Prueba de orina para monitorear cambios en marcadores de salud renal puede predecir insuficiencia cardíaca de nueva aparición
- Analizador compacto de inmunoensayo y química clínica ayuda a laboratorios bajo y medio volumen a abordar los desafíos
Canales
Diagnóstico Molecular
ver canal
Enfoque revolucionario de análisis de células T permite detección temprana del cáncer
La biopsia líquida, un método para diagnosticar el cáncer mediante análisis de sangre de rutina, es una herramienta potencial importante para la detección temprana del... MásPrueba genética única podría acelerar el diagnóstico de trastornos raros del desarrollo
Las alteraciones en el ADN humano varían desde variaciones menores de un solo nucleótido hasta alteraciones sustanciales que implican la eliminación o duplicación de segmentos... Más
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal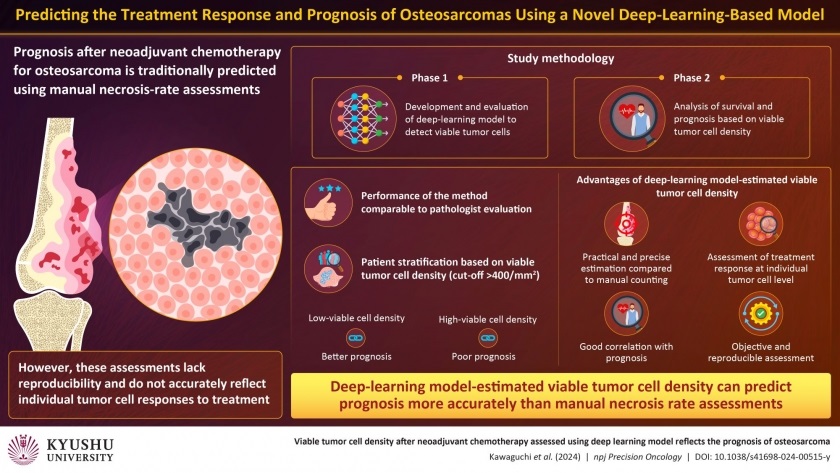
Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico... Más
Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
La comunidad médica mundial reconoce cada vez más que la biopsia líquida es un enfoque transformador para mejorar la atención al paciente con cáncer. Este innovador método de diagnóstico implica detectar... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)