Técnica de microscopía permite más biopsias informativas
|
Por el equipo editorial de LabMedica en español Actualizado el 14 Aug 2017 |
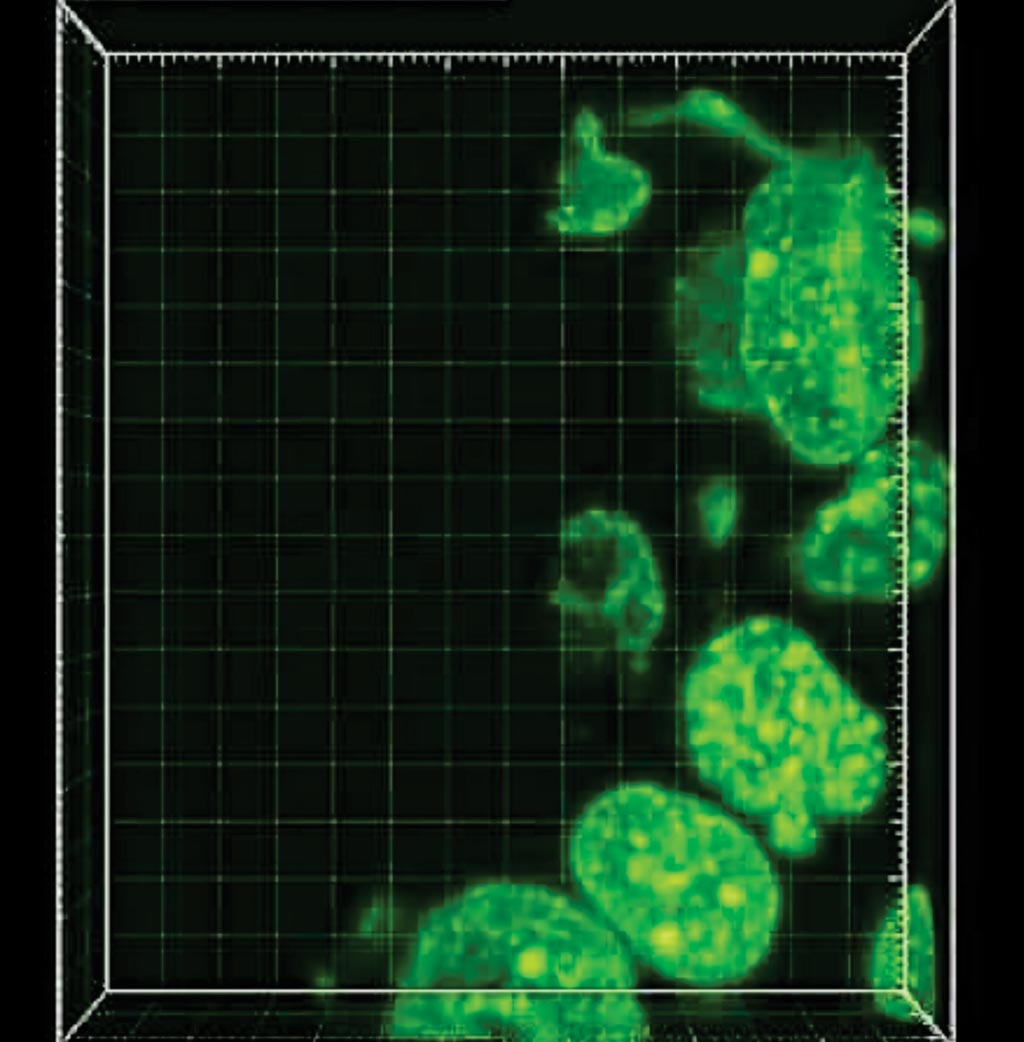
Imagen: La técnica de patología de expansión (ExPath) muestra el tejido expandido del cáncer de mama, facilitando la visualización de los núcleos en 3D (Fotografía cortesía del Instituto Ludwig para la Investigación del Cáncer).
La microscopía de expansión (ExM), es un método para mejorar la resolución de la microscopía óptica mediante la expansión física de una muestra, pero esta técnica no ha sido aplicada a muestras de tejido clínico. En este método ExM, una muestra de tejido se expande hasta 100 veces su volumen original, antes de empezar a ver las imágenes.
Esta expansión permite a los científicos ver las características, con un microscopio de luz convencional, que normalmente sólo se podrían ver con un microscopio electrónico costoso. También revela información molecular adicional que el microscopio electrónico no puede proporcionar.
Los científicos del Instituto Tecnológico de Massachusetts (Cambridge, MA, EUA) y sus colegas, desarrollaron una forma clínicamente optimizada de ExM que permite ver las imágenes en nanoescala de muestras de tejidos humanos que se han fijado con formol, han sido incluidas en parafina, coloreadas con hematoxilina y eosina, y/o se han mantenido congeladas o frescas. El método, que denominan patología de expansión (ExPath), convierte las muestras clínicas en un estado compatible con ExM, luego aplica un protocolo ExM con anclaje de proteínas y pasos de homogeneización mecánica optimizados para muestras clínicas.
El equipo ensayó este método en muestras de tejidos de pacientes con lesiones mamarias en etapas tempranas. Una forma de predecir si estas lesiones se convertirán en malignas es evaluar la apariencia de los núcleos de las células. Las lesiones benignas con núcleos atípicos tienen aproximadamente una probabilidad cinco veces mayor de progresar a cáncer que aquellas que muestran núcleos típicos. Sin embargo, los estudios han revelado discrepancias significativas entre las evaluaciones de las atipias nucleares realizadas por diferentes patólogos, que pueden conducir potencialmente a un diagnóstico inexacto y cirugía innecesaria. ExPath permite obtener imágenes con ~ 70 nm de resolución de diversas biomoléculas en tejidos intactos usando microscopios convencionales de difracción limitada, anticuerpos estándar y reactivos de hibridación fluorescente in situ.
Después de expandir las muestras de tejido, los científicos las analizaron con un algoritmo de aprendizaje automático que puede clasificar los núcleos con base en docenas de características, incluyendo orientación, diámetro y cuánto se desvían de la circularidad verdadera. Este algoritmo fue capaz de diferenciar entre las lesiones que tenían mucha probabilidad de convertirse en invasoras y las que no lo eran, con una exactitud del 93% en las muestras expandidas, en comparación con sólo el 71% en el tejido pre-expandido. También analizaron muestras de tejido renal de pacientes con síndrome nefrótico y cuando mostraron las imágenes de las muestras de tejido expandido a un grupo de científicos que incluía patólogos y no patólogos, el grupo fue capaz de identificar el tejido enfermo con un 90% de exactitud, en comparación con solo 65% de exactitud en las muestras de tejidos no expandidas.
Edward S. Boyden, PhD, un profesor de Ingeniería Biológica y coautor principal del estudio, dijo: “Ahora usted puede diagnosticar la enfermedad renal nefrótica sin necesidad de un microscopio electrónico, una máquina muy cara. Usted puede hacerlo con unos pocos productos químicos y un microscopio de luz. Si se puede ampliar un tejido por cien veces en volumen, manteniendo todas las demás cosas iguales, obtendrá 100 veces la cantidad de información”. El estudio fue publicado el 17 de julio de 2017 en la revista Nature Biotechnology.
Esta expansión permite a los científicos ver las características, con un microscopio de luz convencional, que normalmente sólo se podrían ver con un microscopio electrónico costoso. También revela información molecular adicional que el microscopio electrónico no puede proporcionar.
Los científicos del Instituto Tecnológico de Massachusetts (Cambridge, MA, EUA) y sus colegas, desarrollaron una forma clínicamente optimizada de ExM que permite ver las imágenes en nanoescala de muestras de tejidos humanos que se han fijado con formol, han sido incluidas en parafina, coloreadas con hematoxilina y eosina, y/o se han mantenido congeladas o frescas. El método, que denominan patología de expansión (ExPath), convierte las muestras clínicas en un estado compatible con ExM, luego aplica un protocolo ExM con anclaje de proteínas y pasos de homogeneización mecánica optimizados para muestras clínicas.
El equipo ensayó este método en muestras de tejidos de pacientes con lesiones mamarias en etapas tempranas. Una forma de predecir si estas lesiones se convertirán en malignas es evaluar la apariencia de los núcleos de las células. Las lesiones benignas con núcleos atípicos tienen aproximadamente una probabilidad cinco veces mayor de progresar a cáncer que aquellas que muestran núcleos típicos. Sin embargo, los estudios han revelado discrepancias significativas entre las evaluaciones de las atipias nucleares realizadas por diferentes patólogos, que pueden conducir potencialmente a un diagnóstico inexacto y cirugía innecesaria. ExPath permite obtener imágenes con ~ 70 nm de resolución de diversas biomoléculas en tejidos intactos usando microscopios convencionales de difracción limitada, anticuerpos estándar y reactivos de hibridación fluorescente in situ.
Después de expandir las muestras de tejido, los científicos las analizaron con un algoritmo de aprendizaje automático que puede clasificar los núcleos con base en docenas de características, incluyendo orientación, diámetro y cuánto se desvían de la circularidad verdadera. Este algoritmo fue capaz de diferenciar entre las lesiones que tenían mucha probabilidad de convertirse en invasoras y las que no lo eran, con una exactitud del 93% en las muestras expandidas, en comparación con sólo el 71% en el tejido pre-expandido. También analizaron muestras de tejido renal de pacientes con síndrome nefrótico y cuando mostraron las imágenes de las muestras de tejido expandido a un grupo de científicos que incluía patólogos y no patólogos, el grupo fue capaz de identificar el tejido enfermo con un 90% de exactitud, en comparación con solo 65% de exactitud en las muestras de tejidos no expandidas.
Edward S. Boyden, PhD, un profesor de Ingeniería Biológica y coautor principal del estudio, dijo: “Ahora usted puede diagnosticar la enfermedad renal nefrótica sin necesidad de un microscopio electrónico, una máquina muy cara. Usted puede hacerlo con unos pocos productos químicos y un microscopio de luz. Si se puede ampliar un tejido por cien veces en volumen, manteniendo todas las demás cosas iguales, obtendrá 100 veces la cantidad de información”. El estudio fue publicado el 17 de julio de 2017 en la revista Nature Biotechnology.
Últimas Patología noticias
- Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
- Herramienta bioinformática para identificar alteraciones cromosómicas en células tumorales puede mejorar diagnóstico del cáncer
- Dispositivo del tamaño de una moneda aísla rápidamente plasma sanguíneo para diagnósticos clínicos más rápidos y precisos
- IA predice propagación del cáncer al cerebro a partir de imágenes de biopsia de pulmón
- Tecnología de microagujas mejorada acelera extracción de muestra de líquido intersticial para diagnóstico de enfermedades
- IA supera a patólogos expertos en predicción de propagación del cáncer de pulmón
- Primer prototipo para aplicar IA al diagnóstico colorrectal
- Nueva prueba identifica cánceres de ovario agresivos más temprano
- Instrumento compacto de detección fotoacústica mejora diagnóstico biomédico de tejidos
- Dispositivo de esponja en cápsula no endoscópica ayuda a detectar cáncer de esófago
- Sistema de citología digital ofrece tecnología de próxima generación para prueba de Papanicolaou
- Red neuronal reconoce cáncer de mama en muestras histológicas con 100 % de precisión
- Modelo de aprendizaje automático calcula éxito de quimioterapia en pacientes con cáncer de hueso
- Herramienta de IA analiza rápidamente actividades genéticas en imágenes médicas para resaltar cánceres ocultos
- Diagnóstico de patología digital impulsado por IA para biomarcador de cáncer colorrectal podría optimizar acceso del paciente a inmunoterapia
- Modelo de IA para clasificación de tumores cerebrales avanza en neuropatología
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal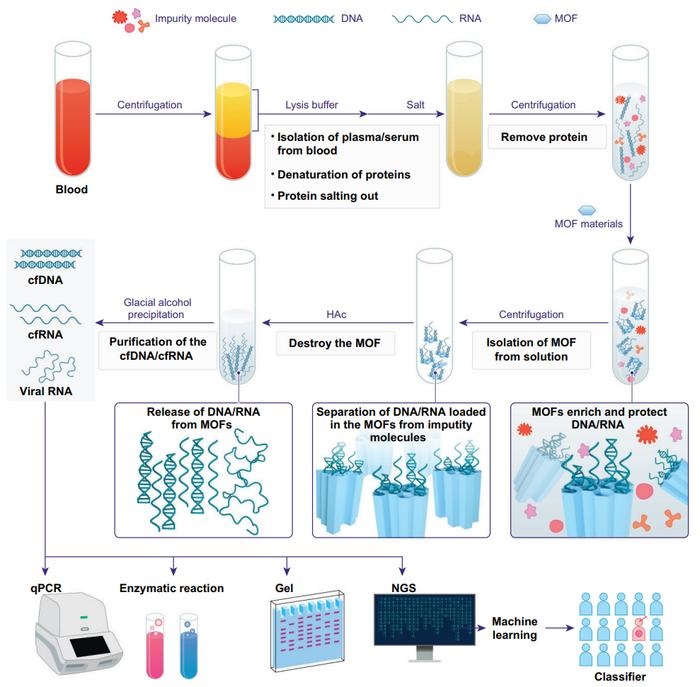
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más











.jpg)
.jpg)

.jpg)