Prueba no invasiva determina estado RhD fetal a partir del plasma materno
|
Por el equipo editorial de LabMedica en español Actualizado el 08 Dec 2024 |

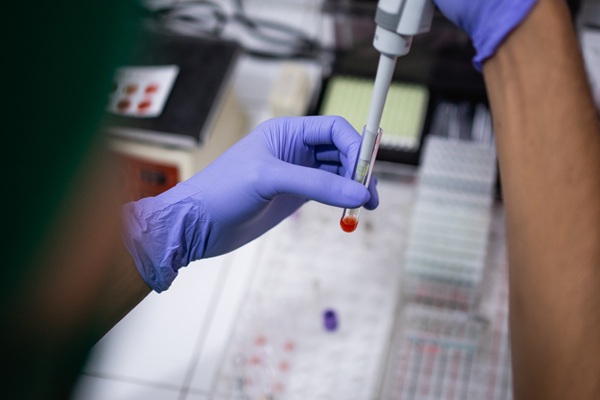
El RhD (rhesus D) es un tipo de grupo sanguíneo que puede desencadenar respuestas inmunitarias. Las personas que carecen de RhD en sus glóbulos rojos se clasifican como RhD-negativas. Estas personas pueden producir anticuerpos contra el RhD si entran en contacto con glóbulos rojos RhD-positivos. La incompatibilidad RhD entre una madre y su feto es la principal causa de enfermedad hemolítica fetal y neonatal (EHFN), y es la única causa prevenible. Desde la introducción de la profilaxis anti-RhD en la década de 1960, la prevalencia de la EHFN ha disminuido significativamente. En muchos países, todas las madres RhD-negativas reciben tratamiento para prevenir la aloinmunización. Sin embargo, alrededor del 40 % de estas mujeres tienen un feto RhD-negativo, lo que hace que la profilaxis sea innecesaria para muchas. Determinar el estado RhD fetal permite a los médicos adaptar el tratamiento anti-RhD, asegurando que se administre solo cuando sea necesario para prevenir el riesgo de enfermedad hemolítica. Ahora, una prueba confiable, altamente sensible y precisa ofrece una detección no invasiva del RhD fetal en mujeres embarazadas, lo que ayuda a evitar tratamientos profilácticos innecesarios.
El ensayo Devyser RHD, desarrollado por Devyser (Estocolmo, Suecia) es una prueba de PCR cuantitativa con marcado CE-IVD de alta sensibilidad que proporciona una detección no invasiva precisa del RhD fetal, lo que permite a los médicos evitar tratamientos innecesarios. Esta prueba única determina el estado RhD fetal a partir del plasma materno ya en la décima semana de embarazo. El kit de un solo exón tiene un tiempo de respuesta de menos de cinco horas y requiere menos de 60 minutos de tiempo de trabajo práctico. Con una detección temprana, los médicos pueden evaluar el riesgo de EHFN antes de proceder con pruebas invasivas como la amniocentesis o la interrupción del embarazo. La profilaxis anti-D se puede administrar antes de cualquier procedimiento que pueda provocar una hemorragia fetomaterna o se puede suspender con confianza en función del estado RhD fetal. Este enfoque garantiza que las mujeres RhD negativas eviten recibir profilaxis anti-D innecesaria aproximadamente el 40 % de las veces.
La prueba Devyser RHD ha demostrado una gran relevancia clínica a través de su uso rutinario durante los últimos diez años. Tiene una sensibilidad y especificidad diagnósticas de ≥99,86 %, según la correlación con la serología Rh del recién nacido. El kit de prueba CE-IVD está diseñado para ser fácil de usar y de rápida implementación. Solo se requiere una pequeña cantidad de ADN genómico, y el flujo de trabajo y el análisis de laboratorio optimizados son ideales para fines de detección. Devyser ha recibido la aprobación del IVDR para este producto de detección RhD fetal no invasivo, lo que marca la primera aprobación de producto de Clase D según las nuevas regulaciones europeas que entraron en vigor en mayo de 2022. Esta aprobación confirma que el producto Devyser RHD cumple con rigurosos estándares de seguridad, eficacia y calidad.
"Los programas de detección nacionales y regionales presentan importantes oportunidades para Devyser RHD, uno de nuestros productos de más rápido crecimiento, con un número cada vez mayor de usuarios en Europa", afirmó el director ejecutivo de Devyser, Fredrik Alpsten. "Estamos seguros de que esta aprobación mejorará aún más el potencial de crecimiento de este producto. La certificación garantiza que nuestro producto pionero continúa brindando resultados confiables de la más alta calidad a médicos y pacientes".
Enlaces relacionados:
Devyser
Últimas Hematología noticias
- Análisis sanguíneo de actividad plaquetaria en mediana edad podría identificar riesgo temprano de Alzheimer
- Medición de microvesículas podría detectar lesiones vasculares en pacientes con anemia falciforme
- Nueva guía de ADLM sobre pruebas de coagulación mejora atención a pacientes que toman anticoagulantes
- Pruebas viscoelásticas podrían mejorar tratamiento de hemorragia materna
- Modelo mide exposición a radiación en sangre para tratamientos precisos contra cáncer
- Las plaquetas podrían mejorar detección temprana y mínimamente invasiva del cáncer
- Dispositivo portátil desechable obtiene plasma rico en plaquetas sin equipos complejos
- Prueba de cartucho desechable ofrece resultados de hemograma rápidos y precisos
- Primera prueba de monitorización de heparina POC proporciona resultados rápidos

- Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
- Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
- Recuento de leucocitos predice gravedad de síntomas de COVID-19
- Tecnología de recuento de plaquetas ayudará a prevenir errores de diagnóstico
- Sistema de hemostasia POC podría prevenir muertes maternas
- Nueva prueba evalúa capacidad de los glóbulos rojos para transportar oxígeno midiendo su forma
- Pruebas de hemograma completo personalizadas ayudarían a diagnosticar enfermedades en etapa temprana
Canales
Química Clínica
ver canal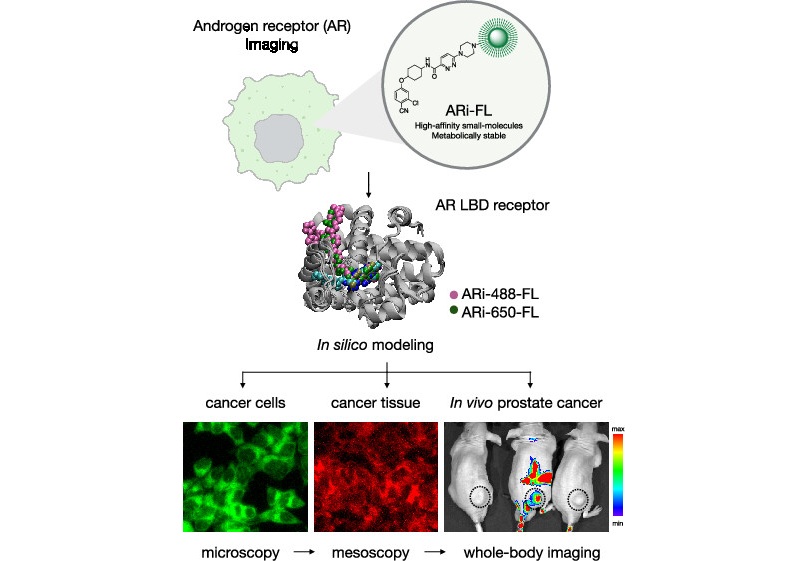
Sonda de imágenes químicas podría rastrear y tratar cáncer de próstata
El cáncer de próstata sigue siendo una de las principales causas de enfermedad y muerte en hombres, y muchos pacientes desarrollan resistencia a las terapias hormonales bloqueantes convencionales.... Más
Discrepancia entre dos pruebas comunes de función renal indica problemas de salud graves
La creatinina ha sido durante mucho tiempo el método estándar para medir la filtración renal, mientras que la cistatina C, una proteína producida por todas las células humanas, se ha recomendado como marcador... MásDiagnóstico Molecular
ver canal
Sencilla prueba de orina revolucionará diagnóstico y tratamiento del cáncer de vejiga
El cáncer de vejiga es uno de los cánceres urológicos más comunes y mortales, y se caracteriza por una alta tasa de recurrencia. El diagnóstico y el seguimiento aún... Más
Análisis snaguíneo para detección más temprana y sencilla de fibrosis hepática
El daño hepático persistente causado por el abuso de alcohol o infecciones virales puede desencadenar fibrosis hepática, una afección en la que el tejido sano se reemplaza gradualmente... MásInmunología
ver canal
Nueva prueba distingue falsos positivos inducidos por vacuna de infección activa por VIH
Desde que se identificó el VIH en 1983, más de 91 millones de personas han contraído el virus y más de 44 millones han fallecido por causas relacionadas. Hoy en día, casi 40 millones de personas en todo... Más
Prueba de firma genética predice respuesta a tratamientos clave para cáncer de mama
Los inhibidores de DK4/6, combinados con terapia hormonal, se han convertido en un tratamiento fundamental para el cáncer de mama avanzado HR+/HER2–, ya que ralentizan el crecimiento tumoral... MásMicrobiología
ver canal
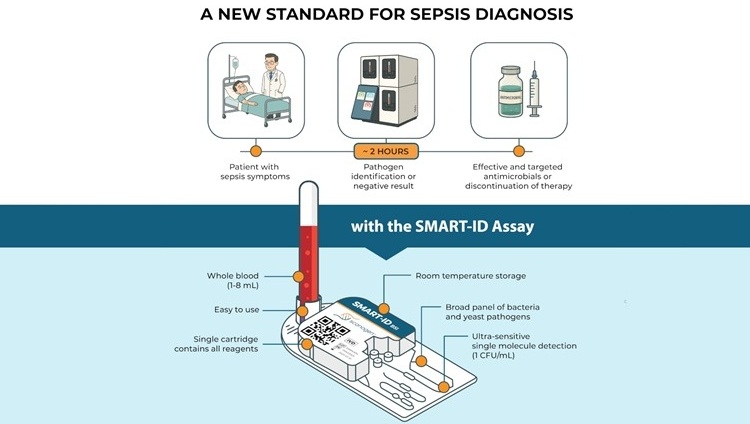
Prueba de diagnóstico rápido es estándar de oro para detección de sepsis
La sepsis causa la muerte de 11 millones de personas en todo el mundo cada año y genera enormes costos de atención médica. Solo en EUA y Europa, la sepsis representa 100.... MásPrueba rápida de tuberculosis POC proporciona resultados en 15 minutos
La tuberculosis sigue siendo una de las enfermedades infecciosas más mortales del mundo, y la reducción de nuevos casos depende de la identificación de las personas con infección... MásPatología
ver canal
Problemas de salud comunes pueden influir en nuevos análisis sanguíneos para enfermedad de Alzheimer
Las pruebas de sangre para la enfermedad de Alzheimer están transformando el diagnóstico al ofrecer una alternativa más sencilla a las punciones lumbares y las imágenes cerebrales.... Más
Fórmula de análisis sanguíneo identifica pacientes con enfermedad hepática crónica con mayor riesgo de cáncer
La enfermedad hepática crónica afecta a millones de personas en todo el mundo y puede progresar silenciosamente a carcinoma hepatocelular (CHC), uno de los cánceres más mortales... MásTecnología
ver canal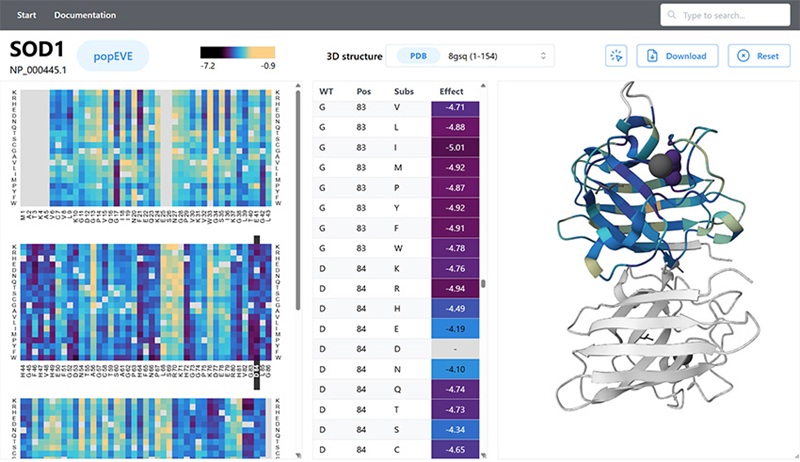
Modelo de inteligencia artificial podría acelerar diagnóstico de enfermedades raras
Identificar qué variantes genéticas causan enfermedades sigue siendo uno de los mayores desafíos de la medicina genómica. Cada persona porta decenas de miles de cambios en el... Más
Sensor de saliva con IA permite detección precoz del cáncer de cabeza y cuello
La detección precoz del cáncer de cabeza y cuello sigue siendo difícil porque la enfermedad produce pocos o ningún síntoma en sus primeras etapas, y las lesiones a menudo... MásIndustria
ver canal
Abbott adquiere Exact Sciences, empresa de detección de cáncer
Abbott (Abbott Park, IL, EUA) ha firmado un acuerdo definitivo para adquirir Exact Sciences (Madison, WI, EUA), lo que le permitirá entrar y liderar en segmentos de diagnóstico de cáncer... Más








 Analyzer.jpg)