Desarrollan un análisis diagnóstico para la deficiencia inmune combinada y severa sin clasificar
|
Por el equipo editorial de LabMedica en español Actualizado el 30 Jun 2020 |

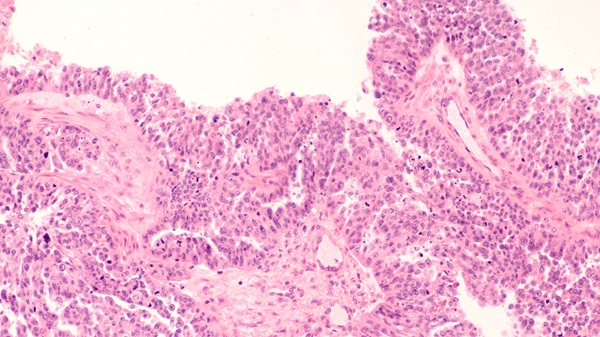
Imagen: El kit de separación celular MACS utiliza una combinación de microesferas superparamagnéticas de nanotamaño y un gradiente magnético muy alto en columnas MACS (Fotografía cortesía de Miltenyi Biotec).
La inmunodeficiencia combinada severa (SCID) es un grupo de trastornos genéticos hereditarios raros, y se caracteriza por una ausencia total de la función del sistema inmune, incluida la ausencia de linfocitos T, los glóbulos blancos que juegan un papel crucial en la defensa inmunológica del cuerpo.
Sin el tratamiento adecuado, este trastorno es fatal durante los primeros meses de vida en la mayoría de los casos. Los programas de detección de los recién nacidos han llevado a una mayor incidencia de pacientes diagnosticados con SCID. Aunque se han identificado muchos genes causantes de SCID, los médicos pueden enfrentar a un paciente sin haber identificado algún gen anormal.
Un equipo de científicos del Centro Hospitalario Universitario Sainte-Justine (Montreal, QC, Canadá) aisló un número muy pequeño de células madre de pacientes usando una cantidad limitada de sangre (3 mL a 5 mL). Se usa una prueba con un cultivo tridimensional (3D) que imita la función de un timo humano para probar esta pequeña cantidad de células, y se obtiene una respuesta en menos de cinco semanas. Si los resultados son normales, se recomienda el trasplante de timo, pero si son anormales, se prefiere un trasplante de médula ósea.
Para el cultivo en 3D, las células CD34+ se separaron de las células mononucleares por purificación con Ficoll a partir de sangre de cordón umbilical (SC) o sangre periférica (SP) fresca o congelada y descongelada, utilizando el kit MACS (Miltenyi Biotec, Bergisch Gladbach, Alemania). Las células CD34+ se mezclaron con células OP9-DLL4 cosechadas con tripsina (mezcla 1:23) para formar un comprimido celular de 2,5 µL, que se colocó en un inserto seco de cultivo de policarbonato de 25 mm. Este inserto se transfirió a una placa de 6 pozos que contenía 1,5 mL de medio. Los medios se cambiaron cada tres o cuatro días. Las células se cosecharon del inserto para realizar el análisis del clasificador de células activado por fluorescencia.
Los investigadores aplicaron el ensayo de diferenciación de células T 3D in vitro para verificar si podían diferenciar los defectos intrínsecos de diferenciación de las células madre hematopoyéticas extrínsecas (CMH) de los extrínsecos, mediante cantidades limitantes de sangre periférica de pacientes jóvenes con SCID. Como demostración de un defecto intrínseco de diferenciación, mostraron que las CMH SP-CD34+ de un paciente IL2RG/γc no podían diferenciarse en células CD34-CD7+CD1a+ doble negativo (DN), células CD4+CD8+ doble positivo (DP) o células CD3+, después de tres semanas de cultivo, aunque las células pro-T CD34+CD7+ estaban presentes en abundancia.
Por otro lado, las CMH SP-CD34+ de un paciente con SCID con deficiencia completa de RAG2 (mutación nula) avanzaron normalmente a la etapa CD34−CD7+CD1a+ DN, con escasa presencia de células CD4+CD8+ DP (0,72% versus 22,7% para el control) y sin células CD3+ después de cinco semanas de cultivo. Sin embargo, un paciente hipomorfo RAG1 adicional que se presenta con el síndrome de Omenn se podría diferenciar eficientemente hasta la etapa CD4+CD8+ DP (39,5% versus 12,36% para el control) después de cinco semanas de cultivo, pero no mostró evidencia de presencia de células CD3+.
Los autores concluyeron que presentaron una prueba de principio para un ensayo que utiliza células obtenidas de un volumen mínimo de SP para informar al médico sobre el nivel aproximado de deficiencia (células madre hematopoyéticas y células progenitoras versus defecto del timo) en el SCID no clasificado. El estudio fue publicado el 17 de junio de 2020 en la revista Blood Advances.
Enlace relacionado:
Centro Hospitalario Universitario Sainte-Justine
Sin el tratamiento adecuado, este trastorno es fatal durante los primeros meses de vida en la mayoría de los casos. Los programas de detección de los recién nacidos han llevado a una mayor incidencia de pacientes diagnosticados con SCID. Aunque se han identificado muchos genes causantes de SCID, los médicos pueden enfrentar a un paciente sin haber identificado algún gen anormal.
Un equipo de científicos del Centro Hospitalario Universitario Sainte-Justine (Montreal, QC, Canadá) aisló un número muy pequeño de células madre de pacientes usando una cantidad limitada de sangre (3 mL a 5 mL). Se usa una prueba con un cultivo tridimensional (3D) que imita la función de un timo humano para probar esta pequeña cantidad de células, y se obtiene una respuesta en menos de cinco semanas. Si los resultados son normales, se recomienda el trasplante de timo, pero si son anormales, se prefiere un trasplante de médula ósea.
Para el cultivo en 3D, las células CD34+ se separaron de las células mononucleares por purificación con Ficoll a partir de sangre de cordón umbilical (SC) o sangre periférica (SP) fresca o congelada y descongelada, utilizando el kit MACS (Miltenyi Biotec, Bergisch Gladbach, Alemania). Las células CD34+ se mezclaron con células OP9-DLL4 cosechadas con tripsina (mezcla 1:23) para formar un comprimido celular de 2,5 µL, que se colocó en un inserto seco de cultivo de policarbonato de 25 mm. Este inserto se transfirió a una placa de 6 pozos que contenía 1,5 mL de medio. Los medios se cambiaron cada tres o cuatro días. Las células se cosecharon del inserto para realizar el análisis del clasificador de células activado por fluorescencia.
Los investigadores aplicaron el ensayo de diferenciación de células T 3D in vitro para verificar si podían diferenciar los defectos intrínsecos de diferenciación de las células madre hematopoyéticas extrínsecas (CMH) de los extrínsecos, mediante cantidades limitantes de sangre periférica de pacientes jóvenes con SCID. Como demostración de un defecto intrínseco de diferenciación, mostraron que las CMH SP-CD34+ de un paciente IL2RG/γc no podían diferenciarse en células CD34-CD7+CD1a+ doble negativo (DN), células CD4+CD8+ doble positivo (DP) o células CD3+, después de tres semanas de cultivo, aunque las células pro-T CD34+CD7+ estaban presentes en abundancia.
Por otro lado, las CMH SP-CD34+ de un paciente con SCID con deficiencia completa de RAG2 (mutación nula) avanzaron normalmente a la etapa CD34−CD7+CD1a+ DN, con escasa presencia de células CD4+CD8+ DP (0,72% versus 22,7% para el control) y sin células CD3+ después de cinco semanas de cultivo. Sin embargo, un paciente hipomorfo RAG1 adicional que se presenta con el síndrome de Omenn se podría diferenciar eficientemente hasta la etapa CD4+CD8+ DP (39,5% versus 12,36% para el control) después de cinco semanas de cultivo, pero no mostró evidencia de presencia de células CD3+.
Los autores concluyeron que presentaron una prueba de principio para un ensayo que utiliza células obtenidas de un volumen mínimo de SP para informar al médico sobre el nivel aproximado de deficiencia (células madre hematopoyéticas y células progenitoras versus defecto del timo) en el SCID no clasificado. El estudio fue publicado el 17 de junio de 2020 en la revista Blood Advances.
Enlace relacionado:
Centro Hospitalario Universitario Sainte-Justine
Últimas Hematología noticias
- Análisis sanguíneo de actividad plaquetaria en mediana edad podría identificar riesgo temprano de Alzheimer
- Medición de microvesículas podría detectar lesiones vasculares en pacientes con anemia falciforme
- Nueva guía de ADLM sobre pruebas de coagulación mejora atención a pacientes que toman anticoagulantes
- Pruebas viscoelásticas podrían mejorar tratamiento de hemorragia materna
- Modelo mide exposición a radiación en sangre para tratamientos precisos contra cáncer
- Las plaquetas podrían mejorar detección temprana y mínimamente invasiva del cáncer
- Dispositivo portátil desechable obtiene plasma rico en plaquetas sin equipos complejos
- Prueba de cartucho desechable ofrece resultados de hemograma rápidos y precisos
- Primera prueba de monitorización de heparina POC proporciona resultados rápidos

- Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
- Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
- Recuento de leucocitos predice gravedad de síntomas de COVID-19
- Tecnología de recuento de plaquetas ayudará a prevenir errores de diagnóstico
- Sistema de hemostasia POC podría prevenir muertes maternas
- Nueva prueba evalúa capacidad de los glóbulos rojos para transportar oxígeno midiendo su forma
- Pruebas de hemograma completo personalizadas ayudarían a diagnosticar enfermedades en etapa temprana
Canales
Química Clínica
ver canal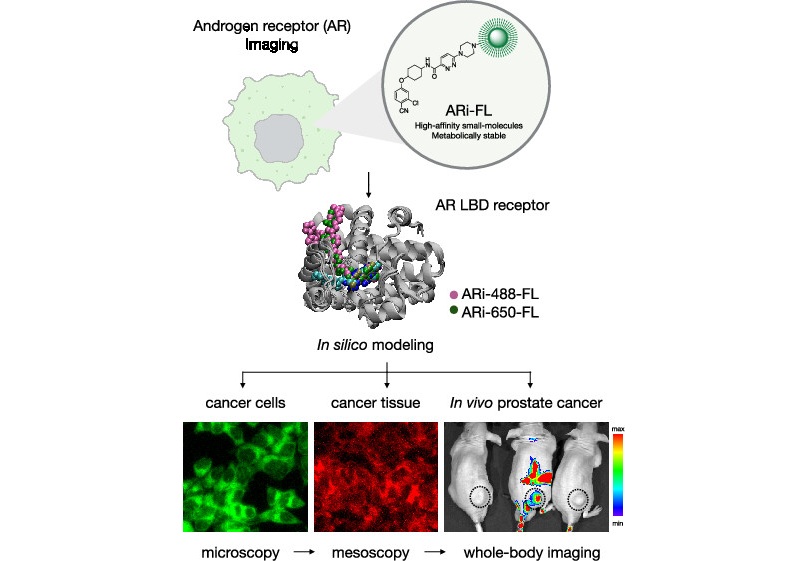
Sonda de imágenes químicas podría rastrear y tratar cáncer de próstata
El cáncer de próstata sigue siendo una de las principales causas de enfermedad y muerte en hombres, y muchos pacientes desarrollan resistencia a las terapias hormonales bloqueantes convencionales.... Más
Discrepancia entre dos pruebas comunes de función renal indica problemas de salud graves
La creatinina ha sido durante mucho tiempo el método estándar para medir la filtración renal, mientras que la cistatina C, una proteína producida por todas las células humanas, se ha recomendado como marcador... MásDiagnóstico Molecular
ver canal
Sencilla prueba de orina revolucionará diagnóstico y tratamiento del cáncer de vejiga
El cáncer de vejiga es uno de los cánceres urológicos más comunes y mortales, y se caracteriza por una alta tasa de recurrencia. El diagnóstico y el seguimiento aún... Más
Análisis snaguíneo para detección más temprana y sencilla de fibrosis hepática
El daño hepático persistente causado por el abuso de alcohol o infecciones virales puede desencadenar fibrosis hepática, una afección en la que el tejido sano se reemplaza gradualmente... MásHematología
ver canal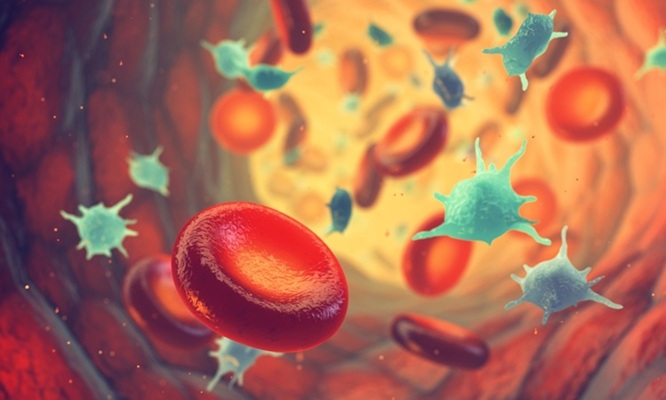
Análisis sanguíneo de actividad plaquetaria en mediana edad podría identificar riesgo temprano de Alzheimer
La detección temprana de la enfermedad de Alzheimer sigue siendo una de las mayores necesidades insatisfechas en neurología, sobre todo porque los cambios biológicos que subyacen al... Más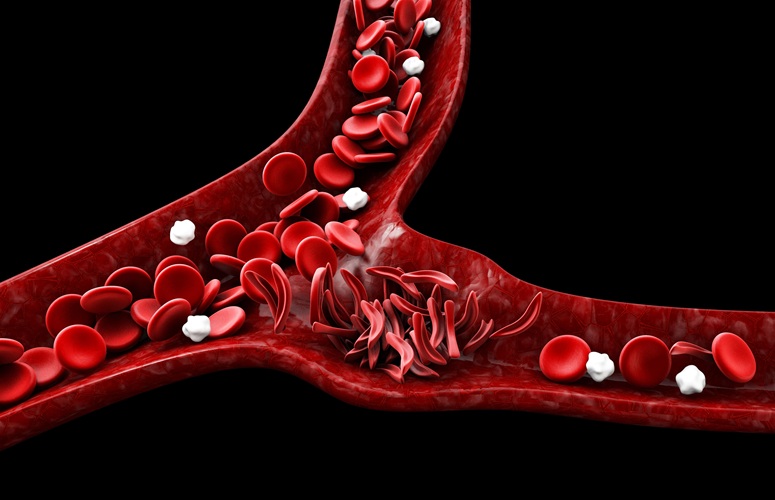
Medición de microvesículas podría detectar lesiones vasculares en pacientes con anemia falciforme
Evaluar la gravedad de la enfermedad de células falciformes (ECF) sigue siendo un reto, sobre todo al intentar predecir la hemólisis, el daño vascular y el riesgo de complicaciones... MásMicrobiología
ver canal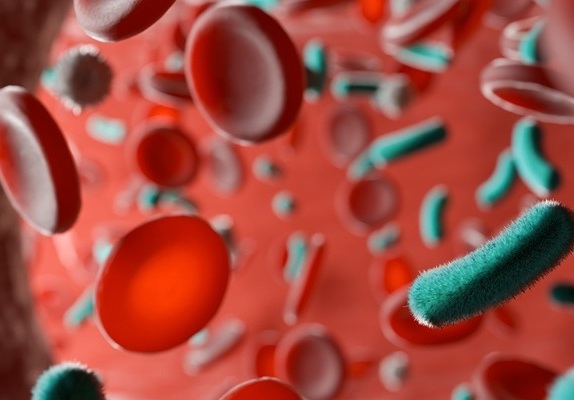
Prueba de diagnóstico rápido es estándar de oro para detección de sepsis
La sepsis causa la muerte de 11 millones de personas en todo el mundo cada año y genera enormes costos de atención médica. Solo en EUA y Europa, la sepsis representa 100.... MásPrueba rápida de tuberculosis POC proporciona resultados en 15 minutos
La tuberculosis sigue siendo una de las enfermedades infecciosas más mortales del mundo, y la reducción de nuevos casos depende de la identificación de las personas con infección... MásPatología
ver canal
Problemas de salud comunes pueden influir en nuevos análisis sanguíneos para enfermedad de Alzheimer
Las pruebas de sangre para la enfermedad de Alzheimer están transformando el diagnóstico al ofrecer una alternativa más sencilla a las punciones lumbares y las imágenes cerebrales.... Más
Fórmula de análisis sanguíneo identifica pacientes con enfermedad hepática crónica con mayor riesgo de cáncer
La enfermedad hepática crónica afecta a millones de personas en todo el mundo y puede progresar silenciosamente a carcinoma hepatocelular (CHC), uno de los cánceres más mortales... MásTecnología
ver canal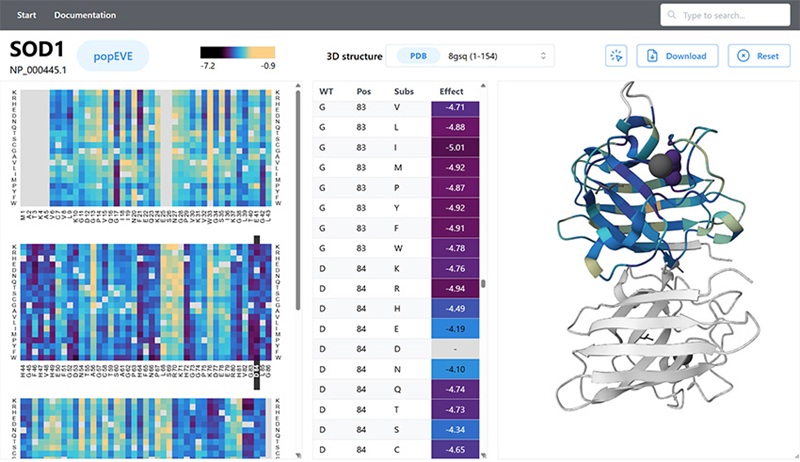
Modelo de inteligencia artificial podría acelerar diagnóstico de enfermedades raras
Identificar qué variantes genéticas causan enfermedades sigue siendo uno de los mayores desafíos de la medicina genómica. Cada persona porta decenas de miles de cambios en el... Más
Sensor de saliva con IA permite detección precoz del cáncer de cabeza y cuello
La detección precoz del cáncer de cabeza y cuello sigue siendo difícil porque la enfermedad produce pocos o ningún síntoma en sus primeras etapas, y las lesiones a menudo... MásIndustria
ver canal
Abbott adquiere Exact Sciences, empresa de detección de cáncer
Abbott (Abbott Park, IL, EUA) ha firmado un acuerdo definitivo para adquirir Exact Sciences (Madison, WI, EUA), lo que le permitirá entrar y liderar en segmentos de diagnóstico de cáncer... Más




 assay.jpg)