Células T reconocen variantes recientes del SARS-CoV-2
|
Por el equipo editorial de LabMedica en español Actualizado el 06 Jun 2021 |
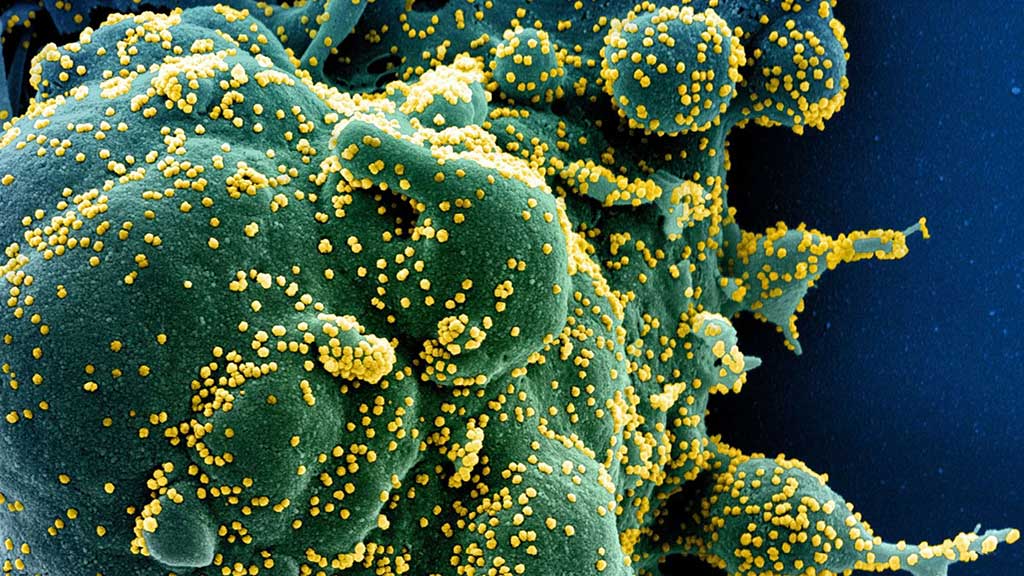
Imagen: los linfocitos de las células T inmunes pueden encontrar y destruir una célula (verde) infectada con SARS-CoV-2 (amarillo) y hacer copias (Fotografía cortesía del Instituto Nacional de Alergias y Enfermedades Infecciosas de los EUA)
Debido a la capacidad de corrección de la ARN polimerasa dependiente del ARN del coronavirus (CoV), la evolución de la población viral global del SARS-CoV-2 durante la pandemia actual ha sido relativamente limitada en comparación con otros virus ARN endémicos que no poseen esta capacidad.
A finales de 2020 se identificaron tres variantes distintas que poseían cada una cantidad significativamente mayor de polimorfismos de aminoácidos en asociación con las proteínas Spike en casos de COVID-19 en el Reino Unido (variante B.1.1.7), Sudáfrica (variante B.1.351) y Brasil (variante B.1.1.248). Todas estas variantes poseen la mutación N501Y en el dominio de unión al receptor (RBD) de la proteína Spike del SARS-CoV-2, un objetivo principal para la unión del anticuerpo neutralizante (NAb).
Un equipo colaborador de científicos dirigido por la Facultad de Medicina de la Universidad Johns Hopkins (Baltimore, MD, EUA), analizó muestras de células sanguíneas de 30 personas que habían contraído y se habían recuperado de la enfermedad del coronavirus 2019 (COVID-19) antes de la aparición de las variantes del virus. La mayoría (60%) de los individuos incluidos en el análisis eran hombres y las muestras se recolectaron una mediana de 42,5 días (rango intercuartílico, 37,5-48 días) desde el diagnóstico inicial. El equipo tenía como objetivo determinar si las células T CD8+ en la sangre aún podían reconocer las tres variantes principales del SARS-CoV-2. Se recolectaron y examinaron muestras de células mononucleares de sangre periférica (PBMC) de los pacientes en seis haplotipos de antígeno leucocitario humano (HLA) diferentes (HLAA*01:01, HLA-A*02:01, HLA-A03:01, HLA-A*11:01, HLA-A*24:02 y HLA-B*07:02).
Un método de coloración de tetrámero de péptido-MHC multiplexado permitió el cribado de 408 epítopos candidatos potenciales de SARS-CoV-2 para el reconocimiento de células T CD8+. Las células T también se evaluaron usando un panel fenotípico de 28 marcadores (Immunoscape Pte. Ltd, Singapur). Se encontraron un total de 52 respuestas de epítopos únicos y se dirigieron contra varias proteínas virales estructurales y no estructurales. Para los controles, se sondaron las células T CD8 + para determinar la reactividad de hasta 20 péptidos de control no relacionados con SARS-CoV-2 diferentes por HLA (epítopos derivados de Adenovirus, CMV, EBV, Influenza y MART-1).
El equipo informó que solo una mutación encontrada en la proteína Spike de B.1.35 se superpuso con un epítopo previamente identificado (1/52), sugiriendo que prácticamente todas las respuestas de células T anti-SARS-CoV-2 CD8+ deberían reconocer estas variantes recién descritas. Esta mutación es la mutación D80A en la proteína Spike y ocurre en el tercer residuo del epítopo RFDN VLPF. Este es un epítopo restringido a HLA*A24: 02 para el que se detectó una respuesta de linfocitos T CD8+ en 1/5 individuos HLA*A24:02+, y con una frecuencia baja (0,005 del total de linfocitos T CD8 +), lo que indica que no es un epítopo de alta prevalencia.
Los autores concluyeron que sus datos resaltaban el papel significativo potencial de una respuesta de células T multiepítopo en la limitación del escape viral y en parte medían la protección de la enfermedad causada por las variantes del SARS-CoV-2. Es importante que las vacunas utilizadas para campañas generalizadas generen fuertes respuestas de células T multivalentes además de anticuerpos neutralizantes (Nab) y otras respuestas humorales para optimizar la eficacia contra el SARS-CoV-2 actual y las cepas emergentes. Será importante continuar monitoreando la amplitud, magnitud y durabilidad de las respuestas de células T anti-SARS-CoV-2 en individuos recuperados y vacunados como parte de cualquier evaluación para determinar si se necesitan vacunas de refuerzo. El estudio fue publicado el 30 de marzo de 2021 en la revista Open Forum Infectious Diseases.
Enlace relacionado:
Facultad de Medicina de la Universidad Johns Hopkins
Immunoscape Pte. Ltd
A finales de 2020 se identificaron tres variantes distintas que poseían cada una cantidad significativamente mayor de polimorfismos de aminoácidos en asociación con las proteínas Spike en casos de COVID-19 en el Reino Unido (variante B.1.1.7), Sudáfrica (variante B.1.351) y Brasil (variante B.1.1.248). Todas estas variantes poseen la mutación N501Y en el dominio de unión al receptor (RBD) de la proteína Spike del SARS-CoV-2, un objetivo principal para la unión del anticuerpo neutralizante (NAb).
Un equipo colaborador de científicos dirigido por la Facultad de Medicina de la Universidad Johns Hopkins (Baltimore, MD, EUA), analizó muestras de células sanguíneas de 30 personas que habían contraído y se habían recuperado de la enfermedad del coronavirus 2019 (COVID-19) antes de la aparición de las variantes del virus. La mayoría (60%) de los individuos incluidos en el análisis eran hombres y las muestras se recolectaron una mediana de 42,5 días (rango intercuartílico, 37,5-48 días) desde el diagnóstico inicial. El equipo tenía como objetivo determinar si las células T CD8+ en la sangre aún podían reconocer las tres variantes principales del SARS-CoV-2. Se recolectaron y examinaron muestras de células mononucleares de sangre periférica (PBMC) de los pacientes en seis haplotipos de antígeno leucocitario humano (HLA) diferentes (HLAA*01:01, HLA-A*02:01, HLA-A03:01, HLA-A*11:01, HLA-A*24:02 y HLA-B*07:02).
Un método de coloración de tetrámero de péptido-MHC multiplexado permitió el cribado de 408 epítopos candidatos potenciales de SARS-CoV-2 para el reconocimiento de células T CD8+. Las células T también se evaluaron usando un panel fenotípico de 28 marcadores (Immunoscape Pte. Ltd, Singapur). Se encontraron un total de 52 respuestas de epítopos únicos y se dirigieron contra varias proteínas virales estructurales y no estructurales. Para los controles, se sondaron las células T CD8 + para determinar la reactividad de hasta 20 péptidos de control no relacionados con SARS-CoV-2 diferentes por HLA (epítopos derivados de Adenovirus, CMV, EBV, Influenza y MART-1).
El equipo informó que solo una mutación encontrada en la proteína Spike de B.1.35 se superpuso con un epítopo previamente identificado (1/52), sugiriendo que prácticamente todas las respuestas de células T anti-SARS-CoV-2 CD8+ deberían reconocer estas variantes recién descritas. Esta mutación es la mutación D80A en la proteína Spike y ocurre en el tercer residuo del epítopo RFDN VLPF. Este es un epítopo restringido a HLA*A24: 02 para el que se detectó una respuesta de linfocitos T CD8+ en 1/5 individuos HLA*A24:02+, y con una frecuencia baja (0,005 del total de linfocitos T CD8 +), lo que indica que no es un epítopo de alta prevalencia.
Los autores concluyeron que sus datos resaltaban el papel significativo potencial de una respuesta de células T multiepítopo en la limitación del escape viral y en parte medían la protección de la enfermedad causada por las variantes del SARS-CoV-2. Es importante que las vacunas utilizadas para campañas generalizadas generen fuertes respuestas de células T multivalentes además de anticuerpos neutralizantes (Nab) y otras respuestas humorales para optimizar la eficacia contra el SARS-CoV-2 actual y las cepas emergentes. Será importante continuar monitoreando la amplitud, magnitud y durabilidad de las respuestas de células T anti-SARS-CoV-2 en individuos recuperados y vacunados como parte de cualquier evaluación para determinar si se necesitan vacunas de refuerzo. El estudio fue publicado el 30 de marzo de 2021 en la revista Open Forum Infectious Diseases.
Enlace relacionado:
Facultad de Medicina de la Universidad Johns Hopkins
Immunoscape Pte. Ltd
Últimas Inmunología noticias
- Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
- Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
- Técnicas de vanguardia para investigar respuesta inmune en infecciones mortales por estreptococo A
- Novedosos inmunoensayos permiten diagnóstico temprano del síndrome antifosfolípido
- Nueva prueba podría predecir éxito de inmunoterapia para una gama más amplia de cánceres
- Pruebas simples de proteínas en sangre predicen resultados de CAR T para pacientes con linfoma
- Tecnología de chip clasificador de células podría allanar el camino para elaboración de perfiles inmunológicos POC
- Chip monitorea células cancerosas en muestras de sangre para evaluar eficacia del tratamiento
- Enfoques de inmunohematología automatizados pueden resolver incompatibilidad de trasplantes
- IA aprovecha genética tumoral para predecir respuesta del paciente a quimioterapia
- Primer dispositivo de monitoreo de leucocitos portátil y no invasivo del mundo elimina necesidad de extracción de sangre
- Prueba predictiva de células T detecta respuesta inmune a virus incluso antes de que se formen anticuerpos
- Analizador de inmunoensayo fluorescente portátil para pruebas POC rápidas transforma diagnósticos clínicos
- Detección multiparamétrica de autoanticuerpos ayuda a diagnosticar miositis
- Analizador CLIA todo en uno transforma el panorama del diagnóstico clínico
- Primera prueba de biomarcadores en sangre para predecir respuesta al tratamiento en pacientes con cáncer
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... Más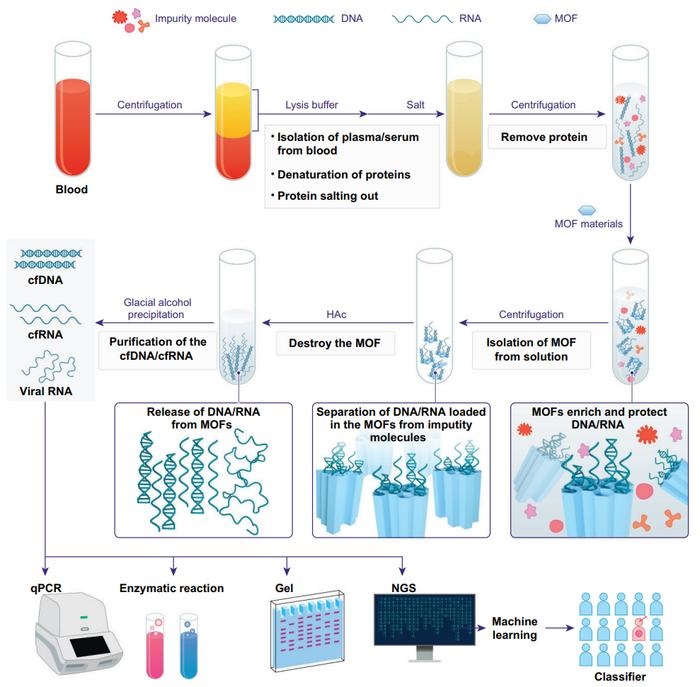
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal
Innovador dispositivo de extracción de sangre supera obstáculos comunes relacionados con la flebotomía
La incomodidad asociada con las extracciones de sangre tradicionales genera un problema importante: aproximadamente el 30 % de las pruebas de diagnóstico prescritas por los médicos nunca... Más
Dispositivo POC intraoperatorio distingue entre quistes ováricos benignos y malignos en 15 minutos
Los quistes ováricos representan un problema de salud importante para las mujeres en todo el mundo, y hasta el 10 % experimenta esta afección en algún momento de sus vidas.... Más
Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
La enfermedad de Parkinson y un grupo de trastornos neurodegenerativos relacionados conocidos como sinucleinopatías afectan a millones de personas en todo el mundo. Estas afecciones, incluida la... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)
.jpg)