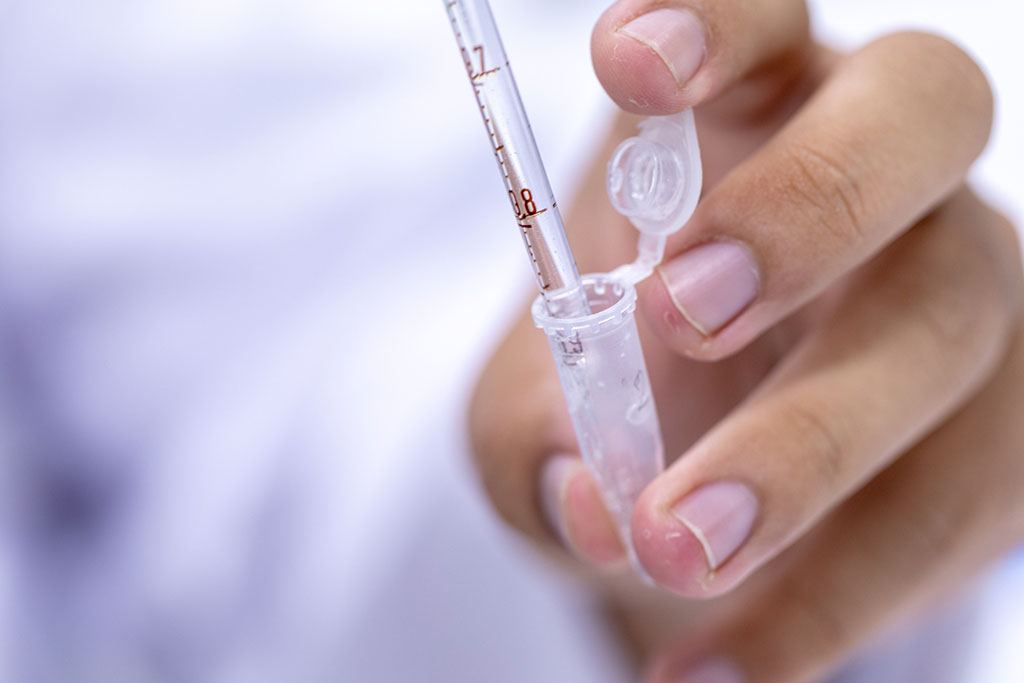
Secuenciación del genoma es más informativa que el análisis citogenético en los cánceres mieloides
|
Por el equipo editorial de LabMedica en español Actualizado el 24 Mar 2021 |

Imagen: El instrumento de secuenciación NovaSeq 6000 (Fotografía cortesía de Illumina)
El perfil genético es un componente de rutina del trabajo de diagnóstico para un número creciente de cánceres y se utiliza para predecir los resultados clínicos y las respuestas a las terapias dirigidas. El análisis genómico es esencial para la estratificación del riesgo en pacientes con leucemia mieloide aguda (LMA) o síndromes mielodisplásicos (SMD).
La secuenciación del genoma completo es un método imparcial para detectar todo tipo de mutaciones y podría ser usado potencialmente para reemplazar los algoritmos de prueba actuales. Dicha secuenciación también se puede realizar en una cantidad limitada de ADN y puede identificar cambios genómicos que pueden ser crípticos en otros tipos de análisis. Estas características de la secuenciación del genoma completo sugieren que podría mejorar el perfil genómico en pacientes con cáncer.
Un gran equipo de científicos dirigido por los de la Universidad de Washington en St. Louis (St. Louis, MO, EUA), utilizó un enfoque simplificado de secuenciación del genoma completo (ChromoSeq) para obtener perfiles genómicos de 263 pacientes con cánceres mieloides, incluidos 235 pacientes a quienes les habían realizado con éxito un análisis citogenético. El equipo analizó el desempeño de la secuenciación del genoma completo comparando sus resultados con los hallazgos del análisis citogenético y la secuenciación dirigida. La secuenciación se realizó en instrumentos de secuenciación, NovaSeq 6000 (Illumina, San Diego, CA, EUA). Los científicos utilizaron hibridación fluorescente in situ (FISH), reacción en cadena de la polimerasa (PCR), análisis de microarrays cromosómicos y datos de secuenciación de ARN para confirmar los hallazgos sobre la secuenciación del genoma completo que no habían sido detectados por análisis citogenético.
Los investigadores informaron que la secuenciación del genoma completo detectó las 40 translocaciones recurrentes y las 91 alteraciones en el número de copias que se habían identificado mediante análisis citogenético. Además, identificaron nuevos eventos genómicos clínicamente notificables en 40 de 235 pacientes (17,0%). La secuenciación prospectiva de muestras obtenidas de 117 pacientes consecutivos se realizó en una mediana de cinco días y proporcionó nueva información genética en 29 pacientes (24,8%), lo que cambió la categoría de riesgo para 19 pacientes (16,2%). Los grupos de riesgo de LMA estándar, según se definen mediante la secuenciación de los resultados en lugar del análisis citogenético, se correlacionan con los resultados clínicos. La secuenciación del genoma completo también se utilizó para estratificar a los pacientes que tenían resultados no concluyentes mediante el análisis citogenético en grupos de riesgo en los que los resultados clínicos eran significativamente diferentes.
Los autores concluyeron que la secuenciación del genoma completo proporcionó un perfil genómico rápido y exacto en pacientes con LMA o SMD. Dicha secuenciación también proporcionó un mayor desempeño diagnóstico que el análisis citogenético convencional y una estratificación de riesgo más eficiente sobre la base de categorías de riesgo estándar. Los autores estimaron el costo de la WGS en su estudio, en alrededor de 1.900 dólares, lo que lo coloca en el rango de otras plataformas de análisis. En los laboratorios de alto rendimiento, el costo podría ser de unos 1.300 dólares. A medida que disminuya el costo de la secuenciación, es probable que la WGS alcance la paridad de precios con las plataformas de prueba convencionales. El estudio fue publicado el 11 de marzo de 2021 en la revista The New England Journal of Medicine.
Enlace relacionado:
Universidad de Washington en St. Louis
Illumina
La secuenciación del genoma completo es un método imparcial para detectar todo tipo de mutaciones y podría ser usado potencialmente para reemplazar los algoritmos de prueba actuales. Dicha secuenciación también se puede realizar en una cantidad limitada de ADN y puede identificar cambios genómicos que pueden ser crípticos en otros tipos de análisis. Estas características de la secuenciación del genoma completo sugieren que podría mejorar el perfil genómico en pacientes con cáncer.
Un gran equipo de científicos dirigido por los de la Universidad de Washington en St. Louis (St. Louis, MO, EUA), utilizó un enfoque simplificado de secuenciación del genoma completo (ChromoSeq) para obtener perfiles genómicos de 263 pacientes con cánceres mieloides, incluidos 235 pacientes a quienes les habían realizado con éxito un análisis citogenético. El equipo analizó el desempeño de la secuenciación del genoma completo comparando sus resultados con los hallazgos del análisis citogenético y la secuenciación dirigida. La secuenciación se realizó en instrumentos de secuenciación, NovaSeq 6000 (Illumina, San Diego, CA, EUA). Los científicos utilizaron hibridación fluorescente in situ (FISH), reacción en cadena de la polimerasa (PCR), análisis de microarrays cromosómicos y datos de secuenciación de ARN para confirmar los hallazgos sobre la secuenciación del genoma completo que no habían sido detectados por análisis citogenético.
Los investigadores informaron que la secuenciación del genoma completo detectó las 40 translocaciones recurrentes y las 91 alteraciones en el número de copias que se habían identificado mediante análisis citogenético. Además, identificaron nuevos eventos genómicos clínicamente notificables en 40 de 235 pacientes (17,0%). La secuenciación prospectiva de muestras obtenidas de 117 pacientes consecutivos se realizó en una mediana de cinco días y proporcionó nueva información genética en 29 pacientes (24,8%), lo que cambió la categoría de riesgo para 19 pacientes (16,2%). Los grupos de riesgo de LMA estándar, según se definen mediante la secuenciación de los resultados en lugar del análisis citogenético, se correlacionan con los resultados clínicos. La secuenciación del genoma completo también se utilizó para estratificar a los pacientes que tenían resultados no concluyentes mediante el análisis citogenético en grupos de riesgo en los que los resultados clínicos eran significativamente diferentes.
Los autores concluyeron que la secuenciación del genoma completo proporcionó un perfil genómico rápido y exacto en pacientes con LMA o SMD. Dicha secuenciación también proporcionó un mayor desempeño diagnóstico que el análisis citogenético convencional y una estratificación de riesgo más eficiente sobre la base de categorías de riesgo estándar. Los autores estimaron el costo de la WGS en su estudio, en alrededor de 1.900 dólares, lo que lo coloca en el rango de otras plataformas de análisis. En los laboratorios de alto rendimiento, el costo podría ser de unos 1.300 dólares. A medida que disminuya el costo de la secuenciación, es probable que la WGS alcance la paridad de precios con las plataformas de prueba convencionales. El estudio fue publicado el 11 de marzo de 2021 en la revista The New England Journal of Medicine.
Enlace relacionado:
Universidad de Washington en St. Louis
Illumina
Últimas Hematología noticias
- Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
- Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
- Rastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
- Analizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
- Plataforma de hematología automatizada ofrece desempeño analítico de alto rendimiento
- Nueva herramienta analiza plaquetas sanguíneas de forma más rápida, sencilla y precisa
- Primer analizador de hematología de resultados rápidos informa medidas de infección y gravedad en el POC
- Prueba de diagnóstico de riesgo de hemorragia reduce complicaciones prevenibles en hospitales
- Verdadero analizador de hematología POC con muestreo capilar directo mejora facilidad de uso y rendimiento de pruebas
- Analizador de hemograma completo para el punto de atención con muestreo capilar directo mejora facilidad de uso y rendimiento de pruebas
- Examen de sangre podría predecir resultados en el departamento de emergencias y admisiones hospitalarias
- Nueva tecnología diagnostica inmunotrombosis mediante análisis de gases de aliento
- Sistema de hematología avanzado permite a laboratorios procesar hasta 119 resultados de hemogramas por hora
- Método único basado en IA automatiza análisis clínico de datos sanguíneos
- Herramienta portátil puede diagnosticar y monitorear enfermedad de células falciformes
- Analizadores de hematología de próxima generación eliminan obstáculos del flujo de trabajo y alcanzan un rendimiento rápido
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más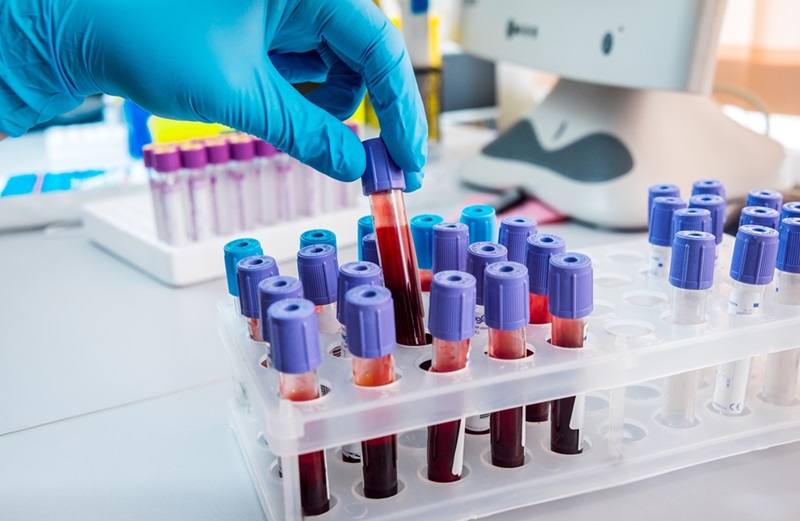
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal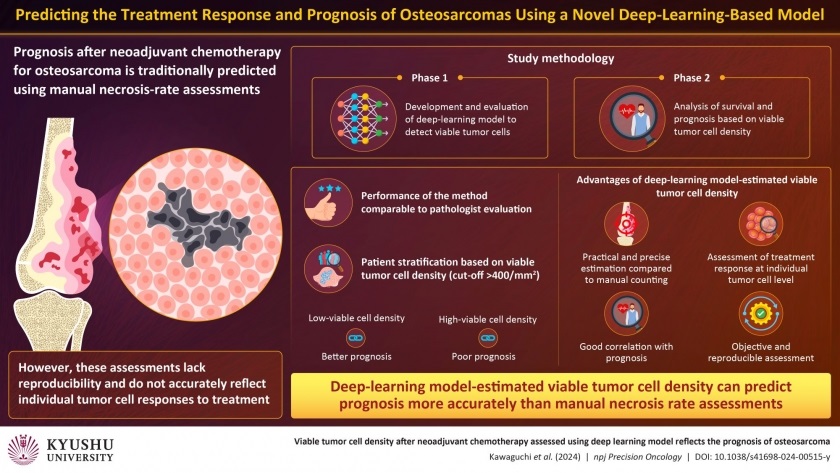
Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico... Más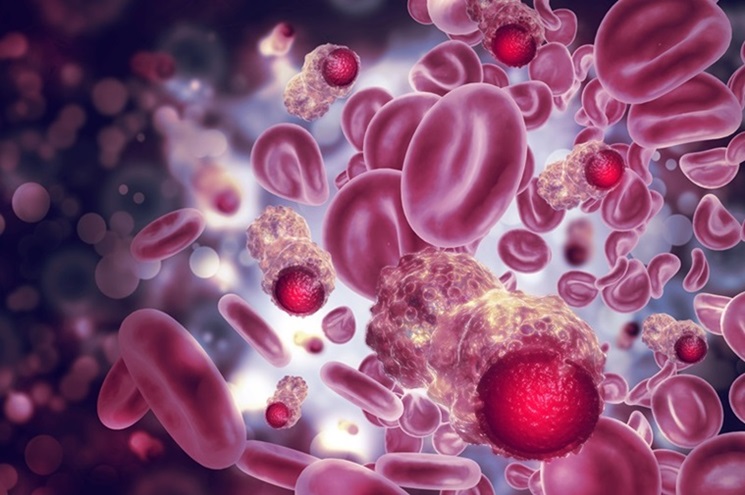
Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
La comunidad médica mundial reconoce cada vez más que la biopsia líquida es un enfoque transformador para mejorar la atención al paciente con cáncer. Este innovador método de diagnóstico implica detectar... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)

.jpg)