Evalúan biomarcadores para determinar la severidad de la fibrosis quística
|
Por el equipo editorial de LabMedica en español Actualizado el 22 Jun 2020 |
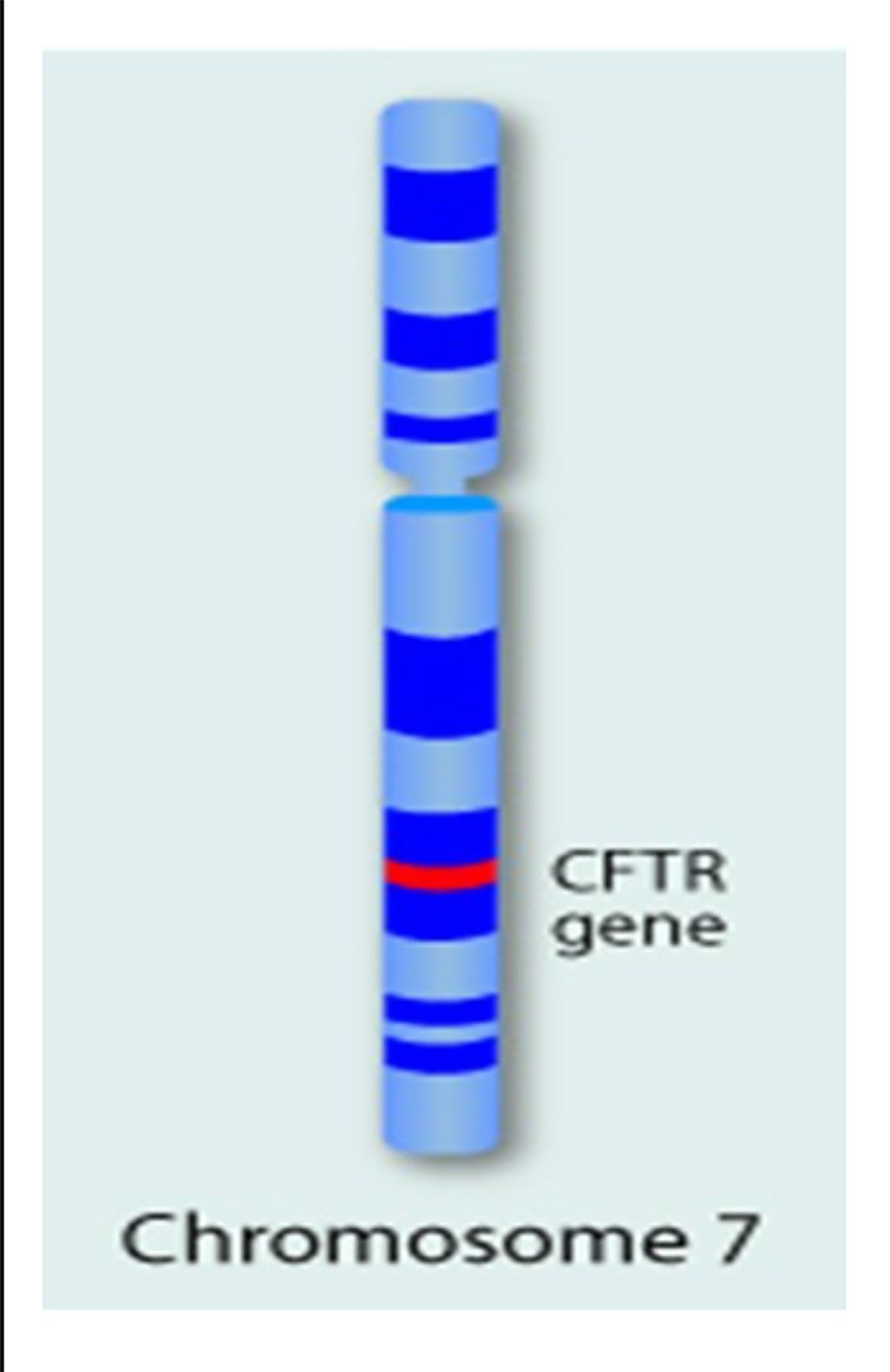
Imagen: El gen único, el gen regulador de la transmembrana de la fibrosis quística (CFTR) se encuentra en el brazo largo del cromosoma 7, y sus mutaciones causan la FQ (Fotografía cortesía de Daryl Isaac).
La fibrosis quística (FQ) es uno de los trastornos monogénicos más comunes, que acortan la vida, entre las poblaciones de ascendencia europea, que actualmente afecta a más de 85.000 pacientes en todo el mundo. El diagnóstico de FQ se basa en criterios clínicos y de laboratorio consensuados.
Para confirmar un diagnóstico de FQ, es necesario obtener evidencia de disfunción del regulador de conductancia transmembrana de la FQ (CFTR) mediante la identificación de dos mutaciones del gen CFTR in trans, previamente asignadas como causantes de la FQ, y realizar pruebas que muestren una alta concentración de cloruro en el sudor, mediciones distintivas de la diferencia de potencial nasal transepitelial (NPD) y/o evaluación de la (dis)función de CFTR en epitelios colónicos nativos ex vivo.
Un equipo internacional de científicos de laboratorio médico dirigido por la Universidad de Debrecen (Debrecen, Hungría) revisó los métodos utilizados para diagnosticar la FQ. El monitoreo de la inflamación pulmonar mediante biomarcadores de sangre periférica es la estrategia más común con posibilidad de estandarización analítica y, en general, es reproducible. El equipo resumió la utilidad de los biomarcadores basados en el lavado de sangre, esputo y lavado broncoalveolar (BAL), hasta ahora estudiados para evaluar las condiciones inflamatorias en los pulmones y seguir la eficacia del tratamiento en la FQ.
Se analizaron las concentraciones séricas o plasmáticas de proteína C reactiva (PCR) como indicadores de inflamación sistémica en la FQ y se descubrió que aumentan en la enfermedad. Se encontraron niveles de PCR plasmáticos basales más altos (≥5,2 mg/L) en pacientes adultos con FQ que tenían una enfermedad más grave y tenían un mayor riesgo de exacerbación pulmonar (PEx). Del mismo modo, la PCR sérica se encontraba entre esos biomarcadores individuales, que podrían diferenciar efectivamente a los niños con FQ de acuerdo con la gravedad de la enfermedad pulmonar.
La enfermedad de las vías respiratorias se caracteriza por infección crónica e inflamación recurrente con predominio de neutrófilos en asociación con una mayor producción de varias citoquinas proinflamatorias, como IL-6, IL-8 y factor de necrosis tumoral α (TNF-α). La IL-6 en suero separó a los pacientes con FQ de los individuos normales y mostró una reducción significativa durante la terapia con antibióticos. Del mismo modo, la IL-8 en plasma monitorizó la eficacia antibiótica a los 21 días e indicó el inicio de una nueva exacerbación temprana. Las concentraciones plasmáticas más altas de IL-6 e IL-8 en el momento de la exacerbación se asociaron con un mayor riesgo de no responder a los antibióticos.
Los neutrófilos activados producen varias proteínas en condiciones inflamatorias, como NE, mieloperoxidasa (MPO), calprotectina, YKL-40, etc., que circulan en gran cantidad en las muestras de sangre de pacientes con FQ. La NE es una serina proteasa “destructiva” que afecta a las proteínas de la matriz extracelular que forma complejos con antiproteasas, que conducen al complejo neutrófilo elastasa-antiproteasa (NE-APC). La NE-APC en el plasma se elevó en personas con FQ versus los controles no FQ. El efecto de la terapia con antibióticos repetidos fue significativo en los niveles séricos de MPO y, por lo tanto, se utilizó para evaluar la eficacia terapéutica en las PEx. El descubrimiento reciente de una nueva proteína (por ejemplo, proteína del epidídimo humano) y biomarcadores basados en ARN, como los microARN, pueden ofrecer una mayor eficacia que, en conjunto, puede ser valiosa para evaluar el pronóstico de la enfermedad y corroborar la eficacia del fármaco contra la FQ.
Los autores concluyeron que el campo del desarrollo de biomarcadores está en rápida evolución, por lo que se espera que se utilicen varias tecnologías ómicas junto con algoritmos avanzados de bioinformática para comprender la complejidad multisistémica de la FQ en varias etapas de su desarrollo. El estudio fue publicado en línea el 16 de mayo de 2020 en la revista Clinica Chimica Acta.
Enlace relacionado:
Universidad de Debrecen
Para confirmar un diagnóstico de FQ, es necesario obtener evidencia de disfunción del regulador de conductancia transmembrana de la FQ (CFTR) mediante la identificación de dos mutaciones del gen CFTR in trans, previamente asignadas como causantes de la FQ, y realizar pruebas que muestren una alta concentración de cloruro en el sudor, mediciones distintivas de la diferencia de potencial nasal transepitelial (NPD) y/o evaluación de la (dis)función de CFTR en epitelios colónicos nativos ex vivo.
Un equipo internacional de científicos de laboratorio médico dirigido por la Universidad de Debrecen (Debrecen, Hungría) revisó los métodos utilizados para diagnosticar la FQ. El monitoreo de la inflamación pulmonar mediante biomarcadores de sangre periférica es la estrategia más común con posibilidad de estandarización analítica y, en general, es reproducible. El equipo resumió la utilidad de los biomarcadores basados en el lavado de sangre, esputo y lavado broncoalveolar (BAL), hasta ahora estudiados para evaluar las condiciones inflamatorias en los pulmones y seguir la eficacia del tratamiento en la FQ.
Se analizaron las concentraciones séricas o plasmáticas de proteína C reactiva (PCR) como indicadores de inflamación sistémica en la FQ y se descubrió que aumentan en la enfermedad. Se encontraron niveles de PCR plasmáticos basales más altos (≥5,2 mg/L) en pacientes adultos con FQ que tenían una enfermedad más grave y tenían un mayor riesgo de exacerbación pulmonar (PEx). Del mismo modo, la PCR sérica se encontraba entre esos biomarcadores individuales, que podrían diferenciar efectivamente a los niños con FQ de acuerdo con la gravedad de la enfermedad pulmonar.
La enfermedad de las vías respiratorias se caracteriza por infección crónica e inflamación recurrente con predominio de neutrófilos en asociación con una mayor producción de varias citoquinas proinflamatorias, como IL-6, IL-8 y factor de necrosis tumoral α (TNF-α). La IL-6 en suero separó a los pacientes con FQ de los individuos normales y mostró una reducción significativa durante la terapia con antibióticos. Del mismo modo, la IL-8 en plasma monitorizó la eficacia antibiótica a los 21 días e indicó el inicio de una nueva exacerbación temprana. Las concentraciones plasmáticas más altas de IL-6 e IL-8 en el momento de la exacerbación se asociaron con un mayor riesgo de no responder a los antibióticos.
Los neutrófilos activados producen varias proteínas en condiciones inflamatorias, como NE, mieloperoxidasa (MPO), calprotectina, YKL-40, etc., que circulan en gran cantidad en las muestras de sangre de pacientes con FQ. La NE es una serina proteasa “destructiva” que afecta a las proteínas de la matriz extracelular que forma complejos con antiproteasas, que conducen al complejo neutrófilo elastasa-antiproteasa (NE-APC). La NE-APC en el plasma se elevó en personas con FQ versus los controles no FQ. El efecto de la terapia con antibióticos repetidos fue significativo en los niveles séricos de MPO y, por lo tanto, se utilizó para evaluar la eficacia terapéutica en las PEx. El descubrimiento reciente de una nueva proteína (por ejemplo, proteína del epidídimo humano) y biomarcadores basados en ARN, como los microARN, pueden ofrecer una mayor eficacia que, en conjunto, puede ser valiosa para evaluar el pronóstico de la enfermedad y corroborar la eficacia del fármaco contra la FQ.
Los autores concluyeron que el campo del desarrollo de biomarcadores está en rápida evolución, por lo que se espera que se utilicen varias tecnologías ómicas junto con algoritmos avanzados de bioinformática para comprender la complejidad multisistémica de la FQ en varias etapas de su desarrollo. El estudio fue publicado en línea el 16 de mayo de 2020 en la revista Clinica Chimica Acta.
Enlace relacionado:
Universidad de Debrecen
Últimas Inmunología noticias
- Análisis de sangre para diagnóstico de rechazo celular después de trasplante de órganos podría reemplazar las biopsias quirúrgicas
- Herramienta de IA ajusta con precisión los medicamentos contra el cáncer con los pacientes utilizando información de cada célula tumoral
- Pruebas genéticas combinadas con la detección de fármacos personalizadas en muestras de tumores podrían revolucionar el tratamiento del cáncer
- Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
- Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
- Técnicas de vanguardia para investigar respuesta inmune en infecciones mortales por estreptococo A
- Novedosos inmunoensayos permiten diagnóstico temprano del síndrome antifosfolípido
- Nueva prueba podría predecir éxito de inmunoterapia para una gama más amplia de cánceres
- Pruebas simples de proteínas en sangre predicen resultados de CAR T para pacientes con linfoma
- Tecnología de chip clasificador de células podría allanar el camino para elaboración de perfiles inmunológicos POC
- Chip monitorea células cancerosas en muestras de sangre para evaluar eficacia del tratamiento
- Enfoques de inmunohematología automatizados pueden resolver incompatibilidad de trasplantes
- IA aprovecha genética tumoral para predecir respuesta del paciente a quimioterapia
- Primer dispositivo de monitoreo de leucocitos portátil y no invasivo del mundo elimina necesidad de extracción de sangre
- Prueba predictiva de células T detecta respuesta inmune a virus incluso antes de que se formen anticuerpos
- Analizador de inmunoensayo fluorescente portátil para pruebas POC rápidas transforma diagnósticos clínicos
Canales
Diagnóstico Molecular
ver canal
Prueba de sangre predice con precisión el riesgo de cáncer de pulmón y reduce la necesidad de escaneos de TC
El cáncer de pulmón es extremadamente difícil de detectar tempranamente debido a las limitaciones de las tecnologías de detección actuales, que son costosas, a veces... Más
Firma única de autoanticuerpos ayuda a diagnosticar la esclerosis múltiple años antes de la aparición de síntomas
Se cree que las enfermedades autoinmunes como la esclerosis múltiple (EM) ocurren en parte debido a respuestas inmunes inusuales a infecciones comunes. Los primeros síntomas de la EM, incluidos... Más
Prueba de sangre podría detectar cánceres asociados al VPH 10 años antes del diagnóstico clínico
Se sabe que el virus del papiloma humano (VPH) causa varios cánceres, incluidos los de genitales, ano, boca, garganta y cuello uterino. El cáncer orofaríngeo asociado al VPH (VPH+COF)... Más
Un diagnóstico de bajo costo en el punto de atención ampliará el acceso a pruebas de enfermedades de transmisión sexual
La gonorrea es la segunda infección bacteriana de transmisión sexual (ITS) más comúnmente reportada, con alrededor de 82 millones de casos en todo el mundo en 2020. La infección puede tener graves consecuencias... MásHematología
ver canal
Primera prueba NAT 4 en 1 para el cribado de arbovirus podría reducir el riesgo de infecciones transmitidas por transfusiones
Los arbovirus representan una amenaza emergente para la salud mundial, exacerbada por el cambio climático y el aumento de la conectividad mundial que está facilitando su propagación a nuevas regiones.... Más
Instrumento de próxima generación detecta trastornos de la hemoglobina en recién nacidos
Las hemoglobinopatías, las enfermedades hereditarias más extendidas a nivel mundial, afectan a alrededor del 7 % de la población como portadores, y el 2,7 % de los recién nacidos nacen con estas enfermedades.... Más
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásInmunología
ver canal
Análisis de sangre para diagnóstico de rechazo celular después de trasplante de órganos podría reemplazar las biopsias quirúrgicas
Los órganos trasplantados enfrentan constantemente el riesgo de ser rechazados por el sistema inmunológico del receptor, que los diferencia de los órganos no propios mediante... Más
Herramienta de IA ajusta con precisión los medicamentos contra el cáncer con los pacientes utilizando información de cada célula tumoral
Las estrategias actuales para emparejar a los pacientes con cáncer con tratamientos específicos a menudo dependen de la secuenciación masiva de ADN y ARN tumoral, que proporciona un perfil promedio de... Más
Pruebas genéticas combinadas con la detección de fármacos personalizadas en muestras de tumores podrían revolucionar el tratamiento del cáncer
El tratamiento del cáncer generalmente se adhiere a un estándar de atención: regímenes establecidos y validados estadísticamente que son efectivos para la mayoría de los pacientes. Sin embargo, la variabilidad... Más
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... MásMicrobiología
ver canal
Nuevos ensayos de hepatitis con marcado CE permite la detección temprana de infecciones
Según la Organización Mundial de la Salud (OMS), se estima que 354 millones de personas en todo el mundo padecen hepatitis B o C crónica. Estos virus son las principales causas de... Más
Prueba de PCR múltiplex identifica el 95 % de los patógenos que causan la sepsis en una hora
La sepsis contribuye a una de cada tres muertes hospitalarias en los Estados Unidos y, a nivel mundial, el shock séptico conlleva una tasa de mortalidad del 30 al 40 %. El diagnóstico temprano de la sepsis... Más
Prueba de bacterias bucales podría predecir la progresión del cáncer de colon
El cáncer de colon, una enfermedad relativamente común pero difícil de diagnosticar, requiere confirmación mediante una colonoscopia o cirugía. Recientemente, ha habido... Más.jpg)
Firma metabólica unica podría permitir el diagnóstico de sepsis dentro de una hora de la extracción de sangre
La sepsis es una afección potencialmente mortal provocada por una respuesta extrema del cuerpo a una infección. Requiere intervención médica inmediata para evitar una posible muerte o daños duraderos.... MásPatología
ver canalSistema de imágenes digitales impulsado por IA podría revolucionar el diagnóstico del cáncer
El proceso de biopsia es importante para confirmar la presencia de cáncer. En la técnica de histopatología convencional, el tejido se extirpa, se corta, se tiñe, se monta en... Más
Nuevo panel de mycobacterium tuberculosis respalda la vigilancia en tiempo real y combate la resistencia a los antimicrobianos
La tuberculosis (TB), la principal causa de muerte por enfermedad infecciosa a nivel mundial, es una infección bacteriana contagiosa que se propaga principalmente a través de la tos de pacientes con tuberculosis... Más
Análisis de tejido espacial identifica patrones asociados con la recaída del cáncer de ovario
El carcinoma de ovario seroso de alto grado es el tipo más letal de cáncer de ovario y plantea importantes desafíos de detección. Por lo general, los pacientes responden inicialmente... Más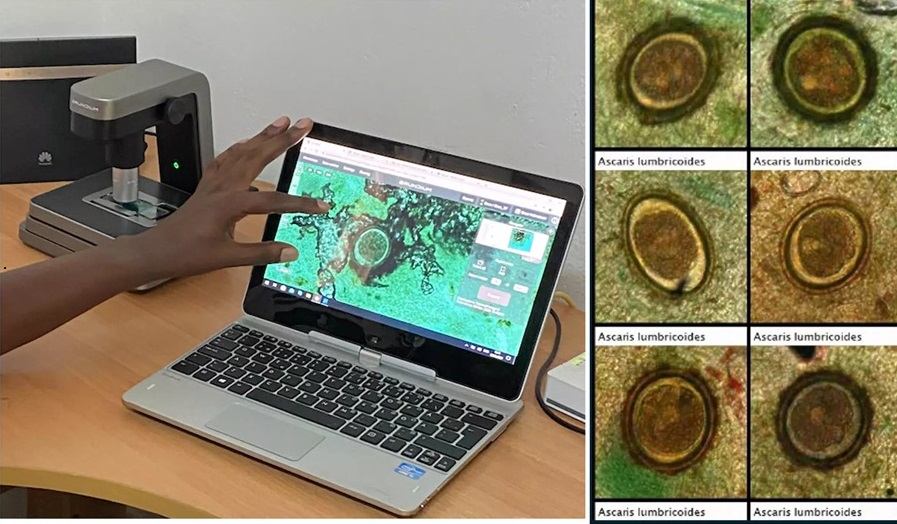
IA basada en imágenes se muestra prometedora para detección de parásitos en muestras de heces digitalizadas
Las infecciones por helmintos transmitidos por el suelo (STH), comúnmente conocidas como gusanos parásitos intestinales, se encuentran entre las enfermedades tropicales desatendidas más... MásTecnología
ver canal
Nuevo sistema de diagnóstico de laboratorio en un chip iguala la precisión de las pruebas de PCR
Si bien las pruebas de PCR son el estándar de oro en cuanto a precisión para las pruebas de virología, tienen limitaciones como la complejidad, la necesidad de operadores de laboratorio capacitados y tiempos... Más
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más