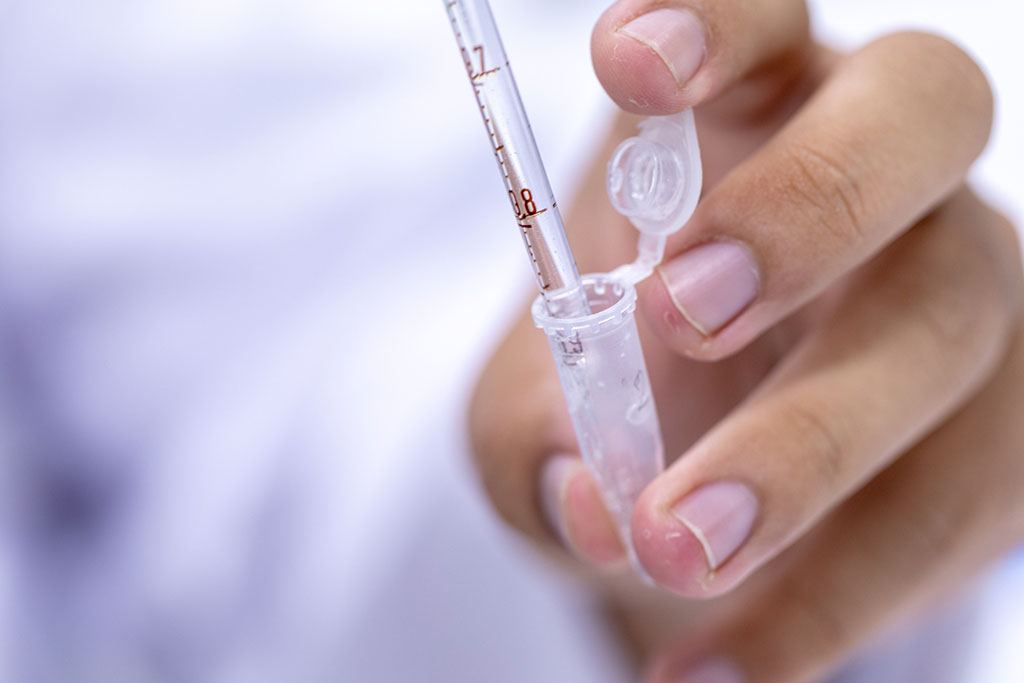
Proceso diagnóstico detecta el Alzheimer muchos años antes de que aparezcan los síntomas
|
Por el equipo editorial de LabMedica en español Actualizado el 28 May 2019 |
Imagen: El kit V-PLEX Aβ Peptide Panel 1 (6E10) (Fotografía cortesía de Meso Scale Discovery).
La patología de la enfermedad de Alzheimer (EA) se acompaña del plegamiento incorrecto del amiloide-β (Aβ) y de la conversión de tau monomérico a especies patógenas enriquecidas en hoja β. Se sugiere que este proceso precede de 10 a 15 años el inicio clínico de la enfermedad.
Un nuevo proceso de diagnóstico de dos pasos podría detectar la enfermedad de Alzheimer casi una década antes de que aparezcan los síntomas clínicos. Se espera que el método, que implica la medición de las proteínas amiloides y tau en la sangre y en el líquido cefalorraquídeo, mejore los resultados de los ensayos clínicos ayudando a identificar mejor a los pacientes en las etapas más tempranas de la enfermedad.
Un equipo de científicos que trabajan en la Universidad Ruhr de Bochum (Bochum, Alemania) realizó un estudio prospectivo de 61 individuos de control de enfermedades (CE) y se adquirieron 39 casos de EA de un estudio prospectivo diseñado e iniciado por una unidad gerontopsiquiátrica del departamento de psiquiatría y psicoterapia entre 2009 y 2013. Para todos los individuos, estaban disponibles los niveles en el LCR de Aβ40, Aβ42, ttau, ptau, la proporción Aβ42/40 y los datos demográficos.
Todas las muestras de LCR se evaluaron con el kit multiplex del panel péptido Meso Scale Discovery V-PLEX Aβ, utilizando el anticuerpo monoclonal 6E10 para la detección (MSD, Rockville, MD, EUA). Los péptidos Aβ Aβ38, 40 y 42 se determinaron después de una dilución de 16 veces de las muestras de LCR con “Diluent 35” (MSD). Las concentraciones de ttau y ptau en el LCR se midieron por duplicado mediante un ELISA disponible comercialmente en un laboratorio experto acreditado para el diagnóstico de la demencia neuroquímica guiada por el LCR. Un sensor de inmuno-infrarrojo fue funcionalizado con un anticuerpo monoclonal para la detección de Aβ en el plasma sanguíneo y en el LCR y el anticuerpo monoclonal TAU-5 se usó para la detección de tau en el LCR, respectivamente. La banda de absorbancia de amida I registrada representó la distribución de la estructura secundaria del biomarcador en el fluido corporal respectivo por su frecuencia máxima.
Los científicos dijeron que, a través de la combinación de ambos análisis, 87 de 100 pacientes con Alzheimer se identificaron correctamente en su estudio y redujeron el número de diagnósticos falsos positivos en los individuos sanos a 3 de cada 100. El segundo análisis se realiza en el líquido cefalorraquídeo extraído de la médula espinal. En esta etapa, la segunda prueba de diagnóstico para las proteínas tau solo se puede medir utilizando líquido cefalorraquídeo. Debido a la naturaleza invasiva de la recolección de líquido cefalorraquídeo, el equipo admitió que esto no es lo ideal, y se trabaja para encontrar formas efectivas de detectar tau en muestras de sangre. Sin embargo, el proceso de dos pasos se puede implementar relativamente pronto en su forma actual, con la sugerencia de que la segunda prueba de líquido cefalorraquídeo solo se realice en aquellos individuos con resultados positivos en la primera prueba de sangre.
Klaus Gerwert, PhD, profesor y autor principal del estudio, dijo: “Ahora, se pueden iniciar nuevos estudios clínicos con participantes de prueba en etapas muy tempranas de la enfermedad. Recientemente, dos estudios prometedores importantes han fracasado, especialmente Crenezumab y Aducanumab, principalmente porque probablemente ya había sido demasiado tarde para cuando se inició la terapia. La nueva prueba abre una nueva ventana de terapia”. El estudio se publicó en línea el 12 de marzo de 2019 en la revista Alzheimer's & Dementia: Diagnosis, Assessment & Disease Monitor.
Enlace relacionado:
Universidad Ruhr de Bochum
Meso Scale Discovery
Un nuevo proceso de diagnóstico de dos pasos podría detectar la enfermedad de Alzheimer casi una década antes de que aparezcan los síntomas clínicos. Se espera que el método, que implica la medición de las proteínas amiloides y tau en la sangre y en el líquido cefalorraquídeo, mejore los resultados de los ensayos clínicos ayudando a identificar mejor a los pacientes en las etapas más tempranas de la enfermedad.
Un equipo de científicos que trabajan en la Universidad Ruhr de Bochum (Bochum, Alemania) realizó un estudio prospectivo de 61 individuos de control de enfermedades (CE) y se adquirieron 39 casos de EA de un estudio prospectivo diseñado e iniciado por una unidad gerontopsiquiátrica del departamento de psiquiatría y psicoterapia entre 2009 y 2013. Para todos los individuos, estaban disponibles los niveles en el LCR de Aβ40, Aβ42, ttau, ptau, la proporción Aβ42/40 y los datos demográficos.
Todas las muestras de LCR se evaluaron con el kit multiplex del panel péptido Meso Scale Discovery V-PLEX Aβ, utilizando el anticuerpo monoclonal 6E10 para la detección (MSD, Rockville, MD, EUA). Los péptidos Aβ Aβ38, 40 y 42 se determinaron después de una dilución de 16 veces de las muestras de LCR con “Diluent 35” (MSD). Las concentraciones de ttau y ptau en el LCR se midieron por duplicado mediante un ELISA disponible comercialmente en un laboratorio experto acreditado para el diagnóstico de la demencia neuroquímica guiada por el LCR. Un sensor de inmuno-infrarrojo fue funcionalizado con un anticuerpo monoclonal para la detección de Aβ en el plasma sanguíneo y en el LCR y el anticuerpo monoclonal TAU-5 se usó para la detección de tau en el LCR, respectivamente. La banda de absorbancia de amida I registrada representó la distribución de la estructura secundaria del biomarcador en el fluido corporal respectivo por su frecuencia máxima.
Los científicos dijeron que, a través de la combinación de ambos análisis, 87 de 100 pacientes con Alzheimer se identificaron correctamente en su estudio y redujeron el número de diagnósticos falsos positivos en los individuos sanos a 3 de cada 100. El segundo análisis se realiza en el líquido cefalorraquídeo extraído de la médula espinal. En esta etapa, la segunda prueba de diagnóstico para las proteínas tau solo se puede medir utilizando líquido cefalorraquídeo. Debido a la naturaleza invasiva de la recolección de líquido cefalorraquídeo, el equipo admitió que esto no es lo ideal, y se trabaja para encontrar formas efectivas de detectar tau en muestras de sangre. Sin embargo, el proceso de dos pasos se puede implementar relativamente pronto en su forma actual, con la sugerencia de que la segunda prueba de líquido cefalorraquídeo solo se realice en aquellos individuos con resultados positivos en la primera prueba de sangre.
Klaus Gerwert, PhD, profesor y autor principal del estudio, dijo: “Ahora, se pueden iniciar nuevos estudios clínicos con participantes de prueba en etapas muy tempranas de la enfermedad. Recientemente, dos estudios prometedores importantes han fracasado, especialmente Crenezumab y Aducanumab, principalmente porque probablemente ya había sido demasiado tarde para cuando se inició la terapia. La nueva prueba abre una nueva ventana de terapia”. El estudio se publicó en línea el 12 de marzo de 2019 en la revista Alzheimer's & Dementia: Diagnosis, Assessment & Disease Monitor.
Enlace relacionado:
Universidad Ruhr de Bochum
Meso Scale Discovery
Últimas Inmunología noticias
- Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
- Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
- Técnicas de vanguardia para investigar respuesta inmune en infecciones mortales por estreptococo A
- Novedosos inmunoensayos permiten diagnóstico temprano del síndrome antifosfolípido
- Nueva prueba podría predecir éxito de inmunoterapia para una gama más amplia de cánceres
- Pruebas simples de proteínas en sangre predicen resultados de CAR T para pacientes con linfoma
- Tecnología de chip clasificador de células podría allanar el camino para elaboración de perfiles inmunológicos POC
- Chip monitorea células cancerosas en muestras de sangre para evaluar eficacia del tratamiento
- Enfoques de inmunohematología automatizados pueden resolver incompatibilidad de trasplantes
- IA aprovecha genética tumoral para predecir respuesta del paciente a quimioterapia
- Primer dispositivo de monitoreo de leucocitos portátil y no invasivo del mundo elimina necesidad de extracción de sangre
- Prueba predictiva de células T detecta respuesta inmune a virus incluso antes de que se formen anticuerpos
- Analizador de inmunoensayo fluorescente portátil para pruebas POC rápidas transforma diagnósticos clínicos
- Detección multiparamétrica de autoanticuerpos ayuda a diagnosticar miositis
- Analizador CLIA todo en uno transforma el panorama del diagnóstico clínico
- Primera prueba de biomarcadores en sangre para predecir respuesta al tratamiento en pacientes con cáncer
Canales
Química Clínica
ver canal.jpg)
Prueba biomédica POC hace girar una gota de agua utilizando ondas sonoras para detección del cáncer
Los exosomas, pequeñas biopartículas celulares que transportan un conjunto específico de proteínas, lípidos y materiales genéticos, desempeñan un papel... Más
Prueba basada en células altamente confiable permite diagnóstico preciso de enfermedades endocrinas
Los métodos convencionales para medir el cortisol libre, la hormona del estrés del cuerpo, en la sangre o la saliva son bastante exigentes y requieren el procesamiento de muestras. Por lo tanto, el método... MásDiagnóstico Molecular
ver canal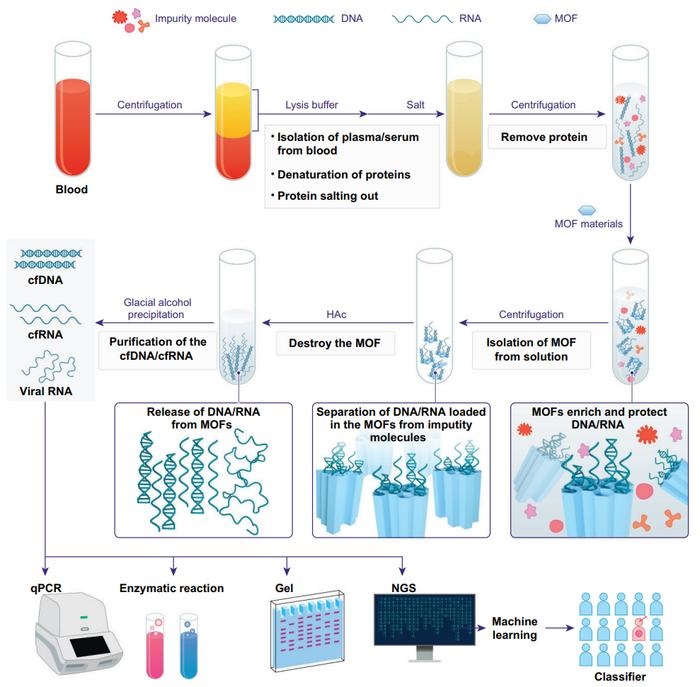
Técnica de enriquecimiento de ácido nucleico circulante en sangre permite diagnóstico no invasivo del cáncer de hígado
La capacidad de diagnosticar enfermedades de forma temprana puede optimizar significativamente la eficacia de los tratamientos clínicos y mejorar las tasas de supervivencia. Un enfoque prometedor... Más
Primera prueba molecular aprobada por la FDA para detectar malaria en donantes de sangre podría mejorar seguridad del paciente
La malaria, una enfermedad grave que a menudo provoca la muerte, se transmite por una especie específica de mosquito que infecta a los humanos con un parásito. Otros modos de transmisión... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más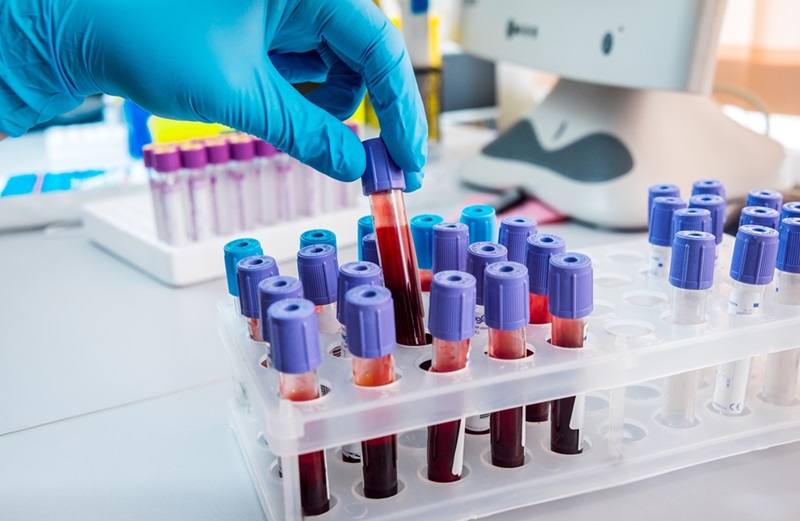
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal
Prueba simple de biopsia de piel detecta el Parkinson y enfermedades neurodegenerativas relacionadas
La enfermedad de Parkinson y un grupo de trastornos neurodegenerativos relacionados conocidos como sinucleinopatías afectan a millones de personas en todo el mundo. Estas afecciones, incluida la... Más.jpg)
Herramienta bioinformática para identificar alteraciones cromosómicas en células tumorales puede mejorar diagnóstico del cáncer
La inestabilidad cromosómica es una característica común en los tumores sólidos y desempeña un papel crucial en el inicio, la progresión y la propagación... Más
Dispositivo del tamaño de una moneda aísla rápidamente plasma sanguíneo para diagnósticos clínicos más rápidos y precisos
La identificación de biomarcadores para diversos cánceres y enfermedades a menudo se basa en ADN, ARN y vesículas extracelulares libres de células. Tradicionalmente, separar... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más












.jpg)
.jpg)
.jpg)