Exploran un candidato a biomarcador nuevo para la esclerosis lateral amiotrófica
|
Por el equipo editorial de LabMedica en español Actualizado el 22 Dec 2020 |
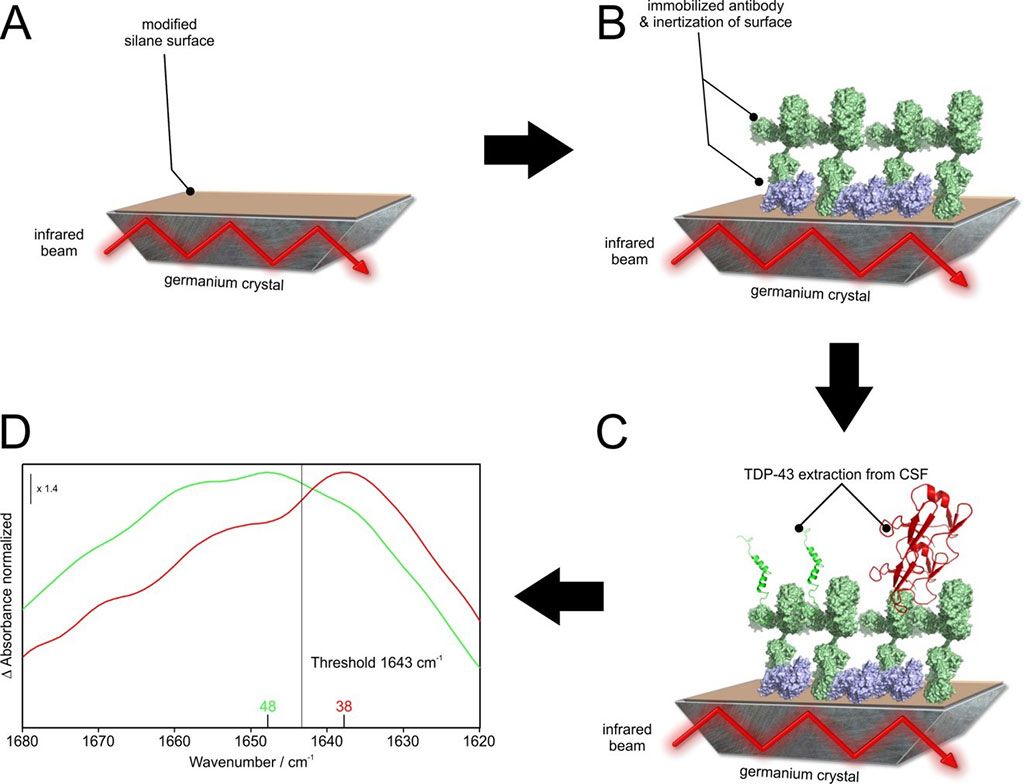
Imagen: Ilustración esquemática del sensor inmunoinfrarrojo. Usando anticuerpos de captura oligoclonales, todas las isoformas de TDP-43 se extraen del LCR (Fotografía cortesía de la Universidad de Ruhr en Bochum).
La esclerosis lateral amiotrófica (ELA) es una enfermedad neurodegenerativa mortal que provoca una pérdida rápida de la función motora, que suele terminar en una enfermedad grave con muerte prematura en unos pocos años. Hasta ahora, el diagnóstico precoz y preciso de la enfermedad ha sido difícil.
Hasta la fecha, uno de los desafíos clave en el diagnóstico de la ELA es excluir otras enfermedades similares, que se evalúan en función de parámetros clínicos y electrofisiológicos, mientras que aún faltan biomarcadores de diagnóstico y pronóstico específicos de la enfermedad. En la ELA, la proteína TDP-43, en particular, juega un papel fundamental. Forma pequeñas inclusiones en las células nerviosas. Las inclusiones de TDP-43 parecen tener un significado patomecanístico crucial y son los marcadores neuropatológicos en casos esporádicos y en muchos casos de ELA genéticos.
Un equipo multidisciplinario de científicos, que trabaja con la Universidad del Ruhr en Bochum (Bochum, Alemania), analizó la distribución de la estructura secundaria de TDP-43 en el líquido cefalorraquídeo de 36 pacientes con ELA, y compararon con la de 30 pacientes con enfermedad de Parkinson (EP) y 34 controles adicionales (Ctrl), utilizando la tecnología de sensor inmunoinfrarrojo. El sensor inmunoinfrarrojo es una tecnología universal que proporciona una medida relativa que refleja directamente la distribución de la estructura secundaria de un biomarcador en un fluido biológico. Las muestras se analizan en un sistema de flujo continuo.
El equipo logró obtener un diagnóstico de ELA basado en la estructura alterada de la proteína TDP-43. En el proceso, demostraron que las proteínas se pliegan desde estructuras predominantemente desordenadas y helicoidales hasta las llamadas láminas ß. Estas formas promueven ensamblajes dañados y depósitos de proteínas en las células nerviosas. En el análisis, se distinguieron 36 pacientes con ELA de 30 pacientes con Parkinson mediante la señal TDP-43 con una sensibilidad del 89% y una especificidad del 77%. Además, un grupo de control, con pacientes neurológicamente discretos, fue diferenciado con una sensibilidad del 89% y una especificidad del 83%. Al analizar la TDP-43, los investigadores pudieron excluir otras enfermedades que afectan la función motora, como la enfermedad de Parkinson.
Léon Beyer, MSc, uno de los autores principales del estudio y estudiante de doctorado en el Departamento de Biospectroscopia de Prodi, dijo: “Este logro puede proporcionar una nueva perspectiva sobre los mecanismos de la enfermedad. En comparación con otros métodos que reflejan concentraciones de ciertas proteínas, nuestra tecnología de sensores infrarrojos brinda información sobre los eventos moleculares y, por lo tanto, puede convertirse en una herramienta crucial en el futuro para diagnosticar y desarrollar terapias clínicas. No obstante, ante todo, contribuirá en gran medida a una comprensión más precisa de las enfermedades”.
Los autores concluyeron que sus hallazgos demuestran que el plegamiento incorrecto de TDP-43, medido por la tecnología del sensor inmunoinfrarrojo, tiene el potencial de servir como un biomarcador candidato para la ELA. El estudio fue publicado el 3 de diciembre de 2020 en la revista Annals of Clinical and Translational Neurology.
Enlace relacionado:
Universidad del Ruhr en Bochum
Hasta la fecha, uno de los desafíos clave en el diagnóstico de la ELA es excluir otras enfermedades similares, que se evalúan en función de parámetros clínicos y electrofisiológicos, mientras que aún faltan biomarcadores de diagnóstico y pronóstico específicos de la enfermedad. En la ELA, la proteína TDP-43, en particular, juega un papel fundamental. Forma pequeñas inclusiones en las células nerviosas. Las inclusiones de TDP-43 parecen tener un significado patomecanístico crucial y son los marcadores neuropatológicos en casos esporádicos y en muchos casos de ELA genéticos.
Un equipo multidisciplinario de científicos, que trabaja con la Universidad del Ruhr en Bochum (Bochum, Alemania), analizó la distribución de la estructura secundaria de TDP-43 en el líquido cefalorraquídeo de 36 pacientes con ELA, y compararon con la de 30 pacientes con enfermedad de Parkinson (EP) y 34 controles adicionales (Ctrl), utilizando la tecnología de sensor inmunoinfrarrojo. El sensor inmunoinfrarrojo es una tecnología universal que proporciona una medida relativa que refleja directamente la distribución de la estructura secundaria de un biomarcador en un fluido biológico. Las muestras se analizan en un sistema de flujo continuo.
El equipo logró obtener un diagnóstico de ELA basado en la estructura alterada de la proteína TDP-43. En el proceso, demostraron que las proteínas se pliegan desde estructuras predominantemente desordenadas y helicoidales hasta las llamadas láminas ß. Estas formas promueven ensamblajes dañados y depósitos de proteínas en las células nerviosas. En el análisis, se distinguieron 36 pacientes con ELA de 30 pacientes con Parkinson mediante la señal TDP-43 con una sensibilidad del 89% y una especificidad del 77%. Además, un grupo de control, con pacientes neurológicamente discretos, fue diferenciado con una sensibilidad del 89% y una especificidad del 83%. Al analizar la TDP-43, los investigadores pudieron excluir otras enfermedades que afectan la función motora, como la enfermedad de Parkinson.
Léon Beyer, MSc, uno de los autores principales del estudio y estudiante de doctorado en el Departamento de Biospectroscopia de Prodi, dijo: “Este logro puede proporcionar una nueva perspectiva sobre los mecanismos de la enfermedad. En comparación con otros métodos que reflejan concentraciones de ciertas proteínas, nuestra tecnología de sensores infrarrojos brinda información sobre los eventos moleculares y, por lo tanto, puede convertirse en una herramienta crucial en el futuro para diagnosticar y desarrollar terapias clínicas. No obstante, ante todo, contribuirá en gran medida a una comprensión más precisa de las enfermedades”.
Los autores concluyeron que sus hallazgos demuestran que el plegamiento incorrecto de TDP-43, medido por la tecnología del sensor inmunoinfrarrojo, tiene el potencial de servir como un biomarcador candidato para la ELA. El estudio fue publicado el 3 de diciembre de 2020 en la revista Annals of Clinical and Translational Neurology.
Enlace relacionado:
Universidad del Ruhr en Bochum
Últimas Inmunología noticias
- Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
- Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
- Técnicas de vanguardia para investigar respuesta inmune en infecciones mortales por estreptococo A
- Novedosos inmunoensayos permiten diagnóstico temprano del síndrome antifosfolípido
- Nueva prueba podría predecir éxito de inmunoterapia para una gama más amplia de cánceres
- Pruebas simples de proteínas en sangre predicen resultados de CAR T para pacientes con linfoma
- Tecnología de chip clasificador de células podría allanar el camino para elaboración de perfiles inmunológicos POC
- Chip monitorea células cancerosas en muestras de sangre para evaluar eficacia del tratamiento
- Enfoques de inmunohematología automatizados pueden resolver incompatibilidad de trasplantes
- IA aprovecha genética tumoral para predecir respuesta del paciente a quimioterapia
- Primer dispositivo de monitoreo de leucocitos portátil y no invasivo del mundo elimina necesidad de extracción de sangre
- Prueba predictiva de células T detecta respuesta inmune a virus incluso antes de que se formen anticuerpos
- Analizador de inmunoensayo fluorescente portátil para pruebas POC rápidas transforma diagnósticos clínicos
- Detección multiparamétrica de autoanticuerpos ayuda a diagnosticar miositis
- Analizador CLIA todo en uno transforma el panorama del diagnóstico clínico
- Primera prueba de biomarcadores en sangre para predecir respuesta al tratamiento en pacientes con cáncer
Canales
Diagnóstico Molecular
ver canal
Enfoque revolucionario de análisis de células T permite detección temprana del cáncer
La biopsia líquida, un método para diagnosticar el cáncer mediante análisis de sangre de rutina, es una herramienta potencial importante para la detección temprana del... MásPrueba genética única podría acelerar el diagnóstico de trastornos raros del desarrollo
Las alteraciones en el ADN humano varían desde variaciones menores de un solo nucleótido hasta alteraciones sustanciales que implican la eliminación o duplicación de segmentos... Más
Analizador de pruebas sindrómicas actualizado permite acceso remoto a resultados de pruebas
QIAGEN (Venlo, Países Bajos) ha lanzado el analizador QIAstat-Dx 2.0, incluida la actualización del software 1.6. Esto representa un avance significativo con respecto al analizador QIAstat-Dx 1.... Más
Prueba de PCR para infecciones respiratorias y de garganta detecta múltiples patógenos con síntomas coincidentes
La pandemia de COVID-19 ha demostrado la necesidad de que los profesionales de la salud tengan pruebas de diagnóstico disponibles lo más cerca posible del paciente, proporcionando resultados... MásHematología
ver canal
Prueba de sangre POC por punción digital determina riesgo de sepsis neutropénica en pacientes sometidos a quimioterapia
La neutropenia, una disminución de los neutrófilos (un tipo de glóbulo blanco crucial para combatir las infecciones), es un efecto secundario frecuente de ciertos tratamientos contra... Más
Primera prueba rápida y asequible para beta talasemia demuestra precisión diagnóstica del 99 %
Los trastornos de la hemoglobina se encuentran entre las enfermedades monogénicas más prevalentes a nivel mundial. Entre los diversos trastornos de la hemoglobina, la beta talasemia, un trastorno sanguíneo... MásRastreador portátil de glóbulos blancos podría permitir pruebas rápidas de infecciones
Los glóbulos blancos, o leucocitos, son indicadores clave de la salud del sistema inmunológico de un individuo. Los recuentos altos o bajos de leucocitos pueden indicar la gravedad de una infección, indicar... MásAnalizador hematológico optofluídico inteligente del tamaño de la palma de la mano permite realizar pruebas POC de células sanguíneas del paciente
Las variaciones en la concentración de células sanguíneas pueden ser indicativas de varias condiciones de salud, incluidas infecciones, enfermedades inflamatorias, trastornos sanguíneos... MásInmunología
ver canal
Método de prueba podría ayudar a más pacientes recibir tratamiento adecuado contra el cáncer
El tratamiento del cáncer no siempre es una solución única, pero el campo de la investigación del cáncer está dando grandes pasos para encontrar a los pacientes los tratamientos más eficaces para sus afecciones... Más
Prueba innovadora monitorea toxicidad de radioterapia en pacientes con cáncer
La concentración de ADN libre de células circulante (ADNlc) en el torrente sanguíneo es un indicador importante que puede ayudar a rastrear qué tan bien están funcionando... MásMicrobiología
ver canal
Análisis de sangre predice sepsis e insuficiencia orgánica en niños
La sepsis plantea un riesgo grave en el que una reacción inmune grave a la infección provoca daño a los órganos. Identificar la sepsis en niños es complejo ya que los... Más
Análisis de sangre para tuberculosis podría detectar millones de propagadores silenciosos
La tuberculosis (TB) es la enfermedad infecciosa más mortal del mundo y se cobra más de un millón de vidas al año, según informa la Organización Mundial de la Salud.... Más
Un análisis de sangre simple combinado con un modelo de riesgo personalizado mejora el diagnóstico de sepsis
La sepsis, una afección crítica que surge de la disfunción orgánica debido a una infección grave, puede progresar a una sepsis grave y un shock séptico, lo que provoca insuficiencia multiorgánica y un... Más
Nuevo análisis de sangre reduce tiempo de diagnóstico de infecciones por micobacterias no tuberculosas de meses a horas
Respirar micobacterias no tuberculosas (MNT) es una experiencia común para muchas personas. Estas bacterias están presentes en los sistemas de agua, el suelo y el polvo de todo el mundo y,... MásPatología
ver canal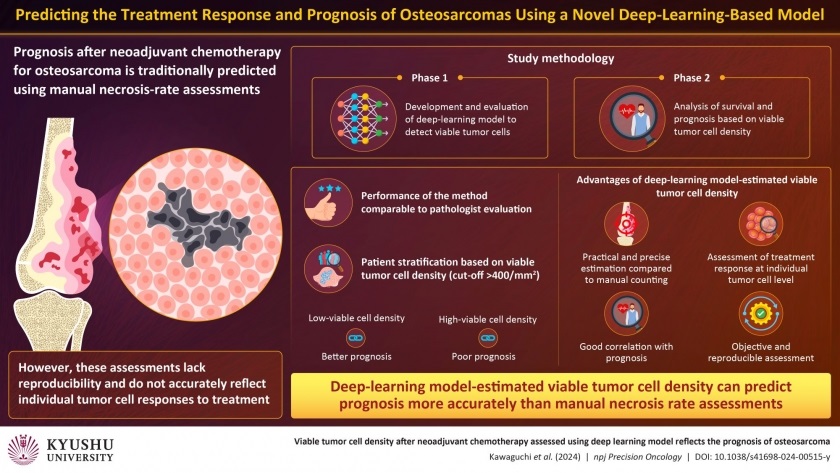
Inteligencia artificial detecta células tumorales viables para pronósticos precisos de cáncer de hueso después de quimioterapia
El osteosarcoma, el tumor óseo maligno más común, ha mostrado tasas de supervivencia mejoradas con cirugía y quimioterapia para casos localizados. Sin embargo, el pronóstico... Más
Nueva técnica identifica células cancerosas individuales en sangre para tratamientos específicos
La comunidad médica mundial reconoce cada vez más que la biopsia líquida es un enfoque transformador para mejorar la atención al paciente con cáncer. Este innovador método de diagnóstico implica detectar... MásTecnología
ver canal
Biosensor de ADN permite diagnóstico temprano del cáncer de cuello uterino
El disulfuro de molibdeno (MoS2), reconocido por su potencial para formar nanoláminas bidimensionales como el grafeno, es un material que llama cada vez más la atención de la comunidad... Más
Dispositivos de microfluidos autocalentables pueden detectar enfermedades en pequeñas muestras de sangre o fluidos
Los microfluidos, que son dispositivos en miniatura que controlan el flujo de líquidos y facilitan reacciones químicas, desempeñan un papel clave en la detección de enfermedades... Más
Avance en tecnología de diagnóstico podría hacer que pruebas en el sitio sean ampliamente accesibles
Las pruebas caseras adquirieron una importancia significativa durante la pandemia de COVID-19, sin embargo, la disponibilidad de pruebas rápidas es limitada y la mayoría de ellas solo pueden conducir un... MásIndustria
ver canal
Congreso ECCMID cambia de nombre a ESCMID Global
En los últimos años, la Sociedad Europea de Microbiología Clínica y Enfermedades Infecciosas (ESCMID, Basilea, Suiza) ha evolucionado notablemente. La sociedad es ahora más... Más











.jpg)