Comparan los métodos automatizados para la determinación de anticuerpos citoplasmáticos anti-neutrófilos
|
Por el equipo editorial de LabMedica en español Actualizado el 19 Oct 2020 |
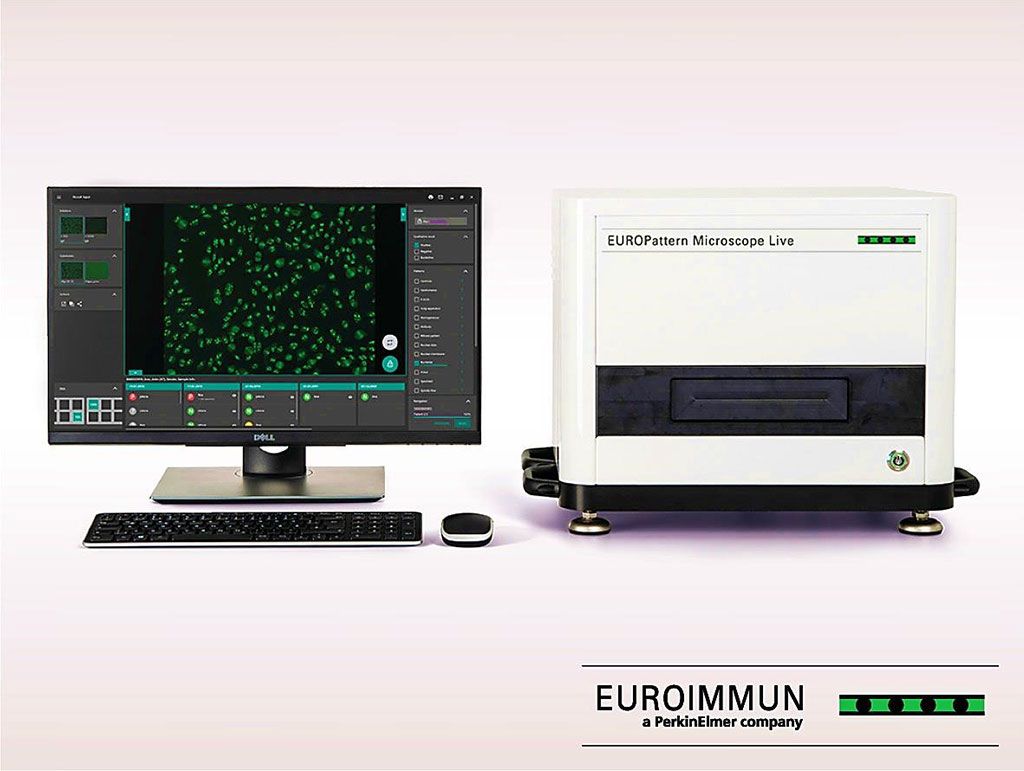
Imagen: EUROPattern Microscope Live: microscopía de fluorescencia ultrarrápida que detecta automáticamente anticuerpos anticitoplasma de neutrófilos (Fotografía cortesía de EUROIMMUN AG).
La detección de anticuerpos anticitoplasma de neutrófilos (ANCA) mediante ensayos de inmunofluorescencia indirecta (IFA) es de importancia diagnóstica en las vasculitis y algunas otras enfermedades inflamatorias.
Varios laboratorios utilizan neutrófilos fijados con formaldehído como sustrato auxiliar además de la fijación con etanol convencional, que ha sido informada como de utilidad para diferenciar entre anticuerpos antinucleares y ANCA y mejora la interpretación de patrones. Muchos, especialmente los laboratorios de alto rendimiento, consideran que los métodos de inmunofluorescencia indirecta (IFI) son engorrosos, requieren mucho tiempo y trabajo.
Un equipo de científicos clínicos de la Universidad de Debrecen (Debrecen, Hungría), recolectó muestras de suero de 570 personas, cuyas referencias eran sospecha o seguimiento de insuficiencia renal aguda y crónica, colitis ulcerativa, enfermedad de Crohn, enfermedades autoinmunes sistémicas, vasculitis y trastornos hepáticos autoinmunes. Cinco pacientes proporcionaron dos muestras.
La prueba de inmunofluorescencia indirecta se realizó utilizando un kit de reactivos diseñado para ser utilizado con EUROPattern (EPa), el microscopio de inmunofluorescencia asistido por computadora de EUROIMMUN (Granulocyte Mosaic 13; EUROIMMUN AG, Lübeck, Alemania). Un área de reacción en el portaobjetos del microscopio contiene tres biochips (cubreobjetos de 2 x 2 mm, recubiertos de sustrato), cubiertos por neutrófilos humanos fijados con etanol o formaldehído o granulocitos esparcidos sobre una capa de células HEp-2, respectivamente. Se utilizó como anticuerpo secundario (conjugado) una anti-IgG humana de cabra marcada con isotiocianato de fluoresceína, que se complementó con colorante azul de Evans para la contracoloración de rojo de las células.
Los portaobjetos se procesaron manualmente y la dilución para el cribado de las muestras de suero fue 1:10. Los resultados automáticos y las imágenes digitales se presentaron al usuario en una pantalla de computadora calibrada, quien verificó y validó los patrones. Finalmente, los portaobjetos se evaluaron mediante lectura visual tradicional bajo un microscopio de epifluorescencia (EUROStar II Plus, EUROIMMUN AG).
El equipo informó que la concordancia de discriminación entre muestras negativas y no negativas fue del 86,1% comparando la lectura de EPa con la convencional, y aumentó al 96,7% después de la validación del usuario en la pantalla. Es importante destacar que de las 334 muestras clasificadas como negativas por EPa, 328 (98,2%) también fueron negativas según la evaluación convencional. El reconocimiento de patrones mostró una concordancia “moderada” entre el análisis microscópico clásico y el de EPa y una concordancia “muy buena” después de la validación del usuario. La clasificación errónea por EPa se debió predominantemente a la presencia de anticuerpos antinucleares/citoplasmáticos (patrón incorrecto, 80/568) y al menor límite de fluorescencia del microscopio automático (falsos positivos, 73/568).
Los autores concluyeron que la prueba ANCA automatizada por EPa es una alternativa confiable de la evaluación microscópica clásica, aunque la clasificación de sueros necesita ser corregida por personal capacitado durante la validación en la pantalla. El estudio fue publicado el 28 de septiembre de 2020 en la revista Clinica Chimica Acta.
Enlace relacionado:
Universidad de Debrecen
Varios laboratorios utilizan neutrófilos fijados con formaldehído como sustrato auxiliar además de la fijación con etanol convencional, que ha sido informada como de utilidad para diferenciar entre anticuerpos antinucleares y ANCA y mejora la interpretación de patrones. Muchos, especialmente los laboratorios de alto rendimiento, consideran que los métodos de inmunofluorescencia indirecta (IFI) son engorrosos, requieren mucho tiempo y trabajo.
Un equipo de científicos clínicos de la Universidad de Debrecen (Debrecen, Hungría), recolectó muestras de suero de 570 personas, cuyas referencias eran sospecha o seguimiento de insuficiencia renal aguda y crónica, colitis ulcerativa, enfermedad de Crohn, enfermedades autoinmunes sistémicas, vasculitis y trastornos hepáticos autoinmunes. Cinco pacientes proporcionaron dos muestras.
La prueba de inmunofluorescencia indirecta se realizó utilizando un kit de reactivos diseñado para ser utilizado con EUROPattern (EPa), el microscopio de inmunofluorescencia asistido por computadora de EUROIMMUN (Granulocyte Mosaic 13; EUROIMMUN AG, Lübeck, Alemania). Un área de reacción en el portaobjetos del microscopio contiene tres biochips (cubreobjetos de 2 x 2 mm, recubiertos de sustrato), cubiertos por neutrófilos humanos fijados con etanol o formaldehído o granulocitos esparcidos sobre una capa de células HEp-2, respectivamente. Se utilizó como anticuerpo secundario (conjugado) una anti-IgG humana de cabra marcada con isotiocianato de fluoresceína, que se complementó con colorante azul de Evans para la contracoloración de rojo de las células.
Los portaobjetos se procesaron manualmente y la dilución para el cribado de las muestras de suero fue 1:10. Los resultados automáticos y las imágenes digitales se presentaron al usuario en una pantalla de computadora calibrada, quien verificó y validó los patrones. Finalmente, los portaobjetos se evaluaron mediante lectura visual tradicional bajo un microscopio de epifluorescencia (EUROStar II Plus, EUROIMMUN AG).
El equipo informó que la concordancia de discriminación entre muestras negativas y no negativas fue del 86,1% comparando la lectura de EPa con la convencional, y aumentó al 96,7% después de la validación del usuario en la pantalla. Es importante destacar que de las 334 muestras clasificadas como negativas por EPa, 328 (98,2%) también fueron negativas según la evaluación convencional. El reconocimiento de patrones mostró una concordancia “moderada” entre el análisis microscópico clásico y el de EPa y una concordancia “muy buena” después de la validación del usuario. La clasificación errónea por EPa se debió predominantemente a la presencia de anticuerpos antinucleares/citoplasmáticos (patrón incorrecto, 80/568) y al menor límite de fluorescencia del microscopio automático (falsos positivos, 73/568).
Los autores concluyeron que la prueba ANCA automatizada por EPa es una alternativa confiable de la evaluación microscópica clásica, aunque la clasificación de sueros necesita ser corregida por personal capacitado durante la validación en la pantalla. El estudio fue publicado el 28 de septiembre de 2020 en la revista Clinica Chimica Acta.
Enlace relacionado:
Universidad de Debrecen
Últimas Hematología noticias
- Prueba rápida en cartuchos busca ampliar acceso al diagnóstico de trastornos de hemoglobina
- Nuevas directrices buscan mejorar diagnóstico de amiloidosis AL
- Sistema automatizado de hemostasia ayuda a laboratorios a optimizar flujo de trabajo
- Prueba rápida y sencilla podría revolucionar transfusiones de sangre
- Análisis de sangre muy sensible mejora evaluación del riesgo de coagulación en pacientes cardíacos
- Algoritmo de IA distingue eficazmente subtipos de alfa talasemia
- Pruebas de MRD podrían predecir supervivencia en pacientes con leucemia
- Análisis sanguíneo de actividad plaquetaria en mediana edad podría identificar riesgo temprano de Alzheimer
- Medición de microvesículas podría detectar lesiones vasculares en pacientes con anemia falciforme
- Nueva guía de ADLM sobre pruebas de coagulación mejora atención a pacientes que toman anticoagulantes
- Pruebas viscoelásticas podrían mejorar tratamiento de hemorragia materna
- Modelo mide exposición a radiación en sangre para tratamientos precisos contra cáncer
- Las plaquetas podrían mejorar detección temprana y mínimamente invasiva del cáncer
- Dispositivo portátil desechable obtiene plasma rico en plaquetas sin equipos complejos
- Prueba de cartucho desechable ofrece resultados de hemograma rápidos y precisos
- Primera prueba de monitorización de heparina POC proporciona resultados rápidos

Canales
Química Clínica
ver canal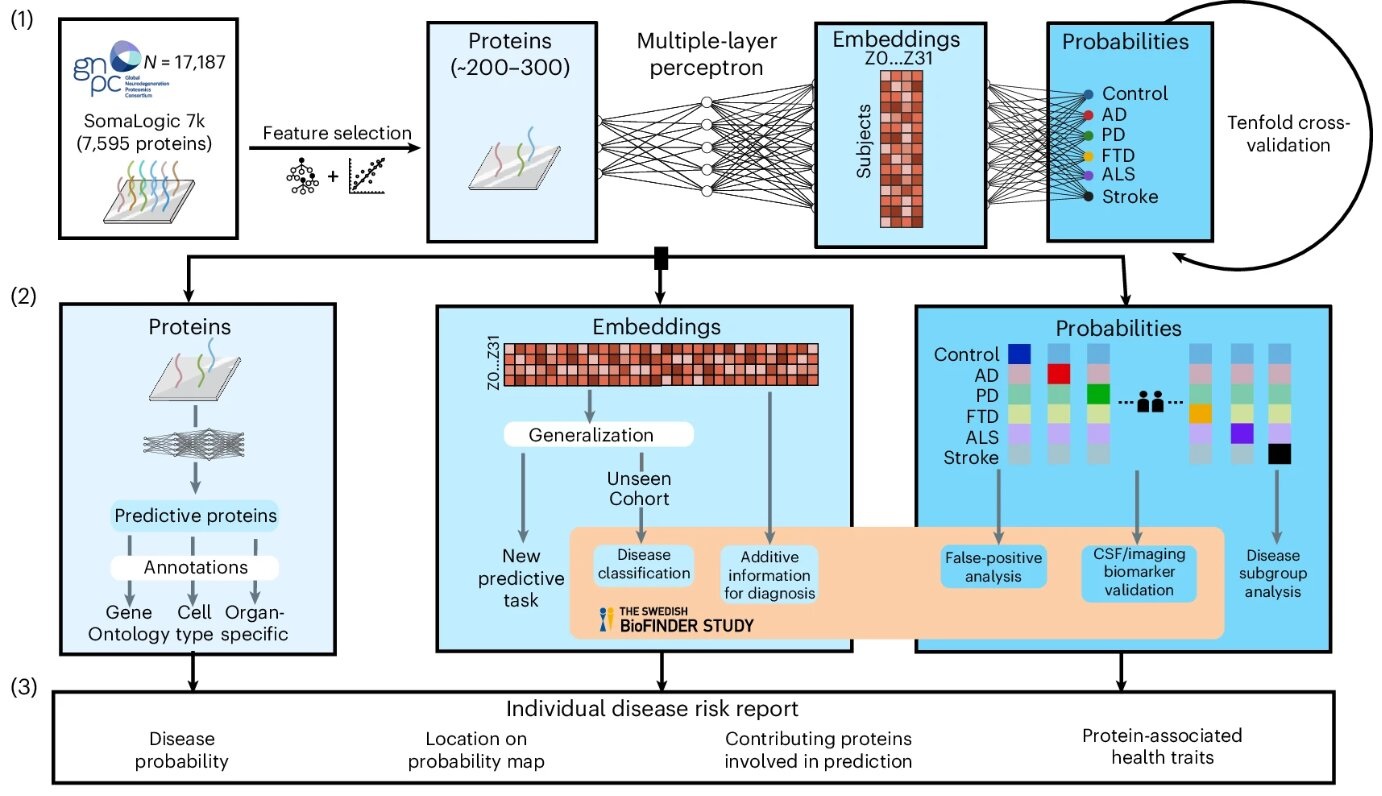
Análisis de sangre basado en IA detecta múltiples trastornos cerebrales a partir de una sola muestra
Diagnosticar la causa de los síntomas cognitivos relacionados con la edad sigue siendo un desafío, ya que las manifestaciones clínicas de las enfermedades neurodegenerativas a menudo se superponen y pueden... Más
Un ensayo automatizado de NfL respalda el seguimiento de trastornos neurológicos
La lesión neuroaxonal ocurre en una amplia gama de trastornos neurológicos y sigue siendo difícil de monitorizar de forma no invasiva a lo largo del tiempo. La medición en sangre... MásDiagnóstico Molecular
ver canal
La secuenciación del genoma completo en la atención médica rutinaria amplía la detección de enfermedades raras
Las enfermedades raras suelen implicar largos procesos diagnósticos que retrasan la toma de decisiones clínicas y complican la planificación familiar. A medida que los fenotipos se... Más
Nueva herramienta de IA mejora la detección de causas genéticas en enfermedades raras
Las familias afectadas por enfermedades raras suelen sufrir años de pruebas inconclusas y derivaciones fragmentadas antes de obtener un diagnóstico definitivo. A pesar del amplio acceso a... MásPlataforma de PCR adaptativa mejora la consistencia en flujos de trabajo de NGS de lotes pequeños
La amplificación por PCR durante la preparación de bibliotecas para secuenciación de nueva generación (NGS) puede introducir variabilidad, lo que a menudo requiere cuantificación manual y conlleva el riesgo... MásHematología
ver canal
Prueba rápida en cartuchos busca ampliar acceso al diagnóstico de trastornos de hemoglobina
La anemia de células falciformes y la beta talasemia son trastornos de la hemoglobina que a menudo requieren la derivación a laboratorios especializados para un diagnóstico definitivo,... Más
Nuevas directrices buscan mejorar diagnóstico de amiloidosis AL
La amiloidosis de cadenas ligeras (AL) es un trastorno poco común y potencialmente mortal de la médula ósea, en el que las proteínas amiloides anormales se acumulan en los órganos. Aproximadamente 3.... MásMicrobiología
ver canal
Nuevo objetivo bacteriano identificado para la detección temprana del noma
La noma es una infección orofacial de rápida progresión que comienza como gingivitis y puede destruir los tejidos orales y faciales, afectando principalmente a niños pequeños... Más
Prueba rápida de orina acelera la selección de antibióticos para infecciones del tracto urinario
Las infecciones del tracto urinario son una causa frecuente de prescripción de antibióticos y han provocado más de 800.000 hospitalizaciones en Inglaterra en los últimos cinco... Más
El análisis genómico vincula cepas estreptocócicas emergentes con infecciones específicas
Las infecciones por Streptococcus dysgalactiae subespecie equisimilis (SDSE) están aumentando en todo el mundo e incluyen variantes que pueden provocar enfermedades graves. Investigadores informan... Más
La OMS respalda las pruebas rápidas en el punto de atención para mejorar la detección de tuberculosis
La tuberculosis (TB) sigue siendo una de las principales causas de muerte por enfermedades infecciosas, con más de 3.300 fallecimientos y 29.000 nuevos casos diarios. Los retrasos en el diagnóstico... MásPatología
ver canal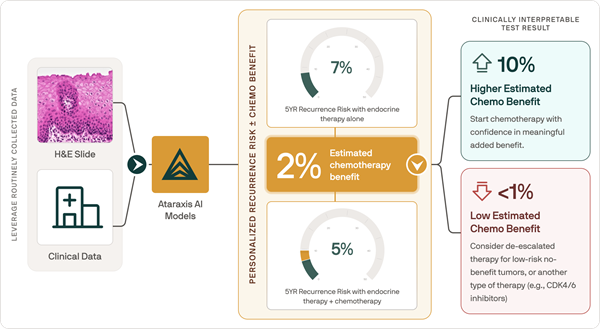
Nueva prueba de IA predice resultados de quimioterapia específicos para cada paciente con cáncer de mama
La selección de la quimioterapia adyuvante para el cáncer de mama en estadio temprano suele basarse en el riesgo de recurrencia y los promedios poblacionales, en lugar del beneficio individualizado... Más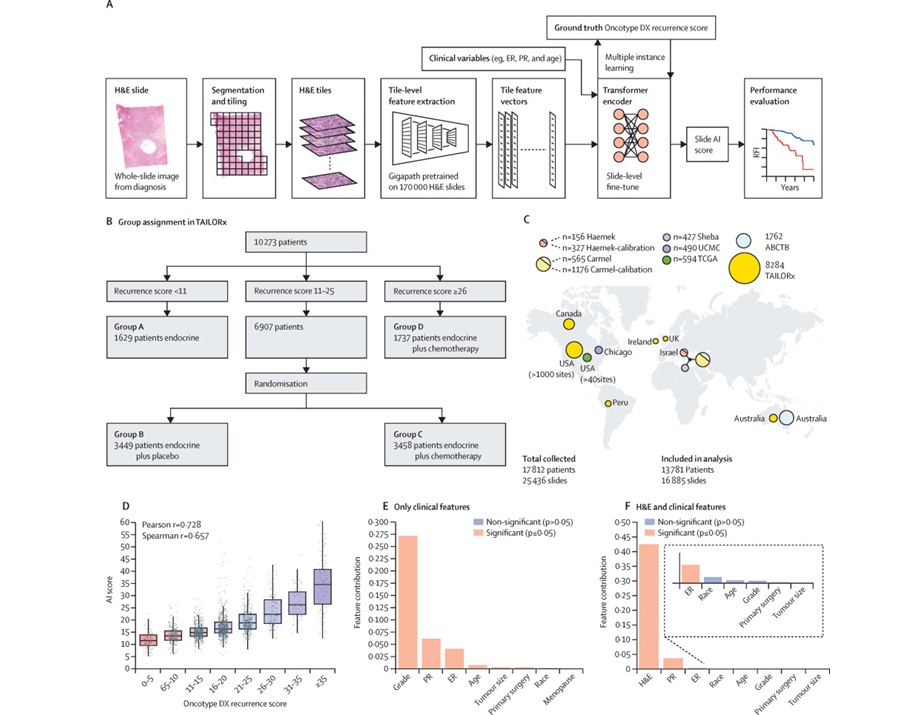
Modelo patológico basado en IA guía las decisiones de quimioterapia en cáncer de mama.
La selección de quimioterapia adyuvante para el cáncer de mama en etapa temprana sigue siendo una decisión difícil, ya que solo un subgrupo de pacientes se beneficia, mientras... MásTecnología
ver canal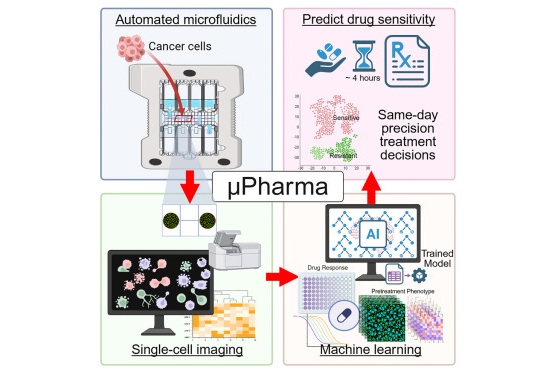
Nueva herramienta de IA permite seleccionar rápidamente el tratamiento en leucemia pediátrica
Los niños con leucemia linfoblástica aguda de células T se enfrentan a una enfermedad agresiva que sigue siendo difícil de tratar. Si bien las tasas de remisión han mejorado,... Más
Diseño innovador de espectrometría de masas podría permitir la detección de abundancias ultrabajas
La espectrometría de masas es fundamental para identificar y cuantificar moléculas en muestras biológicas complejas, pero los instrumentos convencionales suelen analizar los iones... MásIndustria
ver canal
Integrated DNA Technologies se expande al ámbito del diagnóstico clínico
Integrated DNA Technologies (IDT; Coralville, Iowa, EE. UU.) ha anunciado el lanzamiento de Archer FUSIONPlex-HT Dx y VARIANTPlex-HT Dx. Este lanzamiento marca la primera oferta de diagnóstico in... Más