Reportan la predicción temprana de resistencia a los inhibidores a la tirosina quinasa
|
Por el equipo editorial de LabMedica en español Actualizado el 31 Mar 2020 |
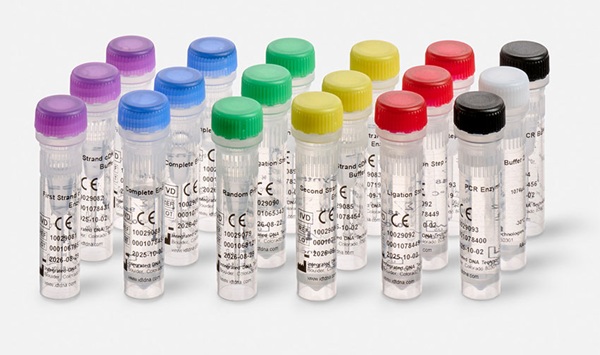
Imagen: Prueba cobas para la Mutación del gen del Receptor del Factor de Crecimiento Epidérmico (EGFR) v2 (Fotografía cortesía de Roche).
Las mutaciones genéticas del receptor del factor de crecimiento epidérmico (EGFR) que confieren sensibilidad a los inhibidores de la tirosina quinasa (TKI) en los carcinomas de pulmón de células no pequeñas allanaron el camino para un método de medicina de precisión en esta forma neoplásica.
En el momento del diagnóstico clínico, la detección de mutaciones de EGFR en tejido tumoral o de ADN tumoral circulante (ADNc), cuando el tejido no está disponible, es obligatoria para la selección de pacientes. Un número limitado de estudios realizados con métodos cuantitativos o semicuantitativos de detección de mutaciones han sugerido una correlación entre la cantidad del alelo mutante EGFR sensibilizante (sEGFRma) en plasma y la carga tumoral.
El especialista en oncología de la Universidad de Chieti (Chieti, Italia) y sus colegas, evaluaron a 116 pacientes con cáncer de pulmón de células no pequeñas (CPCNP) en estadio IIIB/IV, portadores de mutaciones EGFR en sus tumores y tratados con anti-EGFR TKI de primera/segunda generación, para la mutación T790M en la progresión clínica mediante biopsia líquida o biopsias tumorales repetidas.
Se obtuvieron dos muestras de sangre en cada recolección, se efectuó la separación del plasma y se almacenaron a -80°C hasta la extracción del ADN. El ADN se extrajo del plasma usando el kit de preparación de muestras de ADNc cobas vers.2 (Roche Molecular Systems, Pleasanton, CA, EUA) y se recuperó en 200 μL de tampón de elución. La mitad del volumen se usó inmediatamente para la evaluación de la mutación EGFR mediante el ensayo v2 de prueba de mutación cobas EGFR de Roche. Las reacciones en cadena de la polimerasa (PCR) se realizaron en el analizador Roche cobas z480. Se utilizó un enfoque innovador de secuenciación masiva paralela (MPS) (SureSelect Cancer All-In-One; Agilent Technologies, Santa Clara, California, EUA) para optimizar el manejo del material biológico.
El equipo informó que el análisis de plasma mediante la prueba EGFR Cobas mostró en 57 (89%) casos una disminución sustancial en los niveles del alelo mutante de EGFR sensibilizante (sEGFRma), hasta un valor no detectable. Estos pacientes se definieron como buenos respondedores plasmáticos (PGR). En siete pacientes (11%), el sEGFRma no cayó a cero (respondedores plasmáticos malos, PPR). En estos últimos casos, el análisis de secuenciación paralela masiva (MPS) al final del primer mes y en la progresión clínica mostró la presencia de mutaciones inductoras resistentes, incluidas la amplificación de genes MET y HER2, mutaciones de los genes KRAS y PIK3CA. Los PPR mostraron progresión de la enfermedad en cinco (71%) casos, enfermedad estable en dos (29%) casos y una mediana de supervivencia libre de progresión (SLP) más corta (4,3 ± 1,1 meses) que la observada para los PGR (13,3 ± 1,2 meses).
Los autores concluyeron que sus resultados indican que un subconjunto de pacientes con CPCNM sometidos a un tratamiento de segunda línea con osimertinib son resistentes al tratamiento debido a la presencia de diferentes tipos de mutaciones. La monitorización plasmática mediante una prueba de mutación de EGFR basada en RT-PCR simple en el primer mes de tratamiento puede ser útil para identificar rápidamente estos casos y someterlos a análisis de MPS para una caracterización y tratamiento adicionales. El estudio fue publicado el 17 de marzo de 2020 en la revista Oncotarget.
Enlace relacionado:
Universidad de Chieti
Roche Molecular Systems
Agilent Technologies
En el momento del diagnóstico clínico, la detección de mutaciones de EGFR en tejido tumoral o de ADN tumoral circulante (ADNc), cuando el tejido no está disponible, es obligatoria para la selección de pacientes. Un número limitado de estudios realizados con métodos cuantitativos o semicuantitativos de detección de mutaciones han sugerido una correlación entre la cantidad del alelo mutante EGFR sensibilizante (sEGFRma) en plasma y la carga tumoral.
El especialista en oncología de la Universidad de Chieti (Chieti, Italia) y sus colegas, evaluaron a 116 pacientes con cáncer de pulmón de células no pequeñas (CPCNP) en estadio IIIB/IV, portadores de mutaciones EGFR en sus tumores y tratados con anti-EGFR TKI de primera/segunda generación, para la mutación T790M en la progresión clínica mediante biopsia líquida o biopsias tumorales repetidas.
Se obtuvieron dos muestras de sangre en cada recolección, se efectuó la separación del plasma y se almacenaron a -80°C hasta la extracción del ADN. El ADN se extrajo del plasma usando el kit de preparación de muestras de ADNc cobas vers.2 (Roche Molecular Systems, Pleasanton, CA, EUA) y se recuperó en 200 μL de tampón de elución. La mitad del volumen se usó inmediatamente para la evaluación de la mutación EGFR mediante el ensayo v2 de prueba de mutación cobas EGFR de Roche. Las reacciones en cadena de la polimerasa (PCR) se realizaron en el analizador Roche cobas z480. Se utilizó un enfoque innovador de secuenciación masiva paralela (MPS) (SureSelect Cancer All-In-One; Agilent Technologies, Santa Clara, California, EUA) para optimizar el manejo del material biológico.
El equipo informó que el análisis de plasma mediante la prueba EGFR Cobas mostró en 57 (89%) casos una disminución sustancial en los niveles del alelo mutante de EGFR sensibilizante (sEGFRma), hasta un valor no detectable. Estos pacientes se definieron como buenos respondedores plasmáticos (PGR). En siete pacientes (11%), el sEGFRma no cayó a cero (respondedores plasmáticos malos, PPR). En estos últimos casos, el análisis de secuenciación paralela masiva (MPS) al final del primer mes y en la progresión clínica mostró la presencia de mutaciones inductoras resistentes, incluidas la amplificación de genes MET y HER2, mutaciones de los genes KRAS y PIK3CA. Los PPR mostraron progresión de la enfermedad en cinco (71%) casos, enfermedad estable en dos (29%) casos y una mediana de supervivencia libre de progresión (SLP) más corta (4,3 ± 1,1 meses) que la observada para los PGR (13,3 ± 1,2 meses).
Los autores concluyeron que sus resultados indican que un subconjunto de pacientes con CPCNM sometidos a un tratamiento de segunda línea con osimertinib son resistentes al tratamiento debido a la presencia de diferentes tipos de mutaciones. La monitorización plasmática mediante una prueba de mutación de EGFR basada en RT-PCR simple en el primer mes de tratamiento puede ser útil para identificar rápidamente estos casos y someterlos a análisis de MPS para una caracterización y tratamiento adicionales. El estudio fue publicado el 17 de marzo de 2020 en la revista Oncotarget.
Enlace relacionado:
Universidad de Chieti
Roche Molecular Systems
Agilent Technologies
Últimas Diagnóstico Molecular noticias
- Un análisis de orina predice el riesgo de dengue grave en una etapa temprana
- Prueba de sangre con marcado CE permite monitorizar la neuroinflamación en la esclerosis múltiple
- Prueba de VPH en el hogar con genotipificación extendida para el cribado del cáncer cervical
- Marcadores genéticos predicen respuesta y efectos secundarios de fármacos GLP-1 en la pérdida de peso
- Prueba de orina no invasiva predice recurrencia tras tratamiento con BCG en cáncer de vejiga
- Mesotelioma en adultos jóvenes vinculado a factores de riesgo genéticos
- Marcador genético predice insuficiencia cardíaca temprana en hipertensión arterial pulmonar
- Firmas inmunológicas en sangre ayudan a estimar el riesgo de cáncer en el síndrome de Lynch
- Análisis de sangre sencillo permite detectar múltiples enfermedades a partir de una sola muestra
- Prueba rápida de RT-PCR en el punto de atención diferencia influenza A/B y SARS-CoV-2 en minutos
- Prueba de ADNtc en sangre mejora la evaluación del cáncer de garganta relacionado con el VPH
- Análisis del ARN revela dianas terapéuticas en tumores sólidos
- Prueba identifica pacientes con cáncer de mama que podrían evitar la cirugía
- La secuenciación del genoma completo en la atención médica rutinaria amplía la detección de enfermedades raras
- Nueva herramienta de IA mejora la detección de causas genéticas en enfermedades raras
- Plataforma de PCR adaptativa mejora la consistencia en flujos de trabajo de NGS de lotes pequeños
Canales
Química Clínica
ver canal
Un estudio revela que la medición de ApoB es más eficaz que LDL para guiar la terapia lipídica
Los análisis de sangre rutinarios que miden las lipoproteínas de baja densidad (LDL), comúnmente conocidas como colesterol "malo", se utilizan ampliamente para orientar la terapia hipolipemiante, pero... Más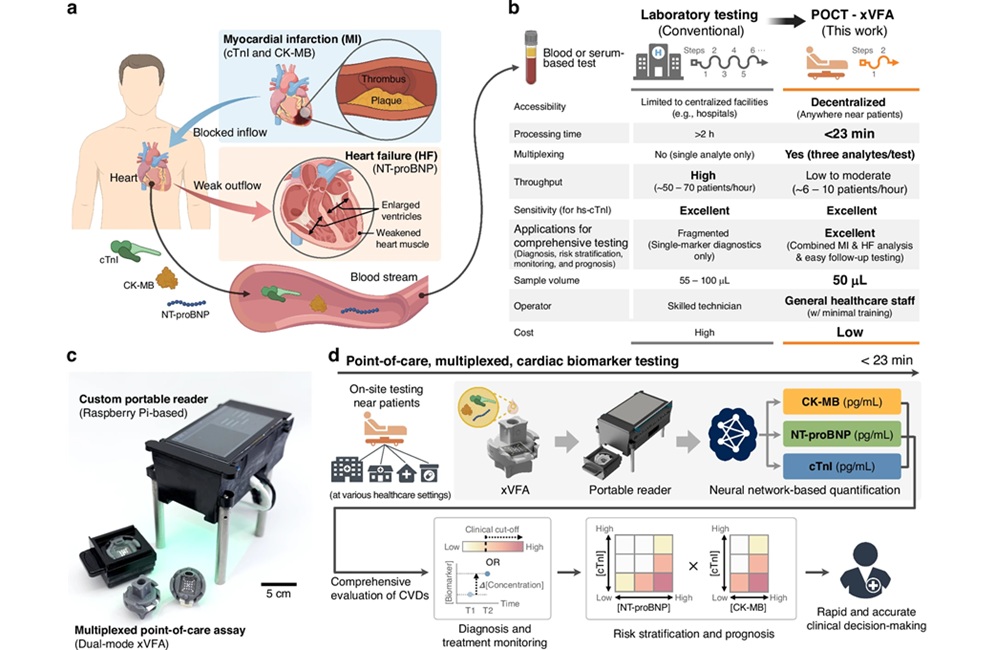
Prueba en el punto de atención basada en IA cuantifica múltiples biomarcadores cardíacos
Las enfermedades cardiovasculares son una de las principales causas de muerte, responsables de casi 20 millones de fallecimientos anuales. La detección temprana del infarto de miocardio y la insuficiencia... Más
Prueba de metabolitos en sangre detecta deterioro cognitivo temprano
La identificación temprana de personas con riesgo de demencia sigue siendo difícil, ya que los síntomas suelen aparecer solo después de una neurodegeneración significativa.... MásAnalizadores automatizados de nueva generación aumentan el rendimiento en química clínica y pruebas de electrolitos
Los laboratorios clínicos siguen enfrentándose a la escasez de personal, el espacio limitado y el creciente volumen de pruebas, lo que ejerce presión sobre los flujos de trabajo de... MásHematología
ver canal
Parámetros rutinarios de análisis de sangre vinculan la anemia con el riesgo de cáncer y la mortalidad
La anemia detectada en la atención médica rutinaria puede indicar una patología subyacente y es frecuente en adultos. Dado que se define por niveles de hemoglobina por debajo del rango... Más
Nuevo ensayo de función plaquetaria permite monitorizar la terapia antiplaquetaria
Para muchos laboratorios clínicos, el seguimiento de la respuesta a la terapia antiplaquetaria sigue siendo un reto. Los ensayos basados en la agregación plaquetaria y los sistemas de cartuchos... MásInmunología
ver canalMétodo de cribado combinado permite identificar casos de lepra en etapas tempranas
La lepra sigue siendo un problema importante de salud pública, con más de 200.000 casos nuevos notificados anualmente en todo el mundo, y la enfermedad temprana a menudo escapa a la detección... Más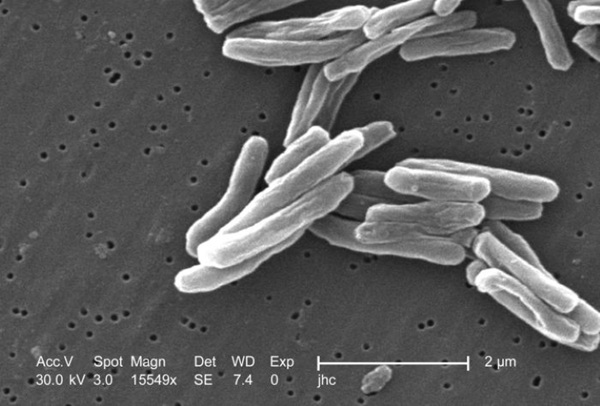
Prueba de anticuerpos en sangre identifica tuberculosis activa y distingue la infección latente
La tuberculosis activa (TB) sigue siendo una de las principales causas de muerte y enfermedad en todo el mundo; sin embargo, distinguir la enfermedad contagiosa de la infección latente continúa... MásMicrobiología
ver canal
Nuevo objetivo bacteriano identificado para la detección temprana del noma
La noma es una infección orofacial de rápida progresión que comienza como gingivitis y puede destruir los tejidos orales y faciales, afectando principalmente a niños pequeños... Más
Prueba rápida de orina acelera la selección de antibióticos para infecciones del tracto urinario
Las infecciones del tracto urinario son una causa frecuente de prescripción de antibióticos y han provocado más de 800.000 hospitalizaciones en Inglaterra en los últimos cinco... Más
El análisis genómico vincula cepas estreptocócicas emergentes con infecciones específicas
Las infecciones por Streptococcus dysgalactiae subespecie equisimilis (SDSE) están aumentando en todo el mundo e incluyen variantes que pueden provocar enfermedades graves. Investigadores informan... Más
La OMS respalda las pruebas rápidas en el punto de atención para mejorar la detección de tuberculosis
La tuberculosis (TB) sigue siendo una de las principales causas de muerte por enfermedades infecciosas, con más de 3.300 fallecimientos y 29.000 nuevos casos diarios. Los retrasos en el diagnóstico... MásPatología
ver canalLa IA ayuda a los clínicos con informes complejos de patología oncológica
Los equipos de oncología dependen cada vez más de informes de patología que integran histopatología, inmunohistoquímica y pruebas de biomarcadores en rápida e... Más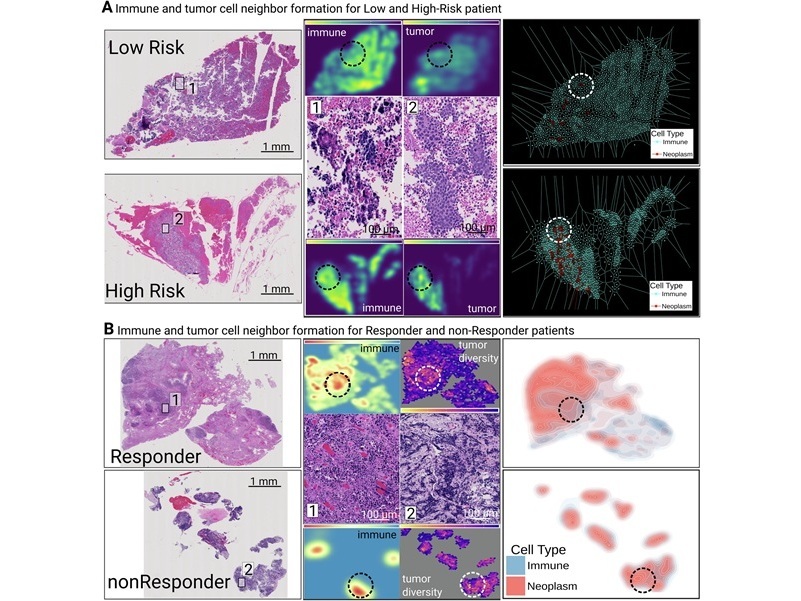
Herramienta de IA predice respuesta a la quimioterapia en cáncer de pulmón de células pequeñas
El cáncer de pulmón de células pequeñas suele presentarse en una etapa avanzada y progresa rápidamente, lo que deja poco tiempo para personalizar la terapia de primera línea. Actualmente, los médicos carecen... Más_image.png)
Biomarcador tumoral específico predice respuesta a inmunoterapia neoadyuvante en cáncer gástrico
El cáncer gástrico es la quinta neoplasia maligna más común y la cuarta causa principal de mortalidad por cáncer en todo el mundo, y China soporta casi la mitad de la carga global.... Más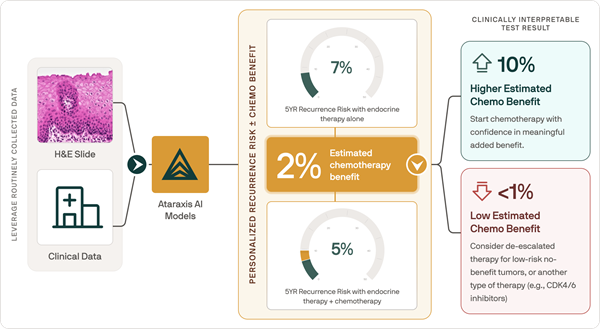
Nueva prueba de IA predice resultados de quimioterapia específicos para cada paciente con cáncer de mama
La selección de la quimioterapia adyuvante para el cáncer de mama en estadio temprano suele basarse en el riesgo de recurrencia y los promedios poblacionales, en lugar del beneficio individualizado... MásTecnología
ver canal
Prueba de esputo no invasiva detecta el cáncer de pulmón en etapa temprana
La detección precoz sigue siendo fundamental para mejorar los resultados en el cáncer de pulmón; sin embargo, los médicos se encuentran cada vez con mayor frecuencia con nódulos pulmonares indeterminados,... Más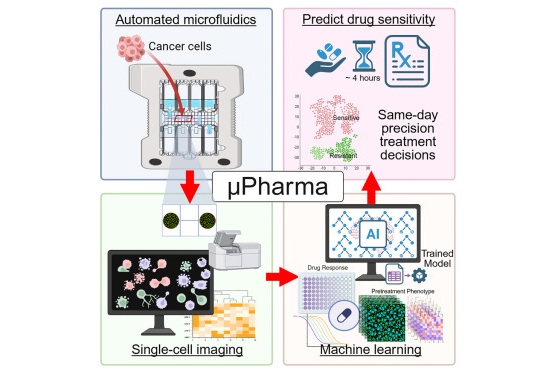
Nueva herramienta de IA permite seleccionar rápidamente el tratamiento en leucemia pediátrica
Los niños con leucemia linfoblástica aguda de células T se enfrentan a una enfermedad agresiva que sigue siendo difícil de tratar. Si bien las tasas de remisión han mejorado,... MásIndustria
ver canal
Takara Bio USA y Hamilton se asocian para automatizar la preparación de bibliotecas NGS
Takara Bio USA, Inc. (San José, California, EE. UU.), una filial de propiedad total de Takara Bio Inc., y Hamilton Company (Reno, Nevada, EE. UU.) anunciaron un acuerdo de desarrollo y comercia... Más