Bacterias como supermicrobios resistentes a los antibióticos
|
Por el equipo editorial de LabMedica en español Actualizado el 23 Apr 2015 |
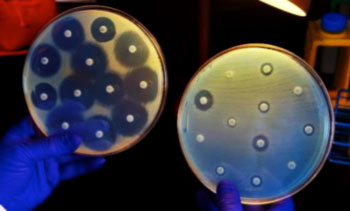
Imagen: La placa de la derecha fue inoculada con una Enterobacteria resistente al Carbapenem (CRE) que resultó ser resistente a todos los antibióticos ensayados; las bacterias en la placa izquierda son susceptibles a los antibióticos en los discos (Fotografía cortesía de James Gathany).
Las enterobacterias patógenas, incluyendo Escherichia coli y Klebsiella pneumoniae, son las principales causas de infecciones resistente a múltiples antibióticos (MDR) en los hospitales de todo el mundo y éstos patógenos han demostrado recientemente que han adquirido resistencia a los carbapenémicos.
Se han identificado dos genes que confieren resistencia contra una clase particularmente fuerte de antibióticos y que pueden ser compartidos fácilmente entre una familia de bacterias responsables de una parte importante de infecciones respiratorias y urinarias adquiridas en los hospitales.
Los científicos de la Facultad de Medicina de la Universidad de Washington (St. Louis, MO, EUA) recolectaron 450 aislados bacterianos, incluyendo 195 Enterobacterias en Pakistán, durante febrero de 2012 hasta marzo de 2013. Los investigadores seleccionaron al azar 55 aislados de Enterobacterias para hacerles la secuenciación de todo el genoma. Luego seleccionaron 23 aislamientos de muestras obtenidas de pacientes en los EUA entre enero de 2010 y junio de 2013, en el Hospital Judío Barnes (St. Louis, MO, EUA), que tenían una proporción similar de susceptibilidad y resistencia a los β-lactámicos a los recolectados en Pakistán para la secuenciación.
Los investigadores también secuenciaron una porción especial de material genético de las bacterias, llamados plásmidos. La mayor parte del ADN de una bacteria se encuentra en su cromosoma, pero las bacterias también tienen muchos pedazos adicionales, más pequeños y circulares de ADN conocidos como plásmidos que fácilmente pueden pasar de una cepa bacteriana a otra. Un plásmido es como un camión de reparto de genes bacterianos; es la forma principal como los genes de resistencia a los antibióticos se difunden entre las bacterias.
La variedad de cepas que descubrieron que codificaban la carbpenemasa de Klebsiella pneumoniae (KPC) y la metalo-β-Lacatamasa-1 de Nueva Delhi (NDM-1) fue consistente con la evidencia existente de que la transferencia horizontal de genes (HGT) es un factor importante en su propagación. Ellos identificaron algunos casos claves en los que el plásmido que llevaba NDM-1 o KPC eran casi idénticos, lo que significa que esto fácilmente podría facilitar la propagación de la resistencia a los antibióticos entre las bacterias que causan enfermedades que se encuentran en los EUA y en el sur de Asia.
Gautam Dantas, PhD, profesor asociado de patología e inmunología y autor principal del estudio, dijo: “Nuestros resultados también sugieren que va a ser más fácil para las cepas de estas bacterias, que aún no son resistentes, captar un gen que les permite sobrevivir el tratamiento con carbapenem. Los carbapenémicos son uno de nuestros últimos recursos para el tratamiento de infecciones bacterianas, los que utilizamos cuando nada más funciona. A medida que las formas resistentes a los medicamentos de Enterobacterias se vuelvan más generalizadas, las probabilidades aumentarán de transmitir una de estas súperbacterias a un amigo con un sistema inmunológico debilitado que realmente puede ser afectado por ellas”. El estudio fue publicado en línea en marzo de 2015 para la edición de junio de 2015 de la revista Emerging Infectious Diseases.
Enlaces relacionados:
Escuela de Medicina de la Universidad Washington
Hospital Barnes Jewish
Se han identificado dos genes que confieren resistencia contra una clase particularmente fuerte de antibióticos y que pueden ser compartidos fácilmente entre una familia de bacterias responsables de una parte importante de infecciones respiratorias y urinarias adquiridas en los hospitales.
Los científicos de la Facultad de Medicina de la Universidad de Washington (St. Louis, MO, EUA) recolectaron 450 aislados bacterianos, incluyendo 195 Enterobacterias en Pakistán, durante febrero de 2012 hasta marzo de 2013. Los investigadores seleccionaron al azar 55 aislados de Enterobacterias para hacerles la secuenciación de todo el genoma. Luego seleccionaron 23 aislamientos de muestras obtenidas de pacientes en los EUA entre enero de 2010 y junio de 2013, en el Hospital Judío Barnes (St. Louis, MO, EUA), que tenían una proporción similar de susceptibilidad y resistencia a los β-lactámicos a los recolectados en Pakistán para la secuenciación.
Los investigadores también secuenciaron una porción especial de material genético de las bacterias, llamados plásmidos. La mayor parte del ADN de una bacteria se encuentra en su cromosoma, pero las bacterias también tienen muchos pedazos adicionales, más pequeños y circulares de ADN conocidos como plásmidos que fácilmente pueden pasar de una cepa bacteriana a otra. Un plásmido es como un camión de reparto de genes bacterianos; es la forma principal como los genes de resistencia a los antibióticos se difunden entre las bacterias.
La variedad de cepas que descubrieron que codificaban la carbpenemasa de Klebsiella pneumoniae (KPC) y la metalo-β-Lacatamasa-1 de Nueva Delhi (NDM-1) fue consistente con la evidencia existente de que la transferencia horizontal de genes (HGT) es un factor importante en su propagación. Ellos identificaron algunos casos claves en los que el plásmido que llevaba NDM-1 o KPC eran casi idénticos, lo que significa que esto fácilmente podría facilitar la propagación de la resistencia a los antibióticos entre las bacterias que causan enfermedades que se encuentran en los EUA y en el sur de Asia.
Gautam Dantas, PhD, profesor asociado de patología e inmunología y autor principal del estudio, dijo: “Nuestros resultados también sugieren que va a ser más fácil para las cepas de estas bacterias, que aún no son resistentes, captar un gen que les permite sobrevivir el tratamiento con carbapenem. Los carbapenémicos son uno de nuestros últimos recursos para el tratamiento de infecciones bacterianas, los que utilizamos cuando nada más funciona. A medida que las formas resistentes a los medicamentos de Enterobacterias se vuelvan más generalizadas, las probabilidades aumentarán de transmitir una de estas súperbacterias a un amigo con un sistema inmunológico debilitado que realmente puede ser afectado por ellas”. El estudio fue publicado en línea en marzo de 2015 para la edición de junio de 2015 de la revista Emerging Infectious Diseases.
Enlaces relacionados:
Escuela de Medicina de la Universidad Washington
Hospital Barnes Jewish
Últimas Microbiología noticias
- OMS recomienda pruebas POC, hisopos de lengua y agrupamiento de esputo para diagnóstico de TB
- Nuevo método de imágenes podría ayudar a predecir infecciones intestinales peligrosas
- La secuenciación rápida podría transformar la atención de la tuberculosis
- Virus intestinales ocultos vinculados al riesgo de cáncer colorrectal
- Panel de tres pruebas para detección de infecciones por duelas del hígado
- Prueba rápida promete respuestas inmediatas a infecciones resistentes a medicamentos
- Tecnología con CRISPR neutraliza bacterias resistentes a antibióticos
- Nuevo estudio identifica características del microbioma intestinal asociadas con enfermedad de Alzheimer
- Plataforma de IA permite detección rápida de patógenos de C. auris resistentes a fármacos
- Nueva prueba mide eficacia de antibióticos para eliminar bacterias
- Nuevas normas para antimicrobianos atienden tuberculosis para optimizar diagnóstico
- Método de diagnóstico de ITU ofrece resultados de resistencia a antibióticos 24 horas antes
- Avances en análisis microbiano mejora predicción de enfermedades
- Método de diagnóstico en sangre identifica infecciones IVRI pediátricas
- Prueba de diagnóstico rápido es estándar de oro para detección de sepsis
- Prueba rápida de tuberculosis POC proporciona resultados en 15 minutos
Canales
Química Clínica
ver canal
Análisis de sangre con IA permite detectar eventos cardíacos mortales
Dos emergencias cardiovasculares potencialmente mortales —el infarto de miocardio y la disección aórtica— suelen presentar el mismo síntoma: dolor torácico repentino... Más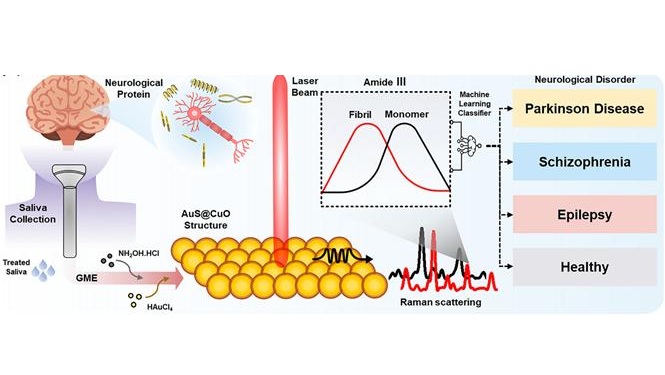
Un sensor de IA detecta trastornos neurológicos con una sola gota de saliva
Trastornos neurológicos como el Parkinson y el Alzheimer suelen desarrollarse gradualmente y presentar síntomas sutiles en sus primeras etapas. Dado que los signos tempranos suelen ser vagos... MásDiagnóstico Molecular
ver canal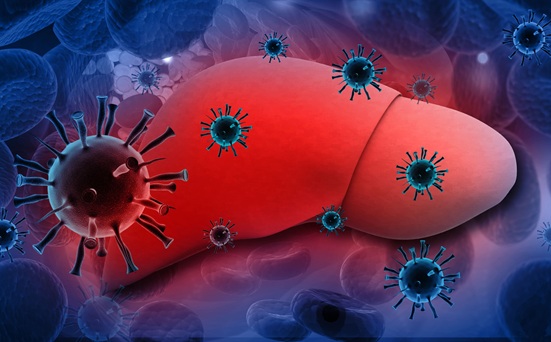
Nuevos biomarcadores indican mayor riesgo de cáncer de hígado en pacientes con hepatitis B crónica
La hepatitis B crónica afecta a unos 296 millones de personas en todo el mundo y es una de las principales causas de cirrosis hepática y cáncer de hígado. Si bien los tratamientos... Más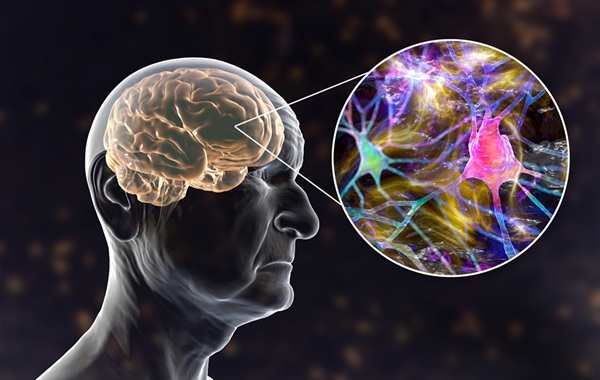
Biomarcador sanguíneo de Alzheimer mejora detección de enfermedades cardíacas y renales
Una proteína en sangre ampliamente utilizada como indicador temprano de la enfermedad de Alzheimer podría no ser tan específica como se pensaba. Investigadores han descubierto ahora que la tau fosforilada... MásHematología
ver canal
Prueba rápida en cartuchos busca ampliar acceso al diagnóstico de trastornos de hemoglobina
La anemia de células falciformes y la beta talasemia son trastornos de la hemoglobina que a menudo requieren la derivación a laboratorios especializados para un diagnóstico definitivo,... Más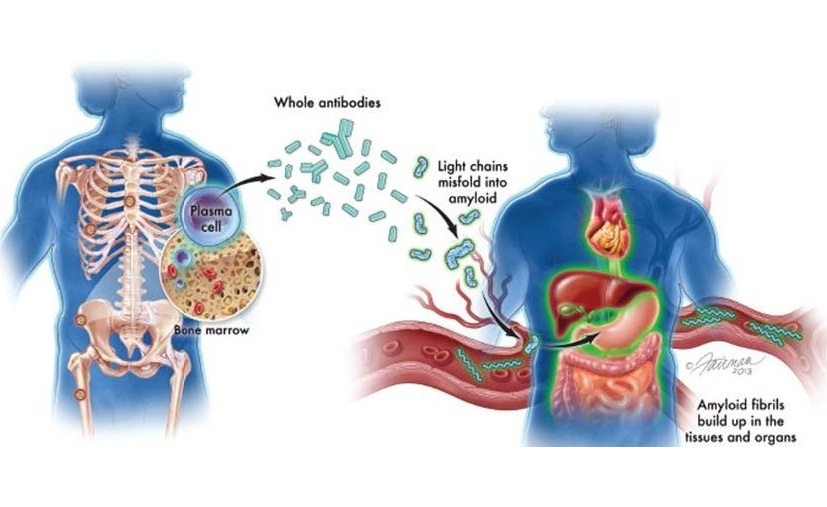
Nuevas directrices buscan mejorar diagnóstico de amiloidosis AL
La amiloidosis de cadenas ligeras (AL) es un trastorno poco común y potencialmente mortal de la médula ósea, en el que las proteínas amiloides anormales se acumulan en los órganos. Aproximadamente 3.... MásInmunología
ver canal
Firmas de mutación del cáncer mejoran la predicción de la respuesta a inmunoterapia
Las células cancerosas acumulan miles de mutaciones genéticas, pero no todas afectan a los tumores de la misma manera. Algunas hacen que las células cancerosas sean más visibles... Más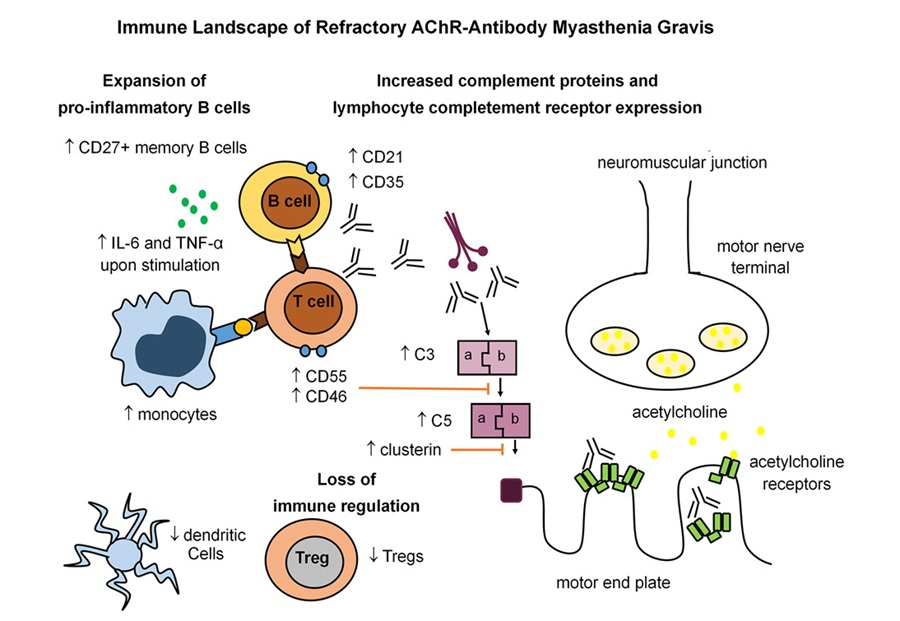
Firma inmunitaria identificada en miastenia gravis resistente al tratamiento
La miastenia gravis es un trastorno autoinmune poco común en el que el ataque inmunitario a la unión neuromuscular causa debilidad fluctuante que puede afectar la visión, el movimiento,... MásPatología
ver canal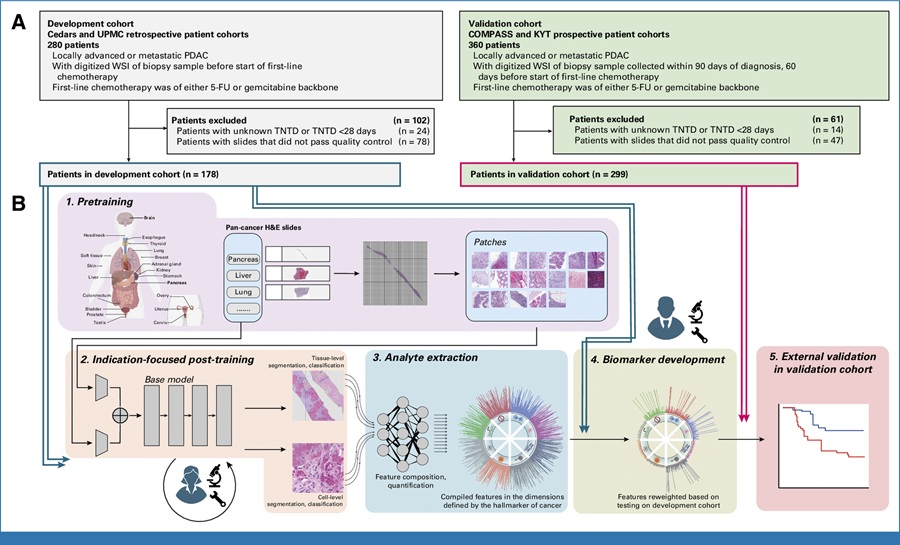
Herramienta de IA predice la respuesta a la quimioterapia a partir de portaobjetos de biopsia
La selección de la quimioterapia de primera línea para el cáncer de páncreas avanzado generalmente implica probar uno de dos regímenes aprobados y cambiarlo si la respuesta... Más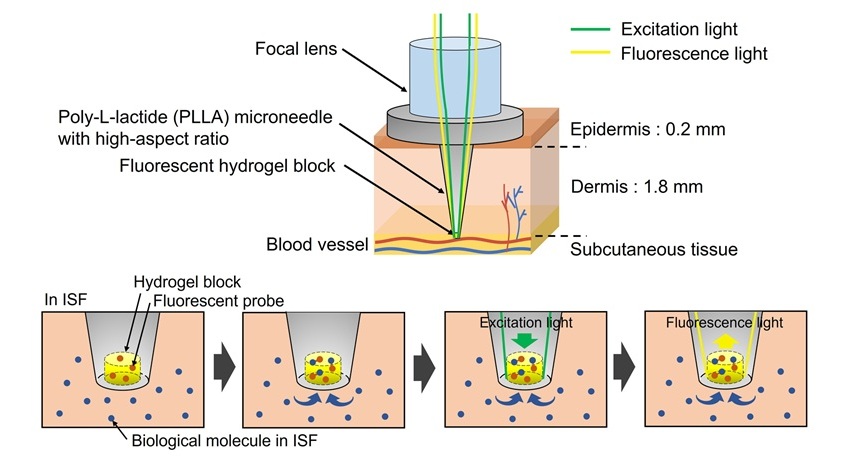
Primer dispositivo óptico con microagujas del mundo permite pruebas clínicas sin extracción de sangre
La extracción de sangre es uno de los procedimientos clínicos más comunes, pero puede resultar difícil o incómoda para muchos pacientes, especialmente para los adultos... MásTecnología
ver canal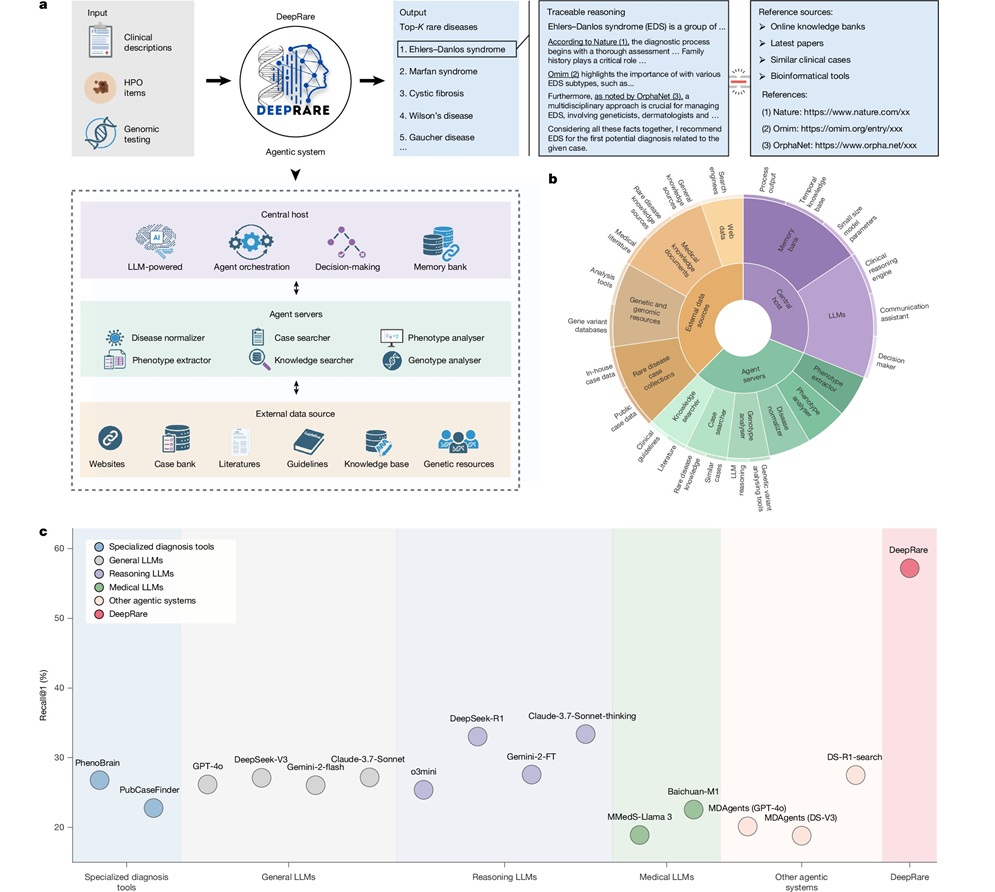
Modelo de IA supera a clínicos en la detección de enfermedades raras
Se estima que las enfermedades raras afectan a 300 millones de personas en todo el mundo; sin embargo, el diagnóstico suele ser largo y propenso a errores. Muchas de estas afecciones presentan signos... Más
Diagnóstico por IA demuestra alta precisión en detección de infecciones articulares periprotésicas
La infección articular periprotésica (IAP) es una complicación poco frecuente pero grave que afecta entre el 1 % y el 2 % de las cirugías primarias de reemplazo articular.... MásIndustria
ver canal
Agilent Technologies adquiere la empresa de diagnóstico patológico Biocare Medical
Agilent Technologies (Santa Clara, California, EE. UU.) ha firmado un acuerdo definitivo para adquirir Biocare Medical (Pacheco, California, EE. UU.), ampliando así su cartera de productos de p... Más