Asocian a la lectina unida a la manosa con la coagulopatía en la COVID-19 severa
|
Por el equipo editorial de LabMedica en español Actualizado el 22 Sep 2020 |
La pandemia de COVID-19 en curso ha causado una morbilidad y mortalidad significativas en todo el mundo, así como efectos profundos en la sociedad. Los pacientes con COVID-19 tienen un mayor riesgo de complicaciones tromboembólicas (TE), que se desarrollan a pesar de la tromboprofilaxis farmacológica.
El mecanismo detrás de la coagulopatía asociada a la COVID-19 sigue sin estar claro. Se ha sugerido que la lectina unida a la manosa (MBL), una molécula de reconocimiento de patrones que inicia la vía de la lectina de activación del complemento es un potencial amplificador de la coagulación sanguínea durante la tromboinflamación.
Los inmunólogos de la Universidad de Uppsala (Uppsala, Suecia) y sus colegas, aclararon el papel de la MBL en la COVID-19 y midieron los niveles plasmáticos de MBL y la actividad en una cohorte de 65 pacientes con COVID-19 en estado crítico e investigaron su relación con el resultado clínico. Todos los pacientes eran mayores de 18 años, que tenían COVID-19 confirmada o sospechada, ingresados en la UCI, entre el 13 de marzo y el 30 de abril de 2020, fueron evaluados para su inclusión.
Se tomaron muestras de sangre en tubos de ácido etilendiaminotetraacético y se almacenó el plasma a –70°C hasta el momento del análisis. Los niveles plasmáticos de MBL en el día 1 en la UCI (en promedio día 10 de la COVID-19) se midieron mediante un ensayo inmunoabsorbente ligado a enzimas (ELISA) interno y fueron significativamente más altos que en los controles sanos. La actividad de la ruta de MBL se evaluó mediante un ELISA funcional utilizando manano como activador y la capacidad de unión de MBL y la deposición de C3 del complemento como lecturas. Este ensayo mide la concentración funcional de MBL en plasma y su capacidad para activar el complemento y confirmó la actividad elevada de MBL y la deposición de C3 dependiente de MBL en el grupo de pacientes.
El equipo informó que nueve (14%) pacientes que desarrollaron tromboembolismo sintomático, a pesar de recibir tromboprofilaxis, tenían niveles de MBL significativamente más altos que los pacientes que no experimentaron un evento tromboembólico (mediana de 1233 kU/L versus 470 kU/L). Todos los pacientes del estudio recibieron tromboprofilaxis con dalteparina sódica (n = 64) o apixaban (n = 1). De los nueve pacientes del estudio que desarrollaron un evento tromboembólico sintomático durante su estancia en la UCI, dos fueron trombosis arteriales (apoplejía o infarto de miocardio) y siete fueron embolias pulmonares (EP). Los pacientes con COVID-19 tienen niveles elevados de MBL en plasma en comparación con los controles sanos: 625 kU/L en el grupo de pacientes (n = 65) versus 444 kU/L en los controles de donantes de sangre sanos (n = 72).
Curiosamente, los pacientes que desarrollaron EP tenían niveles de MBL por encima del percentil 95 en comparación con los controles. MBL mostró una correlación significativa con los niveles de factor C3 del complemento total, pero no con el producto de activación C3d (medido como relación C3d/C3), una medida de la actividad de la vía alternativa del complemento, ni con C1q, el iniciador de la vía clásica. Los niveles totales de C3, la relación C3d/C3 o C1q no se relacionaron con eventos trombóticos, lo que indica una asociación específica entre la MBL y la trombosis.
Los autores concluyeron que habían identificado la activación del complemento a través de la vía MBL como un mecanismo de amplificación novedoso que contribuye a la trombosis patológica en pacientes con COVID-19, críticamente enfermos. El direccionamiento farmacológico de la vía MBL podría ser una nueva opción de tratamiento para la trombosis en la COVID-19. Las pruebas de laboratorio de los niveles de MBL podrían ser valiosas para identificar a los pacientes con COVID-19 en riesgo de eventos tromboembólicos. El estudio fue publicado el 1 de septiembre de 2020 en la revista Thrombosis and Haemostasis.
Enlace relacionado:
Universidad de Uppsala
El mecanismo detrás de la coagulopatía asociada a la COVID-19 sigue sin estar claro. Se ha sugerido que la lectina unida a la manosa (MBL), una molécula de reconocimiento de patrones que inicia la vía de la lectina de activación del complemento es un potencial amplificador de la coagulación sanguínea durante la tromboinflamación.
Los inmunólogos de la Universidad de Uppsala (Uppsala, Suecia) y sus colegas, aclararon el papel de la MBL en la COVID-19 y midieron los niveles plasmáticos de MBL y la actividad en una cohorte de 65 pacientes con COVID-19 en estado crítico e investigaron su relación con el resultado clínico. Todos los pacientes eran mayores de 18 años, que tenían COVID-19 confirmada o sospechada, ingresados en la UCI, entre el 13 de marzo y el 30 de abril de 2020, fueron evaluados para su inclusión.
Se tomaron muestras de sangre en tubos de ácido etilendiaminotetraacético y se almacenó el plasma a –70°C hasta el momento del análisis. Los niveles plasmáticos de MBL en el día 1 en la UCI (en promedio día 10 de la COVID-19) se midieron mediante un ensayo inmunoabsorbente ligado a enzimas (ELISA) interno y fueron significativamente más altos que en los controles sanos. La actividad de la ruta de MBL se evaluó mediante un ELISA funcional utilizando manano como activador y la capacidad de unión de MBL y la deposición de C3 del complemento como lecturas. Este ensayo mide la concentración funcional de MBL en plasma y su capacidad para activar el complemento y confirmó la actividad elevada de MBL y la deposición de C3 dependiente de MBL en el grupo de pacientes.
El equipo informó que nueve (14%) pacientes que desarrollaron tromboembolismo sintomático, a pesar de recibir tromboprofilaxis, tenían niveles de MBL significativamente más altos que los pacientes que no experimentaron un evento tromboembólico (mediana de 1233 kU/L versus 470 kU/L). Todos los pacientes del estudio recibieron tromboprofilaxis con dalteparina sódica (n = 64) o apixaban (n = 1). De los nueve pacientes del estudio que desarrollaron un evento tromboembólico sintomático durante su estancia en la UCI, dos fueron trombosis arteriales (apoplejía o infarto de miocardio) y siete fueron embolias pulmonares (EP). Los pacientes con COVID-19 tienen niveles elevados de MBL en plasma en comparación con los controles sanos: 625 kU/L en el grupo de pacientes (n = 65) versus 444 kU/L en los controles de donantes de sangre sanos (n = 72).
Curiosamente, los pacientes que desarrollaron EP tenían niveles de MBL por encima del percentil 95 en comparación con los controles. MBL mostró una correlación significativa con los niveles de factor C3 del complemento total, pero no con el producto de activación C3d (medido como relación C3d/C3), una medida de la actividad de la vía alternativa del complemento, ni con C1q, el iniciador de la vía clásica. Los niveles totales de C3, la relación C3d/C3 o C1q no se relacionaron con eventos trombóticos, lo que indica una asociación específica entre la MBL y la trombosis.
Los autores concluyeron que habían identificado la activación del complemento a través de la vía MBL como un mecanismo de amplificación novedoso que contribuye a la trombosis patológica en pacientes con COVID-19, críticamente enfermos. El direccionamiento farmacológico de la vía MBL podría ser una nueva opción de tratamiento para la trombosis en la COVID-19. Las pruebas de laboratorio de los niveles de MBL podrían ser valiosas para identificar a los pacientes con COVID-19 en riesgo de eventos tromboembólicos. El estudio fue publicado el 1 de septiembre de 2020 en la revista Thrombosis and Haemostasis.
Enlace relacionado:
Universidad de Uppsala
Últimas Inmunología noticias
- Método de cribado combinado permite identificar casos de lepra en etapas tempranas
- Prueba de anticuerpos en sangre identifica tuberculosis activa y distingue la infección latente
- Identifican una vía inflamatoria que impulsa la resistencia a la inmunoterapia en el cáncer de vejiga
- Chip microfluídico detecta la recurrencia del cáncer a partir de señales de respuesta inmunitaria
- Firmas de mutación del cáncer mejoran la predicción de la respuesta a inmunoterapia
- Firma inmunitaria identificada en miastenia gravis resistente al tratamiento
- Nuevo biomarcador predice respuesta a quimioterapia en cáncer de mama triple negativo
- Análisis de sangre identifica pacientes con cáncer pulmonar beneficiarios de fármaco de inmunoterapia
- Enfoque de secuenciación genómica completa identifica pacientes con cáncer beneficiarios con inhibidores de PARP
- Biopsia líquida ultrasensible demuestra eficacia para predecir respuesta a inmunoterapia
- Análisis sanguíneo identifica pacientes con cáncer de colon que se benefician de AINE
- Análisis sanguíneo podría detectar efectos adversos de inmunoterapia
- Análisis de sangre rutinario puede predecir mayor beneficiario de terapia con células T CAR
- Nueva prueba distingue falsos positivos inducidos por vacuna de infección activa por VIH
- Prueba de firma genética predice respuesta a tratamientos clave para cáncer de mama
- Chip captura células cancerosas de sangre para seleccionar tratamiento adecuado para cáncer de mama
Canales
Química Clínica
ver canal
Prueba de metabolitos en sangre detecta deterioro cognitivo temprano
La identificación temprana de personas con riesgo de demencia sigue siendo difícil, ya que los síntomas suelen aparecer solo después de una neurodegeneración significativa.... MásAnalizadores automatizados de nueva generación aumentan el rendimiento en química clínica y pruebas de electrolitos
Los laboratorios clínicos siguen enfrentándose a la escasez de personal, el espacio limitado y el creciente volumen de pruebas, lo que ejerce presión sobre los flujos de trabajo de... Más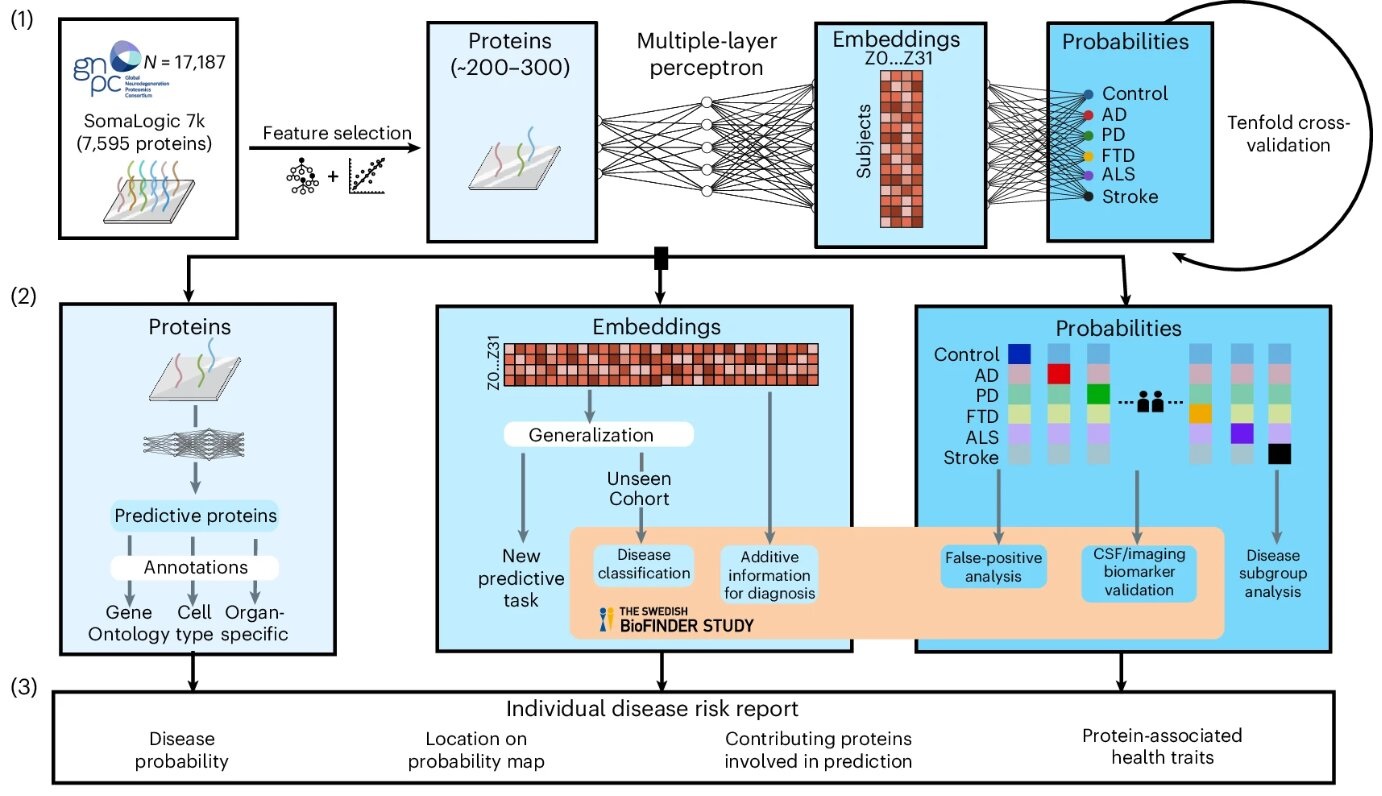
Análisis de sangre basado en IA detecta múltiples trastornos cerebrales a partir de una sola muestra
Diagnosticar la causa de los síntomas cognitivos relacionados con la edad sigue siendo un desafío, ya que las manifestaciones clínicas de las enfermedades neurodegenerativas a menudo se superponen y pueden... MásDiagnóstico Molecular
ver canal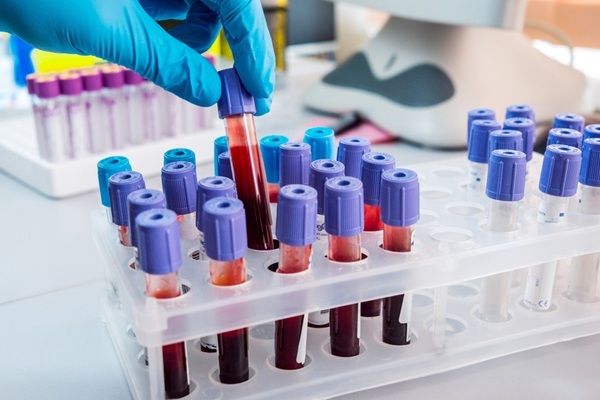
Análisis de sangre sencillo permite detectar múltiples enfermedades a partir de una sola muestra
La detección precoz y precisa del cáncer y las enfermedades orgánicas sigue viéndose limitada por el coste, la dependencia de ensayos de mutación específicos y... Más
Prueba rápida de RT-PCR en el punto de atención diferencia influenza A/B y SARS-CoV-2 en minutos
Los virus respiratorios como la influenza A/B y el SARS-CoV-2 siguen representando una carga para los servicios de urgencias y emergencias, donde una diferenciación rápida y fiable es fundamental... MásHematología
ver canal
Plataforma abierta de multiómica identifica subtipos pronósticos en cánceres hematológicos
Los cánceres hematológicos abarcan diversas entidades cuya biología y comportamiento clínico se comprenden mejor mediante análisis integradores en grandes cohortes.... Más
Prueba rápida en cartuchos busca ampliar acceso al diagnóstico de trastornos de hemoglobina
La anemia de células falciformes y la beta talasemia son trastornos de la hemoglobina que a menudo requieren la derivación a laboratorios especializados para un diagnóstico definitivo,... MásMicrobiología
ver canal
Nuevo objetivo bacteriano identificado para la detección temprana del noma
La noma es una infección orofacial de rápida progresión que comienza como gingivitis y puede destruir los tejidos orales y faciales, afectando principalmente a niños pequeños... Más
Prueba rápida de orina acelera la selección de antibióticos para infecciones del tracto urinario
Las infecciones del tracto urinario son una causa frecuente de prescripción de antibióticos y han provocado más de 800.000 hospitalizaciones en Inglaterra en los últimos cinco... Más
El análisis genómico vincula cepas estreptocócicas emergentes con infecciones específicas
Las infecciones por Streptococcus dysgalactiae subespecie equisimilis (SDSE) están aumentando en todo el mundo e incluyen variantes que pueden provocar enfermedades graves. Investigadores informan... Más
La OMS respalda las pruebas rápidas en el punto de atención para mejorar la detección de tuberculosis
La tuberculosis (TB) sigue siendo una de las principales causas de muerte por enfermedades infecciosas, con más de 3.300 fallecimientos y 29.000 nuevos casos diarios. Los retrasos en el diagnóstico... MásPatología
ver canal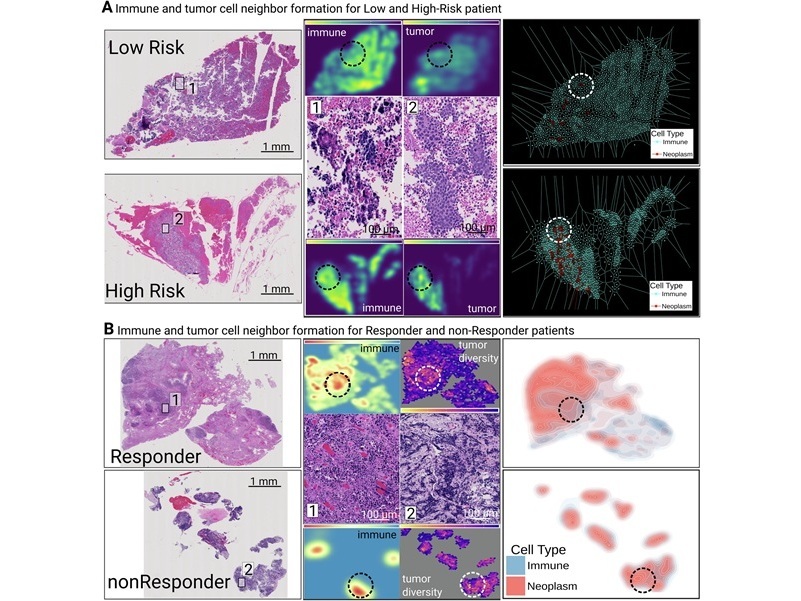
Herramienta de IA predice respuesta a la quimioterapia en cáncer de pulmón de células pequeñas
El cáncer de pulmón de células pequeñas suele presentarse en una etapa avanzada y progresa rápidamente, lo que deja poco tiempo para personalizar la terapia de primera línea. Actualmente, los médicos carecen... Más_image.png)
Biomarcador tumoral específico predice respuesta a inmunoterapia neoadyuvante en cáncer gástrico
El cáncer gástrico es la quinta neoplasia maligna más común y la cuarta causa principal de mortalidad por cáncer en todo el mundo, y China soporta casi la mitad de la carga global.... Más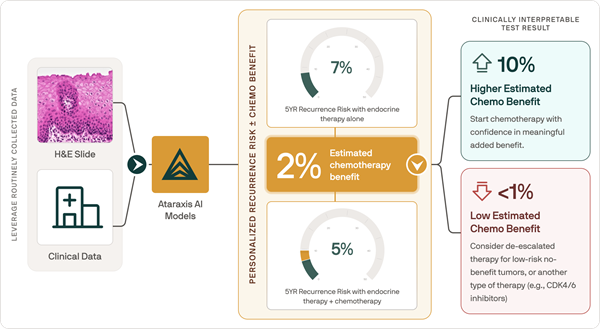
Nueva prueba de IA predice resultados de quimioterapia específicos para cada paciente con cáncer de mama
La selección de la quimioterapia adyuvante para el cáncer de mama en estadio temprano suele basarse en el riesgo de recurrencia y los promedios poblacionales, en lugar del beneficio individualizado... MásTecnología
ver canal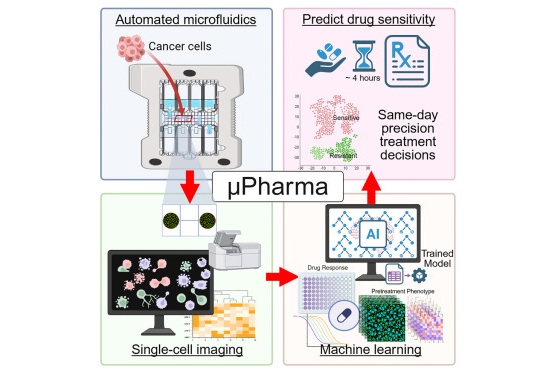
Nueva herramienta de IA permite seleccionar rápidamente el tratamiento en leucemia pediátrica
Los niños con leucemia linfoblástica aguda de células T se enfrentan a una enfermedad agresiva que sigue siendo difícil de tratar. Si bien las tasas de remisión han mejorado,... Más
Diseño innovador de espectrometría de masas podría permitir la detección de abundancias ultrabajas
La espectrometría de masas es fundamental para identificar y cuantificar moléculas en muestras biológicas complejas, pero los instrumentos convencionales suelen analizar los iones... MásIndustria
ver canal
Takara Bio USA y Hamilton se asocian para automatizar la preparación de bibliotecas NGS
Takara Bio USA, Inc. (San José, California, EE. UU.), una filial de propiedad total de Takara Bio Inc., y Hamilton Company (Reno, Nevada, EE. UU.) anunciaron un acuerdo de desarrollo y comercia... Más