Pfizer y BioNTech presentan a la FDA una solicitud de autorización de uso de emergencia para una vacuna contra COVID-19
|
Por el equipo editorial de LabMedica en español Actualizado el 25 Nov 2020 |

Ilustración
Pfizer Inc. (Nueva York, NY, EUA) y Biopharmaceutical New Technologies (BioNTech Maguncia, Alemania) presentaron a la Dirección de Medicamentos y Alimentos de EUA (FDA) una solicitud para la Autorización para Uso en Emergencias (AUE) de su prospecto de vacuna de ARNm contra el SARS-CoV-2, BNT162b2.
Esto podría permitir el uso de dicha vacuna en poblaciones de alto riesgo de los EUA, hacia mediados o finales de diciembre de 2020. La solicitud se basa en que se demostró una tasa de eficacia de la vacuna del 95% en el estudio clínico de fase 3 de esas empresas, en participantes sin infección por SARS-CoV-2 (primer objetivo primario) y también en participantes con y sin infección previa por SARS-CoV-2 (segundo objetivo primario), medidas en cada grupo siete días después de la segunda dosis. El análisis del primer objetivo principal se basó en 170 casos confirmados de COVID-19. Dicha solicitud también está respaldada por datos de seguridad solicitados de un subconjunto aleatorizado de aproximadamente 8.000 participantes mayores de 18 años y datos de seguridad no solicitados de aproximadamente 38.000 participantes del estudio a quienes se les ha hecho seguimiento durante una mediana de dos meses después de la segunda dosis del prospecto de vacuna. La solicitud también incluye datos de seguridad solicitados de cerca de 100 niños de 12 a 15 años. Hasta la fecha, el Comité de Monitoreo de Datos (DMC) del estudio no ha reportado ningún problema de seguridad serio relacionado con la vacuna.
Las empresas ya han iniciado solicitudes continuas ante varias agencias reguladoras de todo el mundo, como la EMA y la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) del Reino Unido, y tienen la intención de enviar solicitudes a otras agencias reguladoras en todo el mundo en los próximos días. En algunos casos, los gobiernos pueden tener recursos regulatorios similares a una AUE. Las empresas estarán listas para distribuir su prospecto de vacuna pocas horas después de ser autorizadas. La red de fabricación combinada de Pfizer y BioNTech tiene el potencial de suministrar hasta 50 millones de dosis de vacunas a nivel mundial en 2020 y hasta 1.300 millones de dosis para fines de 2021 (dependiendo del éxito clínico, la capacidad de fabricación y la aprobación o autorización regulatoria).
“Nuestro trabajo para ofrecer una vacuna segura y eficaz nunca ha sido más urgente, ya que seguimos viendo un aumento alarmante en el número de casos de COVID-19 a nivel mundial. La solicitud en los EUA representa un hito crítico en nuestro viaje para entregarle al mundo una vacuna contra la COVID-19 y ahora tenemos una imagen más completa de la eficacia y del perfil de seguridad de nuestra vacuna, lo cual nos da confianza en su potencial”, dijo el Dr. Albert Bourla, presidente y director ejecutivo de Pfizer. "Esperamos con interés la próxima discusión del Comité Asesor de Vacunas y Productos Biológicos Relacionados y continuamos nuestro trabajo en estrecha colaboración con la FDA y las autoridades reguladoras de todo el mundo para asegurar la autorización de nuestro prospecto de vacuna, lo más pronto posible".
“Solicitar una Autorización para Uso en Emergencias en los EUA, es un paso fundamental para que nuestro prospecto de vacuna esté disponible para la población mundial lo más pronto posible”, dijo Ugur Sahin, M.D., director ejecutivo y cofundador de BioNTech. “Tenemos la intención de continuar trabajando con las agencias reguladoras en todo el mundo para obtener la distribución rápida de nuestra vacuna a nivel mundial. Como empresa ubicada en Alemania, en el corazón de Europa, nuestras interacciones con la Agencia Europea de Medicamentos (EMA) son de particular importancia para nosotros y les hemos proporcionado datos continuamente como parte de nuestro proceso de revisión continua".
Enlace relacionado:
Biopharmaceutical New Technologies
Esto podría permitir el uso de dicha vacuna en poblaciones de alto riesgo de los EUA, hacia mediados o finales de diciembre de 2020. La solicitud se basa en que se demostró una tasa de eficacia de la vacuna del 95% en el estudio clínico de fase 3 de esas empresas, en participantes sin infección por SARS-CoV-2 (primer objetivo primario) y también en participantes con y sin infección previa por SARS-CoV-2 (segundo objetivo primario), medidas en cada grupo siete días después de la segunda dosis. El análisis del primer objetivo principal se basó en 170 casos confirmados de COVID-19. Dicha solicitud también está respaldada por datos de seguridad solicitados de un subconjunto aleatorizado de aproximadamente 8.000 participantes mayores de 18 años y datos de seguridad no solicitados de aproximadamente 38.000 participantes del estudio a quienes se les ha hecho seguimiento durante una mediana de dos meses después de la segunda dosis del prospecto de vacuna. La solicitud también incluye datos de seguridad solicitados de cerca de 100 niños de 12 a 15 años. Hasta la fecha, el Comité de Monitoreo de Datos (DMC) del estudio no ha reportado ningún problema de seguridad serio relacionado con la vacuna.
Las empresas ya han iniciado solicitudes continuas ante varias agencias reguladoras de todo el mundo, como la EMA y la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) del Reino Unido, y tienen la intención de enviar solicitudes a otras agencias reguladoras en todo el mundo en los próximos días. En algunos casos, los gobiernos pueden tener recursos regulatorios similares a una AUE. Las empresas estarán listas para distribuir su prospecto de vacuna pocas horas después de ser autorizadas. La red de fabricación combinada de Pfizer y BioNTech tiene el potencial de suministrar hasta 50 millones de dosis de vacunas a nivel mundial en 2020 y hasta 1.300 millones de dosis para fines de 2021 (dependiendo del éxito clínico, la capacidad de fabricación y la aprobación o autorización regulatoria).
“Nuestro trabajo para ofrecer una vacuna segura y eficaz nunca ha sido más urgente, ya que seguimos viendo un aumento alarmante en el número de casos de COVID-19 a nivel mundial. La solicitud en los EUA representa un hito crítico en nuestro viaje para entregarle al mundo una vacuna contra la COVID-19 y ahora tenemos una imagen más completa de la eficacia y del perfil de seguridad de nuestra vacuna, lo cual nos da confianza en su potencial”, dijo el Dr. Albert Bourla, presidente y director ejecutivo de Pfizer. "Esperamos con interés la próxima discusión del Comité Asesor de Vacunas y Productos Biológicos Relacionados y continuamos nuestro trabajo en estrecha colaboración con la FDA y las autoridades reguladoras de todo el mundo para asegurar la autorización de nuestro prospecto de vacuna, lo más pronto posible".
“Solicitar una Autorización para Uso en Emergencias en los EUA, es un paso fundamental para que nuestro prospecto de vacuna esté disponible para la población mundial lo más pronto posible”, dijo Ugur Sahin, M.D., director ejecutivo y cofundador de BioNTech. “Tenemos la intención de continuar trabajando con las agencias reguladoras en todo el mundo para obtener la distribución rápida de nuestra vacuna a nivel mundial. Como empresa ubicada en Alemania, en el corazón de Europa, nuestras interacciones con la Agencia Europea de Medicamentos (EMA) son de particular importancia para nosotros y les hemos proporcionado datos continuamente como parte de nuestro proceso de revisión continua".
Enlace relacionado:
Biopharmaceutical New Technologies
Últimas COVID-19 noticias
- Inmunosensor nuevo allana el camino para pruebas rápidas POC para COVID-19 y enfermedades infecciosas emergentes
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Prueba nueva COVID + Influenza + VSR ayudará a estar preparados para la ‘tripledemia’
- IA elimina las conjeturas de las pruebas de flujo lateral
- Prueba de antígeno del SARS-CoV-2 más rápida, jamás diseñada, permite realizar pruebas de COVID-19 no invasivas en cualquier entorno
- Pruebas rápidas de antígeno detectan las variantes ómicron, delta del SARS-CoV-2
- Prueba en sangre realizada durante la infección inicial predice el riesgo de COVID prolongada
- Investigadores afirman que hay que crear “reservistas” de laboratorio para responder más rápidamente a la próxima pandemia
- Estudio encuentra que los profesionales sanitarios mostraron mayor interés en tecnologías POC durante la pandemia
- Plataforma de análisis de bajo costo para la COVID-19 combina sensibilidad de la PCR y velocidad de pruebas de antígeno
- Prueba de sangre por punción digital identifica inmunidad a la COVID-19
- Kit de prueba rápida determina inmunidad contra la COVID-19 y sus variantes
Canales
Química Clínica
ver canal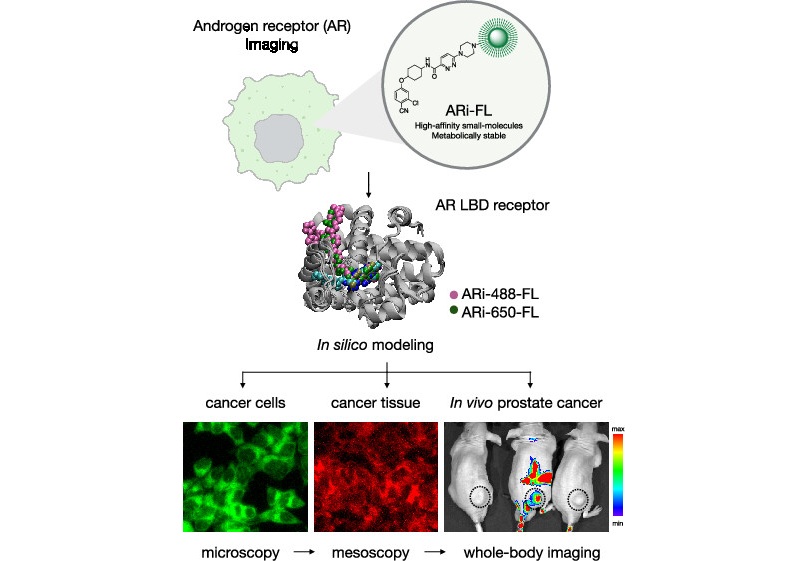
Sonda de imágenes químicas podría rastrear y tratar cáncer de próstata
El cáncer de próstata sigue siendo una de las principales causas de enfermedad y muerte en hombres, y muchos pacientes desarrollan resistencia a las terapias hormonales bloqueantes convencionales.... Más
Discrepancia entre dos pruebas comunes de función renal indica problemas de salud graves
La creatinina ha sido durante mucho tiempo el método estándar para medir la filtración renal, mientras que la cistatina C, una proteína producida por todas las células humanas, se ha recomendado como marcador... MásDiagnóstico Molecular
ver canal
Sencilla prueba de orina revolucionará diagnóstico y tratamiento del cáncer de vejiga
El cáncer de vejiga es uno de los cánceres urológicos más comunes y mortales, y se caracteriza por una alta tasa de recurrencia. El diagnóstico y el seguimiento aún... Más
Análisis snaguíneo para detección más temprana y sencilla de fibrosis hepática
El daño hepático persistente causado por el abuso de alcohol o infecciones virales puede desencadenar fibrosis hepática, una afección en la que el tejido sano se reemplaza gradualmente... MásHematología
ver canal
Análisis sanguíneo de actividad plaquetaria en mediana edad podría identificar riesgo temprano de Alzheimer
La detección temprana de la enfermedad de Alzheimer sigue siendo una de las mayores necesidades insatisfechas en neurología, sobre todo porque los cambios biológicos que subyacen al... Más
Medición de microvesículas podría detectar lesiones vasculares en pacientes con anemia falciforme
Evaluar la gravedad de la enfermedad de células falciformes (ECF) sigue siendo un reto, sobre todo al intentar predecir la hemólisis, el daño vascular y el riesgo de complicaciones... MásInmunología
ver canal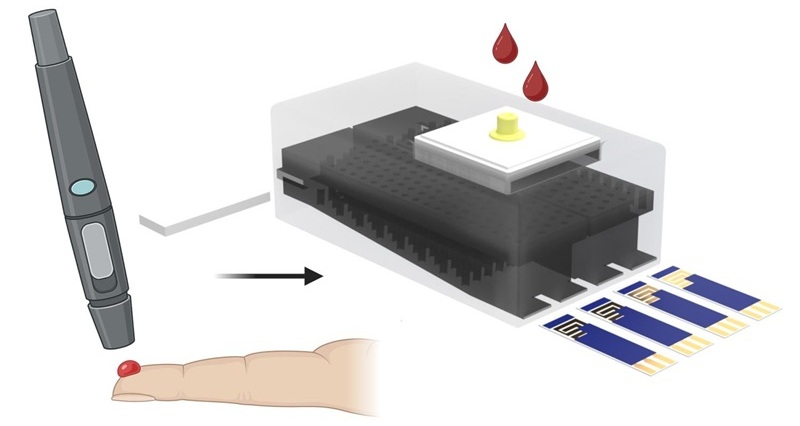
Nueva prueba distingue falsos positivos inducidos por vacuna de infección activa por VIH
Desde que se identificó el VIH en 1983, más de 91 millones de personas han contraído el virus y más de 44 millones han fallecido por causas relacionadas. Hoy en día, casi 40 millones de personas en todo... Más
Prueba de firma genética predice respuesta a tratamientos clave para cáncer de mama
Los inhibidores de DK4/6, combinados con terapia hormonal, se han convertido en un tratamiento fundamental para el cáncer de mama avanzado HR+/HER2–, ya que ralentizan el crecimiento tumoral... MásMicrobiología
ver canal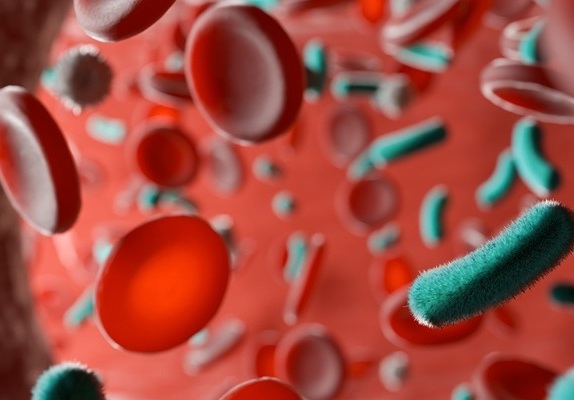
Prueba de diagnóstico rápido es estándar de oro para detección de sepsis
La sepsis causa la muerte de 11 millones de personas en todo el mundo cada año y genera enormes costos de atención médica. Solo en EUA y Europa, la sepsis representa 100.... MásPrueba rápida de tuberculosis POC proporciona resultados en 15 minutos
La tuberculosis sigue siendo una de las enfermedades infecciosas más mortales del mundo, y la reducción de nuevos casos depende de la identificación de las personas con infección... MásPatología
ver canal
Dispositivo de clasificación celular sintonizable tiene potencial para aplicaciones biomédicas
Aislar células cancerosas raras de la sangre es esencial para diagnosticar metástasis y orientar las decisiones terapéuticas, pero sigue siendo un desafío técnico.... MásHerramienta de IA mejora a medicos detectando anomalías en células sanguíneas
El diagnóstico de trastornos sanguíneos depende del reconocimiento de anomalías sutiles en el tamaño, la forma y la estructura celular. Sin embargo, este proceso es lento, subjetivo y requiere años de... Más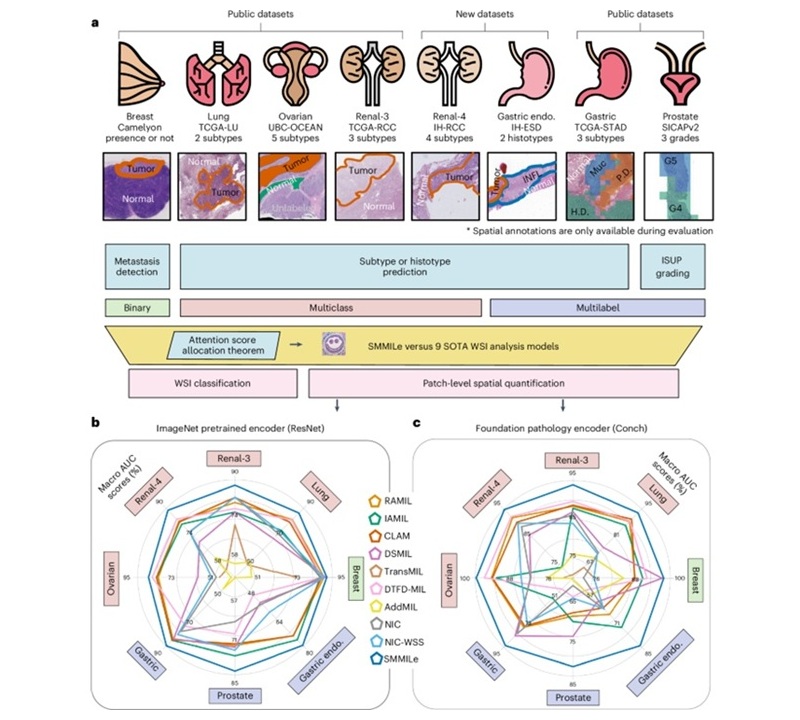
Herramienta de IA analiza rápidamente imágenes complejas de cáncer para tratamiento personalizado
Las imágenes complejas de biopsia digital, que normalmente requieren hasta 20 minutos para ser evaluadas por un patólogo experto, ahora pueden analizarse en aproximadamente un minuto mediante una nueva... MásTecnología
ver canal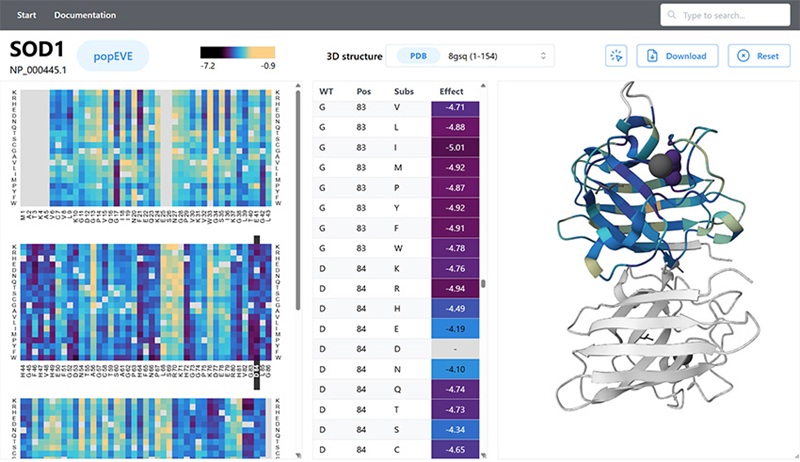
Modelo de inteligencia artificial podría acelerar diagnóstico de enfermedades raras
Identificar qué variantes genéticas causan enfermedades sigue siendo uno de los mayores desafíos de la medicina genómica. Cada persona porta decenas de miles de cambios en el... Más
Sensor de saliva con IA permite detección precoz del cáncer de cabeza y cuello
La detección precoz del cáncer de cabeza y cuello sigue siendo difícil porque la enfermedad produce pocos o ningún síntoma en sus primeras etapas, y las lesiones a menudo... MásIndustria
ver canal
Abbott adquiere Exact Sciences, empresa de detección de cáncer
Abbott (Abbott Park, IL, EUA) ha firmado un acuerdo definitivo para adquirir Exact Sciences (Madison, WI, EUA), lo que le permitirá entrar y liderar en segmentos de diagnóstico de cáncer... Más