Descubren biomarcador en sangre para enfermedades del espectro del autismo
Por el equipo editorial de LabMedica en español
Actualizado el 09 Mar 2021
El trastorno del espectro autista (TEA), un trastorno heterogéneo del neurodesarrollo, se caracteriza por déficits en la comunicación y la interacción social, con patrones de comportamiento, intereses o actividades restringidos y repetitivos. El TEA afecta al menos a uno de cada 59 niños en los EUA, aunque el valor sea, probablemente, mucho mayor.Actualizado el 09 Mar 2021
Se han investigado muchos candidatos a biomarcadores en sangre, incluidos neurotransmisores, citoquinas y marcadores de disfunción mitocondrial, estrés oxidativo y metilación alterada. Sin embargo, dada la prevalencia de los TEA, el uso del aprendizaje automático para incorporar datos demográficos y clínicos en el análisis podría examinar de manera más poderosa el estado de la enfermedad y la gravedad de los síntomas.
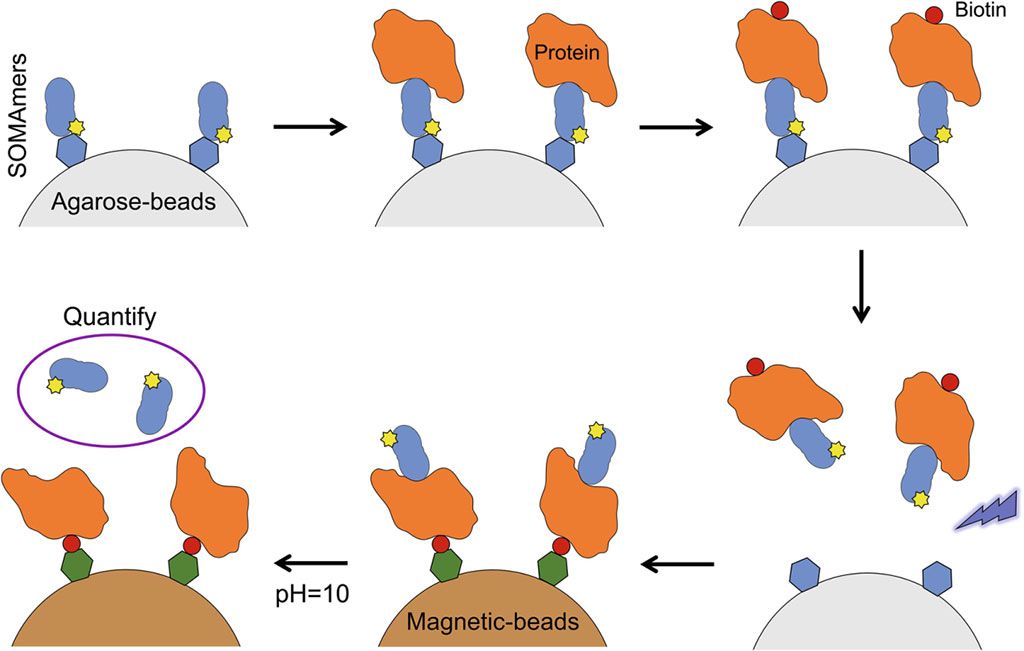
Imagen: El principio del Análisis SOMAscan que permite la detección simultánea de 1300 proteínas humanas utilizando los reactivos de unión a proteínas SOMAmer (aptámeros modificados de velocidad lenta) (Fotografía cortesía de SomaLogic).
Los científicos médicos del Centro Johnson para la Salud y el Desarrollo Infantil (Austin, TX, EUA), inscribieron a un total de 154 pacientes pediátricos masculinos. El grupo de TEA estaba compuesto por 76 pacientes con una edad media de 5,6 años ± 1,7 años. El grupo de desarrollo típico (DT) estaba compuesto por 78 pacientes con una edad media de 5,7 años ± 2,0 años. El desglose étnico fue el siguiente: 73 blancos/caucásicos, 32 hispanos/latinos, 17 afroamericanos/negros, cinco asiáticos o isleños del Pacífico, 23 etnias múltiples u otras, y cuatro no informados.
Se realizó una extracción de sangre en ayunas en los pacientes con TEA y DT entre las 8 y las 10 de la mañana en un tubo de separación de suero de 3,5 ml utilizando una técnica de venopunción estándar. Se utilizó la plataforma SOMAScan 1.3k para el análisis y se procesaron los ensayos (SomaLogic, Boulder, CO, EUA). Los reactivos aptámeros SOMAmer consisten en secuencias cortas de ADN monocatenario con apéndices “similares a proteínas” que permiten una unión estrecha y específica a las proteínas objetivo. Se examinaron más de 1.100 proteínas utilizando la plataforma de análisis de proteínas SomaLogic. Se identificó un panel de nueve proteínas como óptimo para predecir los TEA mediante tres métodos computacionales. Luego, los científicos evaluaron la calidad del panel de biomarcadores utilizando métodos de aprendizaje automático.
El equipo informó que cinco proteínas eran comunes a los tres modelos de predicción utilizados: la proteína quinasa 14 activada por mitógenos (MAPK14), la inmunoglobulina D (IgD), la dermatopontina (DERM), el receptor 2 de efrina tipo B (EPHB2) y la uroquinasa soluble tipo receptor activador del plasminógeno (suPAR). Estas cinco proteínas se definieron como proteínas centrales. Cuatro proteínas que proporcionan poder aditivo se combinaron con las cinco proteínas centrales y, juntas, las nueve proteínas, dieron como resultado un AUC del 86% (sensibilidad 83%; especificidad 84%). Estas proteínas tienen una importancia de vía relacionada con varios procesos, incluida la regulación negativa de CD8+, la proliferación de células T alfa-beta, la respuesta inmune, la retracción de la proyección de las neuronas, la actividad de MAPK14 y la señalización del receptor de glutamato, todos los cuales han sido asociados previamente con los TEA.
Dwight German, PhD, profesor de psiquiatría y autor principal del estudio, dijo: “Cuanto más afectado está el niño, el valor del biomarcador sanguíneo es más alto o más bajo. Idealmente, habrá un día en el que un niño sea identificado mediante biomarcadores sanguíneos como en riesgo de desarrollar TEA para que las terapias se puedan iniciar de inmediato. Eso ayudaría al niño a desarrollar habilidades para optimizar su comunicación y aprendizaje”.
Los autores concluyeron que las nueve proteínas eran significativamente diferentes en los niños con TEA en comparación con los niños con DT y se correlacionaron significativamente con la gravedad del TEA según lo medido por las puntuaciones totales del Programa de Observación de Diagnóstico de Autismo (ADOS). Utilizando métodos de aprendizaje automático, se identificó un panel de proteínas séricas que puede ser útil como biomarcador sanguíneo para el TEA en los niños. El estudio fue publicado el 24 de febrero de 2021 en la revista PLOS ONE.
Enlace relacionado:
Centro Johnson para la Salud y el Desarrollo Infantil
SomaLogic