Pruebas de IA de precisión ofrecen información de riesgo de cáncer a partir de láminas H&E rutinarias
Actualizado el 23 Apr 2026
La obtención de perfiles pronósticos fiables y el cribado de biomarcadores son esenciales para guiar las decisiones terapéuticas en oncología, mientras los laboratorios deben equilibrar la rapidez con las limitaciones de recursos. La identificación más temprana de cáncer de mama de alto riesgo y la evaluación rápida de la inestabilidad de microsatélites (MSI) en cáncer colorrectal pueden apoyar la atención personalizada y optimizar los flujos de trabajo. Un nuevo par de pruebas de inteligencia artificial, recientemente autorizadas, permite ahora su uso clínico en toda la Unión Europea tras obtener el marcado CE bajo el IVDR europeo, lo que facilita su implementación en la práctica rutinaria.
Waiv (anteriormente Owkin Dx) ha obtenido la marca CE-IVDR para dos pruebas de precisión basadas en IA: RlapsRisk BC para la elaboración de perfiles de riesgo pronóstico del cáncer de mama y MSIntuit CRC para la detección de MSI en el cáncer colorrectal. Esta autorización permite su implementación clínica en todos los estados miembros de la Unión Europea. Ambas pruebas están disponibles para los laboratorios a través de Destra, una plataforma de patología digital interoperable, o mediante su integración en los flujos de trabajo existentes.
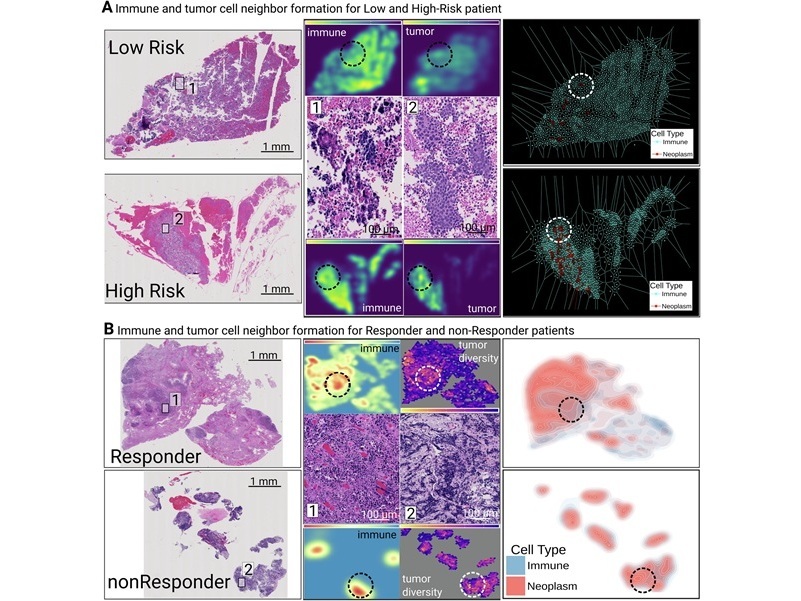
RlapsRisk BC predice el riesgo de recaída del cáncer de mama directamente a partir de muestras histopatológicas estándar. Este método tiene el potencial de proporcionar información sobre el perfil de riesgo a nivel genómico sin necesidad de realizar pruebas adicionales exhaustivas. Al identificar precozmente a las pacientes de alto riesgo, permite tomar decisiones de tratamiento más informadas y personalizadas, y puede ayudar a dirigir las terapias agresivas donde sea necesario, evitando tratamientos innecesarios a las pacientes de menor riesgo.
MSIntuit CRC aplica un enfoque de precisión basado en IA para ofrecer una detección rápida y escalable de MSI a partir de preparaciones histológicas teñidas con hematoxilina y eosina. Al integrarse en los flujos de trabajo de pruebas rutinarias, identifica y descarta rápidamente a los pacientes sin MSI, con el objetivo de optimizar el proceso para toda la población de pacientes. El diseño busca mejorar los tiempos de respuesta y optimizar el uso de recursos, abordando un biomarcador fundamental para identificar a los pacientes que probablemente se beneficien de la inmunoterapia y ayudando a acelerar el acceso a tratamientos más específicos.
Ambas pruebas obtuvieron la marca CE conforme al Reglamento Europeo de Diagnóstico In Vitro (IVDR). La certificación IVDR exige una amplia evidencia clínica, una sólida validación del rendimiento y una supervisión continua posterior a la comercialización. Los laboratorios pueden acceder a las pruebas a través de Destra, que es compatible con los principales sistemas de espectrometría de masas integrada (IMS) y sistemas de visualización, incluidos Proscia, Roche Diagnostics, Sectra y Tribun Health.
"Obtener la marca CE-IVD según IVDR supone un hito para Waiv. Esta certificación refleja no solo el rigor científico y clínico que respalda nuestros modelos, sino también el trabajo dedicado a transformar la innovación en IA en productos que puedan tener un impacto significativo en la atención al paciente, " declaró Meriem Sefta, CEO y cofundadora de Waiv.
"Estamos implementando pruebas de precisión basadas en IA, validadas clínicamente, en la práctica oncológica diaria, preparadas para apoyar el desarrollo de fármacos y las colaboraciones en diagnósticos complementarios que se avecinan. Esta es una ambición global".
Enlaces relacionados
WAIV




.jpg)







_image.png)