Firmas de microARN en sangre diferencian a los individuos con cáncer de pulmón
Por el equipo editorial de LabMedica en español
Actualizado el 18 Mar 2020
La baja tasa de supervivencia general de los pacientes con cáncer de pulmón requiere herramientas de detección mejoradas para permitir mejores opciones de tratamiento y mejores resultados para los pacientes. El cáncer de pulmón afecta a unas 228.000 personas al año en los EUA y tiene una tasa de supervivencia a cinco años de apenas el 20%.Actualizado el 18 Mar 2020
Las firmas moleculares multivariables, como las firmas de microARN transmitidas por la sangre (miARN), pueden tener altas tasas de sensibilidad y especificidad, pero requieren estudios adicionales con grandes cohortes y mediciones estandarizadas para confirmar la generalización de las firmas de miARN. Las firmas de microARN parecen diferenciar a los individuos con cáncer de pulmón de aquellos con otras enfermedades pulmonares, así como de aquellos sin afección pulmonar.
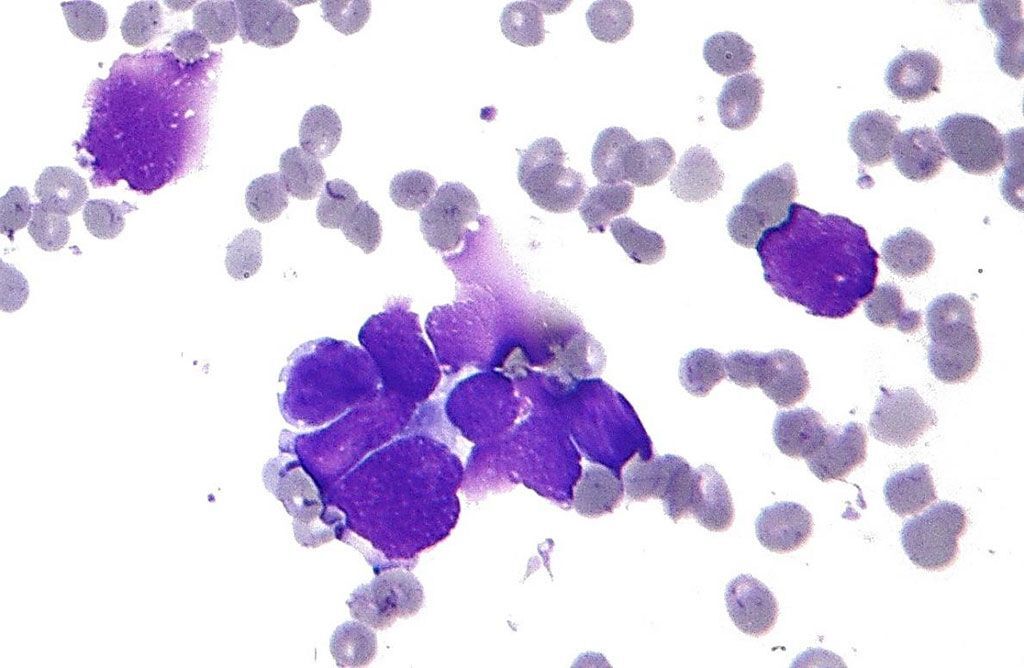
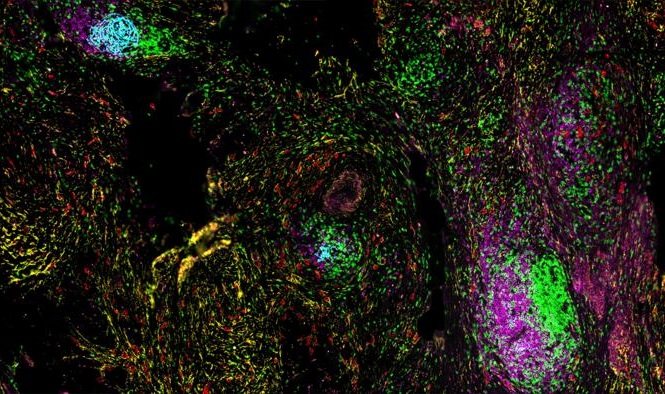
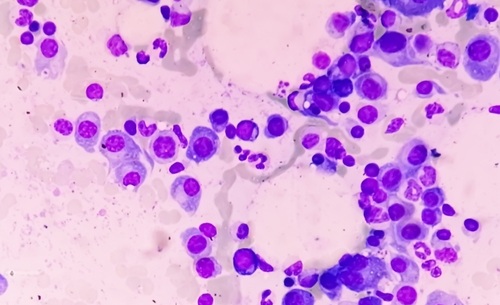
Imagen: Histopatología que muestra las características clave del carcinoma de pulmón de células pequeñas (CPCNM): moldeo nuclear; cromatina de sal y pimienta; y escaso citoplasma (Fotografía cortesía de Nephron).
Un gran equipo de científicos que colaboran con la Universidad de Saarland (Saarbrücken, Alemania) investigó el uso de miARN transmitidos por la sangre como posibles marcadores circulantes para detectar el cáncer de pulmón en una cohorte extendida de pacientes sintomáticos y participantes de control. Se obtuvieron diagnósticos clínicos para 3.046 pacientes (606 pacientes con cáncer de pulmón de células no pequeñas y de células pequeñas, 593 pacientes con enfermedades pulmonares no tumorales, 883 pacientes con enfermedades que no afectan el pulmón y 964 participantes control, no afectados). El equipo calculó la sensibilidad y especificidad de la biopsia líquida utilizando firmas de miARN para la detección del cáncer de pulmón. Las muestras de sangre recolectadas de los participantes se sometieron a un perfil de miARN en todo el genoma utilizando microarrays de miARN humanos.
Los investigadores dividieron su cohorte en conjuntos de entrenamiento y validación de igual tamaño. Dentro del conjunto de entrenamiento, descubrieron una firma de 15 miARN que podría diferenciar a los pacientes con cáncer de pulmón de todos los demás individuos. En el conjunto de validación, esta firma podría diagnosticar el cáncer de pulmón con una exactitud del 91,4%, una sensibilidad del 82,8% y una especificidad del 93,5%. Del mismo modo, descubrieron una firma de 14 miARN que podría distinguir a los pacientes con cáncer de pulmón de aquellos con una enfermedad pulmonar no tumoral con una exactitud del 92,5%, sensibilidad del 96,4% y especificidad del 88,6%. Una tercera firma de 14 miARN podría diferenciar a los pacientes con cáncer de pulmón en estadio temprano de todos los demás pacientes con una exactitud del 95,9%, una sensibilidad del 76,3% y una especificidad del 97,5%. Aunque el equipo se centró en los biomarcadores generales del cáncer de pulmón, notaron que el miARN hsa-miR-30a-5p era capaz de diferenciar mejor el cáncer de pulmón de células pequeñas y el cáncer de pulmón de células no pequeñas.
Los autores concluyeron que su estudio sugirió que se pueden usar los patrones identificados de miARN como un componente de una prueba de cáncer de pulmón mínimamente invasiva, complementando las imágenes, la citología del esputo y las biopsias. El estudio fue publicado el 5 de marzo de 2020 en la revista JAMA Oncology.
Enlace relacionado:
Universidad de Saarland