Biopsia en líquido cefalorraquídeo caracteriza tumores cerebrales
Por el equipo editorial de LabMedica en español
Actualizado el 16 Dec 2015
La explotación del ADN circulante en líquido cefalorraquídeo (LCR) como biopsia líquida promete ser un método más exacto, eficaz y menos invasivo para desenmascarar las características moleculares de los tumores cerebrales.Actualizado el 16 Dec 2015
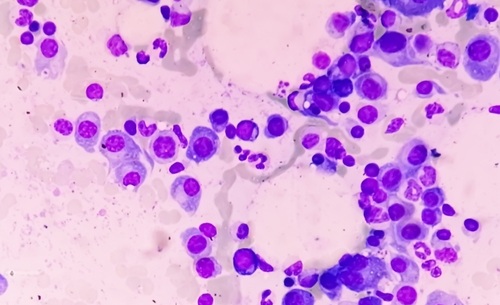
El uso delLCR como biopsia líquida tiene el potencial para el pronóstico, el tratamiento, la identificación y seguimiento de las alteraciones genómicas en los tumores cerebrales no sólo en tiempo real, sino con el tiempo. Las concentraciones de ADN circulante de los tumores del sistema nervioso central son muy bajas en plasma, pero muy altas en el LCR.
Un equipo internacional de científicos liderado por los que están en el Instituto Vall d'Hebron de Oncología (VHIO, Barcelona, España) realizó la secuenciación de todo el exoma de 86 metástasis cerebrales emparejadas, tumores primarios y tejido normal. En 15 de estos casos, se recogieron muestras adicionales, incluyendo siete casos de lesiones múltiples de metástasis cerebral y ocho casos de lesiones extracraneales con metástasis en los ganglios linfáticos regionales, metástasis extracraneales, o tejido adicional de un tumor primario. Unos neuropatólogos certificadosconfirmaron los diagnósticos histológicos y seleccionaron muestras frescas representativas, fijadas en formol e incluidas en parafina, que tenían una pureza estimada de igual o superior al 40%.
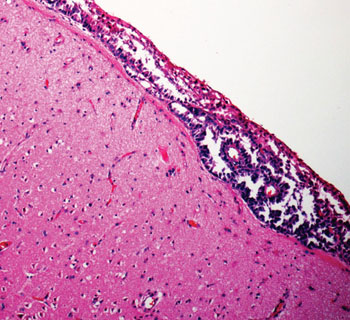
El equipo realizó la secuenciación de todo el exoma del tejido extraído usando los analizadores HiSeq o GenomeAnalyzer IIX (Illumina, San Diego, CA, EUA).También realizaron la secuenciación profunda dirigida (profundidad mediana 455X) en un subconjunto de muestras de tumores primarios utilizando la plataforma Illumina HiSeq. Adicionalmente se usó la inmunohistoquímica para HER2/NEU para validar la amplificación del receptor de tirosina quinasa 2, erb-b2 (ERBB2) en las metástasis cerebrales y el tumor primario en un caso. El estudio se enfocó también en la carcinomatosis leptomeníngea, la infiltración tumoral de la película fina que cubre el cerebro y la médula espinal y que se produce como metástasis de otros tumores.
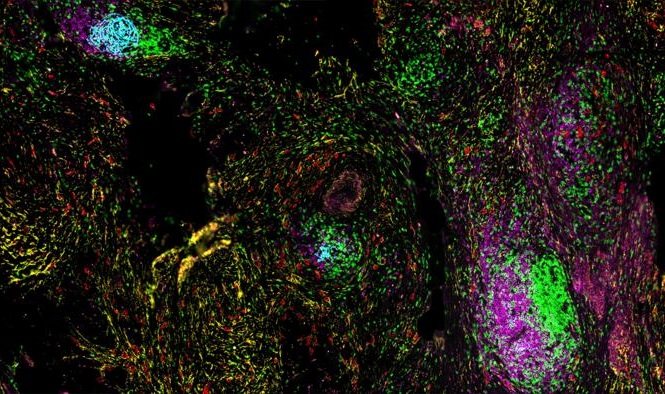
Los científicos, observaron la evolución ramificada en todas las muestras de cáncer relacionadas clonalmente, donde todos los sitios primarios y de metástasis compartían un ancestro común, pero seguían evolucionando de forma independiente. En el 53% de los casos, encontraron alteraciones potencialmente informativas, clínicamente, en las metástasis cerebrales no detectadas en la muestra de tumor primario emparejado. En contraste, los sitios de metástasis cerebrales espacial y temporalmente separados eran genéticamente homogéneos. Las metástasis de los ganglios linfáticos extracraneales y regionales distales, eran muy divergentes de las metástasis cerebrales. Los científicos detectaron alteraciones asociadas con la sensibilidad a los inhibidores de PI3K/AKT/mTOR, CDK, y de HER2/EGFR en las metástasis cerebrales. El análisis genómico de las metástasis cerebrales ofrece una oportunidad para identificar alteraciones potencialmente clínicamente informativas no detectadas en los tumores primarios clínicamente muestreados, los ganglios linfáticos regionales o las metástasis extracraneales.
Joan Seoane, PhD, una profesora y Directora de Investigación Traslacional en el VHIO, dijo: “Nuestra principal limitación fue que los niveles circulantes de ADN tumoral de los tumores cerebrales son muy bajos en el plasma. Pero el cerebro tiene su propio circuito cerrado de líquido, el líquido cefalorraquídeo, que baña el cerebro y la médula espinal, y por lo tanto está en contacto directo con las células tumorales y encontramos circulando el ADN tumoral en el LCR a niveles tan altos que hemos sido capaces de detectar y caracterizar los tumores con un alto grado de sensibilidad”.El estudio fue publicado el 26 de septiembre de 2015, en la revista Cancer Discovery.
Enlaces relacionados:
Vall d´Hebron Institute of Oncology
Illumina